
题目列表(包括答案和解析)
7、下列物质中与某些酸、碱、盐都能起反应的是( )
A、碳酸钙 B、碳酸钠 C、稀硫酸 D、氢氧化钠
6、有锌、稀硫酸、氧化铜、氯化铜溶液、氢氧化钠溶液、氯化钡溶液,常温下两两温混合,共能发生的化学反应有( )
A、4个 B、5个 C、6个 D、7个
5、把一氧化碳和二氧化碳的混合气体20克,通入足量石灰水中产生沉淀10克,则原混合气体中一氧化碳质量为( )
A、4.4克 B、15.6克 C、7.8克 D、无法计算
4、欲除去混入一氧化碳中的少量水蒸气、氧气、二氧化碳,应通过下列哪组物质( )
A、加热的铜丝网,浓硫酸,氢氧化钠溶液B、氢氧化钠溶液,浓硫酸,加热的铜丝网
C、浓硫酸,氢氧化钠溶液,加热的铜丝网D、加热的铜丝网,氢氧化钠溶液,浓硫酸
3、下列各种说法中,错误的是( )
A、空气成分中,以氮气的体积分数最大B、地壳中所含硅元素的质量分数最大
C、常温下,氢气是最轻的气体 D、白磷在空气中由于缓慢氧化而易自燃
2、已知同温同压下等体积的不同气体含有相同的分子数,又知空气中混入氢气的体积达到总体积的4%~74.2%时点燃就会发生爆炸,下面列出了氢气混入空气时所占的不同体积分数。按理论计算爆炸最猛烈的可能是( )
A、氢气占10% B、氢气占29% C、氢气占50% D、氢气占70%
1、在阳光下的松林中,部分氧气转变成臭氧,下列有关说法正确的是( )
A、这一变化属于物理变化 B、氧气和臭氧是同一种物质
C、这一变化是化学变化 D、空气中的氧气和生成的臭氧质量相等
19、镁是重要的金属材料,广泛应用于合金、火箭和飞机制造业,世界上大部分镁是从海水中提取的。威海是一座滨海城市,海岸线长达1000 km,海水资源丰富。某校学习小组的同学对家乡附近海水中镁元素的含量进行测定。称取海水100kg,然后再加入足量的氢氧化钠溶液,过滤、干燥、称量后得到沉淀质量见下表。(重复实验三次)。
|
|
第一次实验 |
第二次实验 |
第三次实验 |
|
所取海水质量/kg |
100 |
100 |
100 |
|
生成沉淀质量/kg |
0.28 |
0.29 |
0.30 |
试计算海水中镁元素的质量分数。
(假定海水中镁元素全部以氯化镁的形式存在,不考虑沉淀中杂质的干扰)。
专题二 身边的化学物质B
18、实验室里某小组正在探究一个问题。根据设计方案,小英向试管中加入2mL氢氧化钠溶液,滴入几滴酚酞溶液,溶液显红色。然后她又用滴管连续滴入一定量的稀硫酸,溶液由红色变为无色。
(1)他们探究的问题是____________(填Ⅰ或Ⅱ)
Ⅰ.酚酞溶液遇酸、碱溶液能显示不同颜色吗?
Ⅱ.酸和碱溶液能发生反应吗?
(2)大家对小英得到的无色溶液继续探究。小斌认为反应后溶液中的溶质是硫酸钠,小亮认为溶质有两种,它们是________________________。同学们根据以下两种方案进行实验后,一致认为小亮的观点是正确的。请你补填下表的空缺。
|
实验操作 |
实验现象 |
实验结论 |
|
方案一:取少许反应后的 溶液置于试管中,向其中加入________ |
|
小亮的观点正确 |
|
方案二:取少许反应后的 溶液置于试管中,向其中加入________ |
|
(3)请你和全组同学一起分析以下问题。

①稀硫酸和氢氧化钠溶液发生反应的微观过程如图1所示。从粒子的角度具体分析该反应能发生的原因是_____________________________________。
②锌和硫酸铜溶液发生反应的微观过程如图2所示。从粒子的角度具体分析该变化是化学变化的原因是____________________________________。
③通过以上分析,揭示出化学反应的微观本质是___________________________。
17、某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道:
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 。
[提出问题]能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
[实验验证]如图16是该学习小组进行模拟实验时所用到的部分主要装置。已知浓氨水遇生石灰会产生大量的NH3。

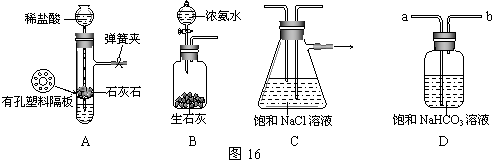
请回答下列问题:
⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若
,说明装置不漏气。
⑵ D是连接在装置A与装置C之间的气体净化装置,进气口是 (填a或b),D的作用是除去__________气体。
⑶ 实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是___________。(填写序号)
① 使CO2更易被吸收 ② NH3比CO2更易制取 ③ CO2的密度比NH3大
⑷ 用____________的方法将生成的NaHCO3晶体从混合物中分离出来。
[得出结论]利用“侯氏制碱法”在实验室可以制取NaHCO3 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com