
题目列表(包括答案和解析)
5.解 设该结晶水合物的化学式为M2SO4·nH2O,M的相对原子质量为x
M2SO4+BaCl2===2MCl+BaSO4↓
2x+96 233
4.(1)设Na2CO3的质量为x,反应生成NaCl的质量为y,稀盐酸的质量为w,则
Na2CO3 + 2HCl===2NaCl+H2O+CO2↑
106 2×36.5 2×58.5 44
x W·10% y 8.8克
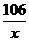 =
=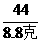 x=21.2克(Na2CO3)
x=21.2克(Na2CO3) 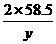 =
=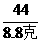 y=23.4克
y=23.4克
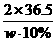 =
=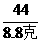 w=146克
w=146克
原来有NaCl;25.8克-21.2克=4.6克
(2)NaCl=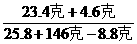 ×100%=17.2%
×100%=17.2%
(3)设加入质量为m的NaCl恰好饱和: 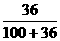 =
=
m=20.6克
97.5克 100克
40克+y 60克
y=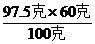 =40克
=40克
y=18.5克
答:略
3.分析 题目未标明是否饱和,只能按不饱和溶液处理,如用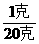 =
=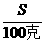 公式计算就会发生错误。
公式计算就会发生错误。
解 (1)设t℃时KNO3的溶解度为S
在100克40%的KNO3溶液中
含溶质质量=40%×100克=40克
含溶剂质量=100克-40克=60克
当蒸发20克水后析出晶体1克此时溶液达到饱和。
溶质 溶剂
40克-1克 60克-20克
S 100克
S=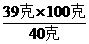 =97.5克
=97.5克
(2)设t℃时在100克40%的KNO3溶液中加入KNO3晶体质量为y时,溶液恰好饱和
溶质 溶 剂
2.解 溶质的质量分数=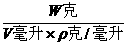 ×100%=
×100%=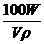 %
%
该湿度下的溶解度
溶质 溶剂 溶液
W克 Vρ-W克 Vρ克
S 100克
则S=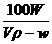 克
克
1.分析 在一定湿度下不饱和溶液蒸发溶剂没有晶体析出,只能使溶液浓缩,当继续蒸发形成饱和溶液后,再蒸发溶剂,过多的溶质就会析出。60℃的硝酸钾溶液500克未注明是否饱和,若为饱和溶液析出晶体的质量为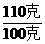 =
=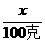 x=11克;若为不饱和溶液析出晶体的质量将小于11克,甚至没有晶体析出。
x=11克;若为不饱和溶液析出晶体的质量将小于11克,甚至没有晶体析出。
解 应选C。
7.质量分数为63%的硝酸W克,跟质量分数为56%的氢氧化钾溶液恰好完全反应。求
(1)该氢氧化钾溶液的质量;
(2)反应后溶液中水的质量;
(3)欲在38℃获得0.5W克硝酸钾晶体,需蒸发的水的质量(38℃时硝酸钾的溶解度是60克)
答案与提示
6.将11.2克氧化钙加到50克盐酸中,使氧化钙完全反应,此时溶液的pH值小于,当再加入4克10%的氢氧化钠溶液,溶液的pH值等于7,求此盐酸的溶质的质量分数。
5.某一价金属硫酸盐的结晶水合物6.44克,加热到结晶水全部失去,其质量减少55.9%。将加热后的固体全部溶于水,加入过量的氯化钡可得到沉淀4.66克,通过计算(查原子量表)确定结晶水合物的化学式。
4.向25.8克含有少量NaCl杂质的Na2CO3的白色固体中,慢慢加入10%的稀盐酸到恰好不再产生气体为止,共收集到干燥的CO2气体8.8克。求:
(1)白色固体中Na2CO3的质量是多少?
(2)所得溶液中NaCl的质量分数是多少?
(3)若要使所得溶液在20℃时成为饱和溶液,还需加入NaCl固体的质量是多少?(20℃时NaCl的溶液度为36克).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com