
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
18Θ°(2Ζ÷)ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΔΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
17Θ°(2Ζ÷)ΓΓ ______ΓΓ __ΓΓ ____; ____ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ __ΓΘ
24.ΓΑΫΎΡήΦθ≈≈Γ±“―Ψ≠“ΐΤπΒ±Ϋώ…γΜαΤ’±ιΙΊΉΔΓΘΜ· ·»ΦΝœ»Φ…’Μα≤ζ…ζ¥σΝΩΒΡCO2Θ§¥σΤχ÷–CO2Κ§ΝΩΙΐΗΏΜαΒΦ÷¬Έ¬ “–ß”ΠΒ»ΜΖΨ≥Έ ΧβΓΘ
(1)ΓΓ ΦΤΥψ1000g CH4Άξ»Ϊ»Φ…’≤ζ…ζCO2ΒΡ÷ ΝΩmΘΜ
(2)¥”œ¬±μ ΐΨίΖ÷ΈωΘ§”κΟΚœύ±»Θ§”ΟΧλ»ΜΤχΉω»ΦΝœΒΡ”≈Βψ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓ ΓΓΓΘ
|
ΓΓ |
1000g Έο÷ Άξ»Ϊ»Φ…’≤ζ…ζCO2ΒΡ÷ ΝΩ |
1000g Έο÷ Άξ»Ϊ»Φ…’Ζ≈≥ωΒΡ»»ΝΩ |
|
CH4 |
m |
5.6ΓΝ104KJ |
|
C |
3.67ΓΝ103g |
3.2ΓΝ104KJ |
2010-2011―ßΡξΕ»≥θ»ΐΜ·―ßΒΎ»ΐ¥ΈΡΘΡβΩΦ ‘¥πΧβΨμ
Ω…Ρή”ΟΒΫΒΡœύΕ‘‘≠Ή”÷ ΝΩ”–ΘΚC-12ΓΓ H-1ΓΓ O-16ΓΓ S-32ΓΓΓΓ Mg-24
23Θ°(11Ζ÷)“―÷ΣΡ≥Ϋπ τX”–œ¬Ν–œύΙΊ–≈œΔΘΚΔΌΥϋΒΡ÷ς“ΣΩσΈοΒΡΜ·―ß≥…Ζ÷ «X2O3ΘΜΔΎΥϋ÷ς“ΣΆ®Ιΐ»»ΜΙ‘≠Ζ®“±ΝΕΕχ≥…ΘΜΔέΥϋΒΡΡξ≤ζΝΩΈΜ”ΎΫπ τ÷° ΉΓΘ
(1)Ψί¥ΥΆΤΕœX «ΓΓΓΓΓΓΓΓΓΓΓΓ (Χν―ΓœνΉ÷ΡΗ)ΓΘ
ΓΓΓΓ AΘ°ν―ΓΓΓΓΓΓ BΘ°ΧζΓΓΓΓΓΓ CΘ°¬ΝΓΓΓΓΓΓ DΘ°Ά≠
(2)‘ΎΗΏ¬·÷–”ΟΚ§X2O3ΒΡΩσΈο“±ΝΕΗΟΫπ τΒΡ‘≠άμ «ΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (”ΟΜ·―ßΖΫ≥Χ Ϋ±μ Ψ)ΓΘ
(3)ΒγΜ·―ßΗ· ¥ «Ϋπ τΗ· ¥ΒΡ÷ς“Σ‘≠“ρΓΘΒ±ΝΫ÷÷ΜνΤΟ–‘≤ΜΆ§ΒΡΫπ τ‘Ύ≥± ΣΒΡΜΖΨ≥÷–Ϋ”¥Ξ ±Θ§“ρ–Έ≥…‘≠Βγ≥ΊΘ§ΜνΤΟ–‘«ΩΒΡΫπ τ Ήœ»±ΜΗ· ¥ΓΘάϊ”Ο’β“Μ‘≠άμΘ§ΈΣΝΥ±ΘΜΛ¬÷¥§ΒΡΗ÷÷ ΆβΩ«Θ§Ά®≥Θ‘Ύ–– ΜΒΡ¬÷¥§ΆβΩ«…œΝ§Ϋ”_____ΓΓΓΓ _______ (ΧνΓΑΆ≠ΑεΓ±ΓΔΓΑ–ΩΑεΓ±)ΓΘ
ΓΓΓΓ (4)ΈΣΝΥ¬ζΉψΡ≥–©ΦβΕΥΦΦ θΖΔ’ΙΒΡ–η“ΣΘ§»ΥΟ«”÷Κœ≥…ΝΥ–μΕύ–¬–ΆΚœΫπ≤ΡΝœΓΘ¥Δ«βΚœΫπ «“ΜάύΡήΙΜ¥σΝΩΈϋ ’H2Θ§≤Δ”κH2ΫαΚœ≥…Ϋπ τ«βΜ·ΈοΒΡ≤ΡΝœΓΘ¥ΥΙΐ≥ΧΖΔ…ζΝΥ____________±δΜ·(ΧνΓΑΈοάμΓ±ΓΔΓΑΜ·―ßΓ±)Θ§¥Δ«βΚœΫπ τ”Ύ__________ (ΧνΓΑ¥ΩΨΜΈοΓ±ΓΔΓΑΜλΚœΈοΓ±)ΓΘ
(5)ΗυΨίΧζΓΔΆ≠ΓΔ¬Ν»ΐ÷÷Ϋπ τΒΡΜνΕ·Υ≥–ρ≈–Εœœ¬Ν–Μ·―ßΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓ (Χν–ρΚ≈)ΓΘ
ΔΌ3Fe+2AlCl3=3FeCl2+2AlΓΓ ΔΎ3Cu+2AlCl3=3CuCl2+2AlΓΓ ΔέFe+CuCl2=FeCl2+Cu
(6)Ρ≥ Β―ι “Ζœ“Κ÷–Κ§”–HClΓΔFeCl2ΚΆCuCl2Β»Έο÷ Θ§»τœρΤδ÷–Φ”»κ…‘ΙΐΝΩΒΡΧζΖέΘ§≥δΖ÷Ζ¥”ΠΚσΙΐ¬ΥΘ§‘ρ¬Υ‘ϋ÷–Κ§”–ΓΓ ΓΓΓΓΓΓΓΓΓΓ(ΧνΜ·―ß Ϋ)ΓΘ
ΓΓ(7)Ά§―ßΟ«…ηΦΤΝΥ»γœ¬ Β―ιΖΫΑΗ≤βΕ®ΗΟΩσΈο÷–X2O3ΒΡ÷ ΝΩΖ÷ ΐ(ΉΑ÷ΟΤχΟή–‘ΝΦΚΟΘΜΩσΈο÷–ΒΡ‘”÷ ≤Μ≤ΈΦ”Ζ¥”ΠΘΜΦΌ…ηΩσΈο―υΤΖ÷–ΒΡX2O3Άξ»ΪΖ¥”Π)ΘΚ
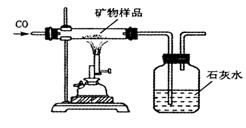 ΔΌ»ΓΩσΈο―υΤΖ≤Δ≥ΤΝΩΗΟ―υΤΖΒΡ÷ ΝΩΘΜ
ΔΌ»ΓΩσΈο―υΤΖ≤Δ≥ΤΝΩΗΟ―υΤΖΒΡ÷ ΝΩΘΜ
ΔΎ≤β≥ωΖ¥”Π«ΑΙψΩΎΤΩΚΆΤΩΡΎΈο÷ Ήή÷ ΝΩΘΜ
Δέ≤β≥ωΖ¥”ΠΚσΙψΩΎΤΩΚΆΤΩΡΎΈο÷ Ήή÷ ΝΩΘΜ
ΔήΦΤΥψΒΟ≥ωΩσΈο―υΤΖ÷–x2O3ΒΡ÷ ΝΩΖ÷ ΐΓΘ
Ρψ»œΈΣΘ§ΗΟ Β―ιΖΫΑΗΓΓΓΓΓΓΓΓΓΓ (ΧνΓΑ“ΜΕ®Γ±Μρ
ΓΑ≤Μ“ΜΕ®Γ±)ΡήΉΦ»Ζ≤β≥ωΩσΈο÷–X2O3ΒΡ÷ ΝΩΖ÷ ΐΘ§άμ”… «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
≤ΜΗΡ±δΉΑ÷ΟΚΆ“©ΤΖΘ§ΡψΜΙΩ…“‘Ά®Ιΐ≤βΕ®ΡΡ–© ΐΨίΘ§‘ΌΆ®ΙΐΦΤΥψΒΟ≥ωΩσΈο÷–X2O3ΒΡ÷ ΝΩΖ÷ ΐΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
¥”ΜΖ±ΘΫ«Ε»Ω¥Θ§ΗΟΉΑ÷ΟΒΡ≤ΜΉψ÷°¥Π «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
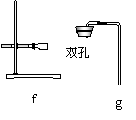
22Θ°(8Ζ÷) Β―ι “”–»γœ¬ΒΡ Β―ι“«ΤςΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
 |
|||||||||||||
 |
|||||||||||||
 |
|||||||||||||
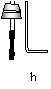 |
|||||||||||||
 |
|||||||||||||
|
|||||||||||||
|
|||||||||||||

ΔΌ―Γ‘ώ…œΆΦ÷–ΒΡ“«ΤςΉιΉΑ“ΜΧΉΦ”»»ΙΧΧε÷Τ»Γ―θΤχ≤Δ”Ο≈≈Υ°Ζ® ’Φ·ΒΡ Β―ιΉΑ÷ΟΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (Χν“«Τς–ρΚ≈)Θ§÷ΤΤχ ±ΗΟΉΑ÷ΟΡΎΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎ“Σ»Ζ±Θ”Ο≈≈Υ°Ζ® ’Φ·ΒΫΒΡ―θΤχΫœ¥ΩΘ§ ’Φ· ±“ΣΉΔ“βΒΡΝΫΒψ «ΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
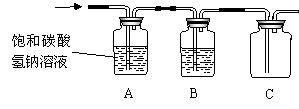
(2)ΈΣΒΟΒΫ¥ΩΨΜΗ…‘οΒΡCO2Θ§ΫΪ Β―ι “÷–÷ΤΒΟΒΡCO2“ά¥ΈΆ®Ιΐ»γœ¬ΉΑ÷ΟΘΚ
 ΓΓ
ΓΓ
ΔΌΉΑ÷ΟAΒΡΉς”ΟΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎΉΑ÷ΟBΡΎΉΑΒΡ“©ΤΖ «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔέΫΪΒψ»ΦΒΡΟΨΧθ…λΫχΦ·¬ζCO2ΒΡΦ·ΤχΤΩC÷–Θ§ΟΨΧθΨγΝ“»Φ…’Θ§ΤΩΡΎ”–ΑΉ…ΪΚΆΚΎ…ΪΝΫ÷÷ΙΧΧεΈο÷ …ζ≥…Θ§Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
Ά®ΙΐΗΟ Β―ιΡψΒΟΒΫΒΡ“ΜΒψΤτΖΔ «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
21Θ°(6Ζ÷)Ζ÷άύΖ® «―ßœΑΜ·―ßΒΡ÷Ί“ΣΥΦœκΖΫΖ®Θ§“άΨίΆ§άύΈο÷ –‘÷ ΒΡœύΥΤ–‘Θ§Ω…“‘Αο÷ζΈ“Ο«ΉωΒΫΨΌ“ΜΖ¥»ΐΓΘ
œ÷”–œ¬Ν–»ΐΉιΈο÷ ΘΚ
AΘ°Ω’ΤχΓΔΒ®Ζ·ΓΔ±υΥ°ΓΔ’αΧ«ΓΓΓΓΓΓΓΓΓΓ
BΘ°KOHΓΔH2SO4ΓΔCa(OH)2ΓΔBa(OH)2
CΘ°NH4ClΓΔNa2CO3ΓΔSO2ΓΔNa2SO4
(1)Χν–¥œ¬±μΩ’ΑΉ
|
ΉιΓΓΓΓ ±π |
AΉι |
BΉι |
CΉι |
|
Ζ÷άύ±ξΉΦ |
¥ΩΨΜΈο |
Φν |
ΓΓΓΓΓΓΓΓ
|
|
≤Μ τ”Ύ…œ ωΖ÷άύ±ξΉΦΒΡΈο÷ |
Ω’Τχ |
ΓΓΓΓΓΓΓΓ
|
 SO2 SO2 |
(2)«κΖ¬’’Φλ―ιCO2ΒΡΖ¥”ΠΘ§―Γ”ΟSO2 ΜρSO3 ι–¥“ΜΗωάύΥΤΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ ΫΓΓΓΓΓΓ ΓΘ
(3)NH4Cl»ή“Κ”κKOH»ή“ΚΡήΙΜΖ¥”ΠΘ§ Β÷ «“ρΈΣΥϋΟ«‘ΎΥ°÷–Ϋβάκ≥ωά¥ΒΡNH4+ΚΆOH-ΫαΚœ…ζ≥…ΝΥNH3ΚΆH2OΓΘΫαΚœΖΔ…ζΗ¥Ζ÷ΫβΖ¥”ΠΒΡΧθΦΰΘ§«κΜΊ¥πΘΚBa(OH)2»ή“Κ”κNa2SO4»ή“ΚΡήΙΜΖ¥”ΠΒΡ Β÷ «ΥϋΟ«‘ΎΥ°÷–Ϋβάκ≥ωΓΓΓΓΓΓ άκΉ”ΫαΚœ…ζ≥…ΝΥΓΓΓΓΓΓ ΓΘ
(4)«κ“άΨί(3)÷–ΜώΒΟΒΡΤτ ΨΘ§≈–Εœœ¬Ν–‘ΎΥ°»ή“Κ÷–Ρή¥σΝΩΙ≤Ά§¥φ‘ΎΒΡ“ΜΉιάκΉ” «ΓΓΓΓ ΓΘ
AΘ°H+ΓΔOH-ΓΓΓΓΓΓ ΓΓBΘ°CO32-ΓΔH+ΓΓΓΓΓΓ CΘ°Cu2+ΓΔOH-ΓΓΓΓΓΓ DΘ°Na+ΓΔCl-
20Θ°(10Ζ÷)Ά®Ιΐ―ßœΑΘ§Έ“Ο«Ω…“‘¥”Μ·―ßΒΡΫ«Ε»Ω¥Έ ΧβΓΘΕΙΫ§Μζ”…”ΎΩλΫίΖΫ±ψΕχΫχ»κ«ßΦ“ΆρΜßΘ§«κΗυΨίΆΦ ΨΜΊ¥πΘΚ
(1)÷ΤΉς≤ΡΝœ÷– τ”ΎΫπ τΜρΚœΫπΒΡ «ΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓ (―ΓΧν“Μ÷÷Έο÷ ±ύΚ≈)Θ§ τ”Ύ”–ΜζΚœ≥…≤ΡΝœΒΡ «ΓΓΓΓΓΓΓΓΓΓ (―ΓΧν“Μ÷÷Έο÷ ±ύΚ≈)ΘΜ
(2)÷ΤΉς ÷±ζΒΡΥήΝœ τ”ΎΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΥήΝœ(ΧνΓΑ»»Υή–‘Γ±ΜρΓΑ»»ΙΧ–‘Γ±)ΘΜΓΓΓΓΓΓΓΓΓΓ
(3)ΕΙΫ§“―≥…ΈΣ÷ΎΕύΦ“ΆΞΒΡ‘γ≤Ά“ϊΤΖΘ§“‘œ¬ «ΕΙΫ§÷–“Μ–©”Σ―χ≥…Ζ÷ΒΡΤΫΨυ÷ ΝΩΖ÷ ΐΓΘ«κΗυΨίœ¬±μΜΊ¥πΘΚ
|
≥…Ζ÷ |
Υ° |
ΒΑΑΉ÷ |
÷§ΖΨ |
Χ«άύ |
ΗΤ |
ΝΉ |
Χζ |
Έ§…ζΥΊA |
|
÷ ΝΩΖ÷ ΐ/% |
96.0 |
1.8 |
0.7 |
1.1 |
0.01 |
0.03 |
0.0005 |
0.015 |
ΔΌΕΙΫ§÷–Κ§”–ΒΡΈΔΝΩ‘ΣΥΊ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΔΎ«ύ…ΌΡξ»±ΖΠΓΓΓΓΓΓΓΓΓΓΓΓ ‘ΣΥΊ“ΉΜΦ”–ΊΰΌΆ≤ΓΓΘ
Δέ‘ΎΕΙΫ§ΥυΚ§ΒΡ”Σ―χΥΊ÷–ΡήΙ©Ηχ»ΥΧεΡήΝΩΒΡ”Σ―χΥΊ”–ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
Δή»τ≥…Ρξ»ΥΟΩΧλ ≥”Ο100gΕΙΫ§Θ§‘ρ…ψ»κΒΑΑΉ÷ ΒΡ÷ ΝΩΈΣΓΓΓΓΓΓΓΓΓΓΓΓ gΓΘ
œΥΈ§ΥΊΒΡΜ·―ß ΫΈΣ(C6H10O5)nΘ§‘Ύ¥ΏΜ·ΦΝΚΆΦ”»»ΒΡΧθΦΰœ¬œΥΈ§ΥΊΩ…“‘”κΥ°Ζ¥”Π…ζ≥…ΤœΧ―Χ«Θ§–¥≥ωΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
Δί»ΥΧε»±ΖΠΈ§…ζΥΊCΜα“ΐΖΔ_______ΓΓ ____≤ΓΓΘΈ§…ζΥΊCΒΡœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ176Θ§Έ§…ζΥΊC÷–CΓΔHΓΔO»ΐ÷÷‘ΣΥΊΒΡ÷ ΝΩ±»ΈΣ9ΓΟ1ΓΟ12Θ§‘ρΈ§…ζΥΊCΒΡΜ·―ß ΫΈΣΓΓΓΓΓΓΓΓ ΓΓΓΘ
19Θ°(4Ζ÷)–μΕύΈόΟςœ‘œ÷œσΒΡΜ·―ßΖ¥”ΠΩ…Ά®ΙΐΒΈΦ”ΤδΥϋ ‘ΦΝΒΡΖΫΖ®Θ§ Ι÷°≤ζ…ζΟςœ‘ΒΡœ÷œσ “‘÷ΛΟςΖ¥”Π»Ζ ΒΖΔ…ζΝΥΓΘάΐ»γ“‘œ¬ΦΗΗω Β―ι:
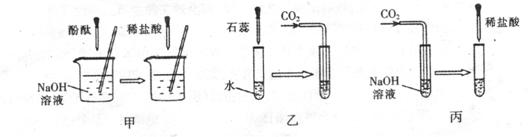
(1) Β―ιΦΉ÷–ΒΡNaOH”κHCl«ΓΚΟΖ¥”Π ±Θ§Ω…Ιέ≤λΒΫΒΡœ÷œσ «_____________________;
(2)¥”―–ΨΩ‘≠άμΒΟ÷ΣΘ§ Β―ιΦΉ «Ά®ΙΐΦλ―ιΖ¥”Π«ΑΚσ»ή“ΚΥαΦν–‘ΒΡΗΡ±δ÷ΛΟςΖ¥”ΠΖΔ…ζΝΥΘ§”κ÷°≤…”ΟœύΆ§‘≠άμΒΡΜΙ”– Β―ι__________________(ΧνΓΑ““Γ±ΜρΓΑ±ϊΓ±);
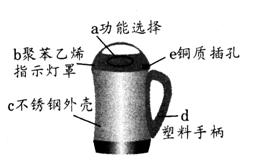 (3)÷ΛΟς Β―ι±ϊ÷–NaOH”κCO2ΖΔ…ζΝΥΖ¥”ΠΘ§≥ΐΝΥΩ…“‘ΒΈΦ”ΥαΘ§ΜΙΩ…ΒΈΦ”ΒΡ ‘ΦΝ «______ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
________
(4)»τΫΪΚ§”–―ΈΥαΒΡ¬»Μ·ΗΤ»ή“Κ÷–ΚΆΒΫ÷––‘Θ§‘Ύ≤Μ”Ο÷Η ΨΦΝΒΡ«ιΩωœ¬Θ§Φ”»κΒΡ ‘ΦΝΩ…“‘ «__ΓΓ ΓΓ______
(–¥Μ·―ß Ϋ)ΓΘ
(3)÷ΛΟς Β―ι±ϊ÷–NaOH”κCO2ΖΔ…ζΝΥΖ¥”ΠΘ§≥ΐΝΥΩ…“‘ΒΈΦ”ΥαΘ§ΜΙΩ…ΒΈΦ”ΒΡ ‘ΦΝ «______ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
________
(4)»τΫΪΚ§”–―ΈΥαΒΡ¬»Μ·ΗΤ»ή“Κ÷–ΚΆΒΫ÷––‘Θ§‘Ύ≤Μ”Ο÷Η ΨΦΝΒΡ«ιΩωœ¬Θ§Φ”»κΒΡ ‘ΦΝΩ…“‘ «__ΓΓ ΓΓ______
(–¥Μ·―ß Ϋ)ΓΘ
18Θ°(2Ζ÷)Μ·Ζ ΚΆ≈©“© «ΙΊœΒ≈©“Β…ζ≤ζΒΡΝΫάύ÷Ί“ΣΈο÷ ΓΘœ÷”–NH4HC O3ΓΔCuCl2ΓΔKNO3ΓΔCuSO4ΥΡ÷÷Έο÷ Θ§Τδ÷– τ”ΎΗ¥ΚœΖ ΒΡ «ΓΓΓΓΓΓΓΓΓΓ Θ§≥Θ”Οά¥÷Τ≈©“©ΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
17Θ°(2Ζ÷)Ρ≥ΝΘΉ”ΫαΙΙ Ψ“βΆΦΈΣ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ§ΗΟΝΘΉ”ΒΡΚΥΒγΚ… ΐΈΣ____________;Β±a=_______ ±, ±μ ΨΒΡ «―τάκΉ”ΫαΙΙ Ψ“βΆΦΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com