
题目列表(包括答案和解析)
2. 为预防自行车生锈,下列做法中不合理的是
A.车架表面喷涂油漆 B.钢圈表面镀防护金属
C.链条表面涂机油 D.露天放置,日晒雨淋
1.下列说法正确的是
A.空气中氧气的质量分数为21%
B. 空气中各成分所占的比例是永恒不变的
C.空气是由多种物质组成的混合物
D. 空气质量级别数目越大,空气的质量越好
25.(6分)造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的______污染。秸秆的主要成分是纤维素[(C6H1005)n],纤维素中C、H、O三种元素的质量比为______(用最简整数比表示)。
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是_____。
②若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8 t(H2SO4的质量分
数为20%),可以处理的废水质量是多少?(计算过程写在答题卡上)
24.(12分)某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。
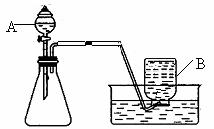 (1)甲同学选用如右图所示的装置制取氧气。
(1)甲同学选用如右图所示的装置制取氧气。
①写出仪器B的名称:______。
②甲同学应选取的试剂是Mn02和_______(填化学式),
Mn02固体在该反应中起_______作用。
③除用排水法外,甲同学还可选择_____法收集氧气。
④实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现。该实验操作的目的是__________。
(2)乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反
应的化学方程式为________。实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
[提出猜想]猜想l:反应生成的MnO2分解放出02;
猜想Ⅱ:反应生成的K2Mn04分解放出O2
做出上述猜想的理由是_______。
[实验验证]同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的Mn02,在250℃条件下加热一段时间,冷却后
测得Mn02的质量不变。则猜想________________错误。
②第二组同学取K2Mn04在250℃条件下加热,没有用测定质量的方法得
出了猜想Ⅱ正确的结论。该组同学选择的实验方法是_________________ 。
[拓展延伸]实验发现,K2MnO4受热只能部分分解,经分析可能是生成物K2O对其分
解产生影响。请设计实验方案验证:________________。
[实验反思]通过以上实验探究,你对“问题的发现与解决”有何认识?_________。
23.(9分)金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于________变化。钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择_____________(选填“铜块”、“锌块”、“铅块”)。
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:
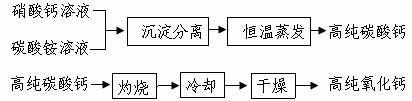
请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为___________。
②实验室常采用______________操作进行沉淀分离。
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是___________ 。
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止_________________(用化学方程式表示)。
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少____________污染。20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用__________方法区分尼龙和蚕丝。
22.(7分)下图是对生成氯化钠反应关系的归纳与整理。

请回答下列问题:
(1)物质A是常见的碱,写出A的化学式:______。
(2)写出反应①的化学方程式:___________________。
(3)说出NaHC03在医疗上的一种用途:______________ 。
(4)反应③、④、⑤、⑥能够进行的原因是_______________ 。
(5)实验室配制200g 8%的NaCl溶液,需要水的质量是___________g,配制过程中为了加快NaCl的溶解,可以采取的措施是_____________。
21.(6分)下表为元素周期表中某一周期元素的原子结构示意图。
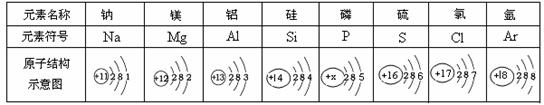 请回答下列问题:
请回答下列问题:
(1)表中磷原子的核电荷数x=___________ 。
(2)表中具有相对稳定结构的元素是______ 。
(3)在化学反应中,每个铝原子失去________个电子形成铝离子。
(4)镁元素与氯元素形成的化合物化学式为_______。
(5)上述元素在周期表中处于同一周期的原因是_______。
(6)硫与氧气的反应(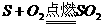 )可用下图表示:
)可用下图表示:
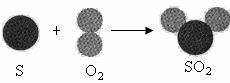
设N个氧气分子的质量为32g,则64g氧气与足量硫粉完全反应生成的二氧化硫分
子数为_______N。
20.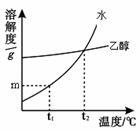 固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线 如右图所示。下列说法错误的是
固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线 如右图所示。下列说法错误的是
A.物质W能溶解在水和乙醇中
B.t1℃时,物质w在水中的溶解度为mg
C.t2℃时,物质W在水中与在乙醇中的溶解度相同
D.将t1℃时物质w的饱和水溶液升温至t2℃有晶体析出
19.认识燃烧原理可以合理利用和控制燃烧反应。下列说法正确的是
A.物质与氧气反应时都会发生燃烧
B.只有燃烧反应可将化学能转化为热能
C.增大可燃物与空气的接触面积,可促进燃烧
D.煤炉生火时,用木材引燃是为了提高煤的着火点
18.已知反应 ,则X的化学式为
,则X的化学式为
A.C2H6 B.C2H4 C.C2H2 D.C2H60
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com