
题目列表(包括答案和解析)
30.(9分)向 8g某一价或二价金属的氧化物固体中加入适量10%的稀H2SO4(密度为1.07g/cm3),使其完全溶解,已知所消耗的硫酸体积为92mL。在所得溶液中插入铂电极进行电解,通电一定时间后,在一个电极上收集到224mL(标准状况)氧气,在另一个电极上析出该金属1.28g。
(1)根据计算确定金属氧化物的名称。
(2)计算通电完毕后硫酸溶液的物质的量浓度。(溶液体积以消耗的硫酸体积92mL为准)
29.(6分)现有MgSO4和Al2(SO4)3的混合溶液,其中Mg2+

Mg2+与Al3+分离,至少应加入1.6 mol/L的NaOH溶液体积为多少?
28.A、B两种有机化合物,分子式都是C9H11O2N。化合物A是天然蛋白质的水解产物,光谱测定显示:分子结构中不存在甲基(-CH3),化合物A的结构式是_____。化合物B是某分子式为C9H12的芳香烃-硝化后的唯一产物(硝基连在芳环上)。化合物B的结构简式是______。
27.(10分)化合物A(C8H8O3)为无色液态,难溶于水,有特殊香味,从A出发,可发生图示的一系列反应,图中的化合物A硝化时可生成四种一硝基取代物,化合物H的分子式为C6H6O,G能发生银镜反应。
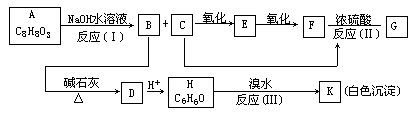
(1)下列化合物可能的结构简式:A____,E____,K____。
(2)反应类型(Ⅰ)____(Ⅱ)____(Ⅲ)____。
(3)反应方程式:H→K:_________
C→E:_________
C+F→G:_________。
26.(8分)已经知25℃时几种物质的电离度(溶液浓度为0.1mol)如下表:

(已知(H2SO4的第一步是完全电离的)
(1)25℃时,0.1mol/L上述几种溶液[H+]由大到小的顺序是(填序号)____;
(2)25℃时,pH值相同的上述几种溶液,其物质的量浓度由大到小的顺序是____;
(3)25℃时,将足量的 Zn粉放入等体积、pH=1的上述几种溶液中产生氢气的体积(同温同压下),由大到小顺序为____;


25.(9分)由常见元素组成的化合物A、B、C、D、E、F、G有如下图关系,其中C、F、G是无色化合物,D是氯化物。若在D或E的纯溶液中通入F气体,都有B和G生成。
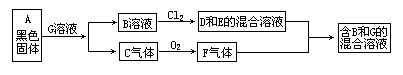
(1)写出下列物质的化学式A____,B____,C____,G____。
(2)写出将F通入D和E的混合溶液中发生反应的离子方程式________。
(3)D溶液中通入C气体,则产生浅黄色浑浊,写出该反应的化学方程式。___________。
24.(14分)硫酸铜在加热条件下发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。请用题给出的仪器、药品(如图3-3所示)设计一个实验,测定硫酸铜在加热分解时产生的氧气、二氧化硫、三氧化硫与参加反应的硫酸铜的物质的量的关系,并确定在该条件下硫酸铜分解反应的化学方程式。

实验测得数据和有关结果如下:
①准确称量无水硫酸铜4.80g;
②测出量筒中水的体积(折算成标准状况下气体的体积)为 224 mL;
③干燥管在实验后质量增加2.56g;
④实验结束时装置F中的溶液变为Na2SO4溶液(不含其他杂质)。
(分子量:CuSO4160 SO264 SO380)
请回答:
(1)硫酸铜加热分解产生的混和气体首先通过____(填序号)装置,发生反应的化学方程式为______。
(2)若气流从左→右,分解后混和气体依次通过装置的顺序(填进出口序号)为____。
(3)装置D的作用____,装置C的作用____。
(4)根据测得数据,确定该条件下硫酸铜分解反应的化学方程式为:____。
23.(6分)一位同学使用①冷开水②碘酒③熟石灰④淀粉⑤肥皂水⑥食醋⑦红墨水⑧废易拉罐(铝合金)⑨废干电池(锌筒里装填有碳粉、二氧化锰、氯化铵、淀粉等物质的糊状混合物)⑩食盐(11)纯碱 为实验试剂,进行家庭小实验。
(1)用给定的试剂,他不能进行的实验是(不考虑电解):____。(填写标号)
a.制NaOH溶液b.制备纯净氯气并实验它的漂白作用c.实验硬水和肥皂的作用d.制二氧化碳
e.制硬脂酸f.进行淀粉水解实验并检验水解产物
(2)该同学制备氨气,先从废干电池中制备氯化铵。为此,他准备把废干电池锌筒里的糊状混合物溶解于少量水,过滤去除不溶物,再蒸发灼烧滤液,以制得干燥的氯化铵晶体。他的设想是否合理____,理由是____________。
(3)该同学拟进行除去淀粉溶液中所含食盐的实验。他把一只鸭蛋浸泡在食醋里,待蛋壳溶去,在膜上打一小洞,小心倒出蛋清、蛋黄,洗净蛋膜,作为半透膜小袋,再装入含食盐的淀粉溶液,扎好袋口。做好这些准备工作后,他即将进行的实验操作名称是____(选填:萃取、盐析、渗析、过滤、分液)要保证全部除去淀粉溶液里的食盐,实验中必须____。
食醋溶去蛋壳发生的反应的离子方程式是____。
22.已知丁基共有4种。不必试写,立即可断定分子式为C5H10O的醛应有 [ ]
A.3种
B.4种
C.5种
D.6种
第Ⅱ卷 (非选择题共67分)
20.某化工厂排放的酸性废液里含有游离的氯。要除去游离氯并中和其酸性,正确方案是 [ ]
A.先加适量的Na2SO3,再加适量的NaOH
B.先加适量的NaOH,再加适量的Na2SO3
C.先加过量的Na2SO3,再加适量的NaOH
D.先加过量的NaOH,再加适量的HCl
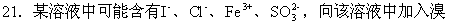
水,溶液无色。因此可知原溶液中 [ ]
A.肯定不含I-
B.肯定不含Cl-
C.肯定含Fe3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com