
题目列表(包括答案和解析)
1] B
27].黄铜矿(主要成分CuFeS2)是提取铜的主要原料
(1) 取12.5g黄铜矿样品,经测定含3.60g硫(杂质不含硫),矿样中CuFeS2含量为_______。
(2) 已知:2CuFeS2+4O2 Cu2S+3SO2+2FeO(炉渣)
Cu2S+3SO2+2FeO(炉渣)
产物Cu2S在1200℃高温下继续反应:2Cu2S+3O2→2Cu2O+2SO2 2Cu2O+Cu2S→6Cu+SO2
假定各步反应都完全,完成下列计算:
①由6mol CuFeS2生成6mol Cu,求消耗O2的物质的量。
②6mol CuFeS2和14.25mol O2反应,理论上可得到多少摩尔铜?
③6mol CuFeS2和15.75 mol O2反应,理论上可得到多少摩尔铜?
26].当140g铁粉跟213g氯气充分反应后,加入适量的水,完全溶解后无残余固体,加入稀释至2L。
(1) 求溶液中氯化铁的物质的量浓度。
(2) 若要求溶液中只含溶质氯化铁,还需在此溶液通入标准状况下的氯气多少升?
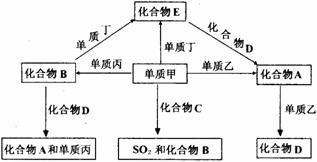
25].A、B、C、D、E是中学化学中常见的五种化合物,它们分别由两种元素组成。甲、乙、丙、丁是单质,甲、丙、A、C、D常温下均为气体,B是液体,E是黑色固体,这些单质和化合物之间存在如下关系(反应条件均无注明):
(1) 写出下列物质的分子式:甲 、B 。
(2) 在以上有关转化的反应中充当还原剂的物质有 (填写化学式)。
(3) 写出化合物A的电子式 。
(4) 写出单质丁跟化合物B反应生成化合物E的化学方程式:______________________________。
24].某化学反应的反应物和产物为:KMnO4 + KI + H2SO4 → MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1) 该反应的氧化剂是
(2) 如果该反应方程式中I2和KIO3的系数都是5
①KMnO4的系数是
②在给出的化学式上标出电子转移的方向和数目: KMnO4 + KI + H2SO4 →
(3) 如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组。原因是_____________
 ____________________________________________________________。
____________________________________________________________。
23].KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
____KClO3+____HCl(浓)=____KCl+____ClO2↑+____Cl2↑+____H2O
(1) 请配平上述化学方程式。
(2) 浓盐酸在反应中显示出来的性质是________(填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3) 产生0.1mol Cl2,则转移的电子的物质的量为________mol。
(4) 氧化剂是________,还原剂是________;氧化产物是________,还原产物是________。
22].有A、B、C、D四种金属,将A、B用导线连接后浸入稀H2SO4中,A上放出氢气,B逐渐溶解生成B2+;电解含A2+和C2+的混合溶液时,阴极上先析出C;将D放入含B2+的硝酸溶液中,D表面有B析出,同时生成D2+。则这四种金属阳离子的氧化性由强到弱的顺序是:
。
21].在铁与铜的混和物中,加入不足量的稀硝酸,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,m1与m2的关系是
A.m1一定大于m2 B.m1可能等于m2
C.m1一定等于m2 D.m1可能大于m2
20].根据下表下列叙述中正确的是
|
序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
|
|
FeCl3 |
|
② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
|
③ |
KClO3 |
HCl(浓) |
|
Cl2 |
Cl2 |
|
④ |
KMnO4 |
HCl(浓) |
|
Cl2 |
MnCl2 |
A.表中第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+
C.还原性比较:H2O2>Mn2+>Cl-
D.④的离子方程式配平后,H+的化学计量数为16
19].实验室可通过以下反应来制取碘:2NO+O2=2NO2;2H++2I-+NO2=NO+I2+H2O。在这一过程中,每制取1mol I2时,所消耗氧化剂的质量是
A.16g B.28g C.32g D.46g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com