
题目列表(包括答案和解析)
29.(8分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B元素原子L层上的电子数为K层电子数的2倍;元素D的2价阴离子的核外电子排布与氖原子相同;E与A同主族;A和E 这两种元素与D都能形成X2Y、X2Y2型化合物。
(1) 写出元素的符号:A ;B___ ___;C ;E________。
(2) 画出D的离子结构示意图____________________________。
(3) A的X2Y型化合物的电子式是_________________________。
28.(15分)下表是元素周期表的一部分,按要求填空:
|
族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
|
⑴ |
|
⑵ |
|
|
3 |
⑶ |
⑷ |
⑸ |
⑹ |
|
⑺ |
⑻ |
⑼ |
|
4 |
⑽ |
⑾ |
|
|
|
|
⑿ |
|
(1)写出下列元素的元素名称⑴ ⑵ ⑾ ⑿
(2)在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,最不活泼的元素是 。(填元素符号)
(3)写出元素⑻的氢化物的结构式___________________
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。(填化学式,下同)
(5)在⑶与⑷的单质中,化学性质较活泼的是 ,写出(3)的单质与水反应的化学方程式 ,该反应的氧化剂是_______________。
27.(5分)元素的金属性越强,形成的最高价氧化物的水化物的碱性越 ,与酸或水反应生成氢气越 。 元素的非金属性越强,形成的最高价氧化物的水化物的酸性越 ,与氢气化合生成气态氢化物越 ,生成的气态氢化物越_____。
26.(5分)在①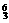 Li ②
Li ②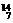 N ③
N ③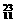 Na ④
Na ④ Mg ⑤
Mg ⑤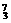 Li ⑥
Li ⑥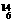 C ⑦C60 ⑧NH4CNO ⑨CO(NH2)2⑩石墨 中:
C ⑦C60 ⑧NH4CNO ⑨CO(NH2)2⑩石墨 中:
(1) 和 互为同位素;(填编号,下同)
(2) 和 质量数相等,但不能互称同位素;
(3) 和 的中子数相等,但质子数不相等,所以不是同一种元素;
(4) 和 互为同素异形体, 和 互为同分异构体。
25、比较下列情况混合时,开始时的反应速率最小的是( )。
A、10mL 2mol•L-1 Na2S2O3和 10mL 1mol•L-1HCl
B、10mL 4mol•L-1 Na2S2O3和 30mL 2/3mol•L-1HCl
C、10mL 1mol•L-1 Na2S2O3和 30mL 0.5mol•L-1HCl
D、10mL 3mol•L-1 Na2S2O3和 20mL 1mol•L-1HCl
第Ⅱ卷(非选择题 共50分)
24、下列说法中可以充分说明反应: P(气)+Q(气)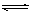 R(气)+S(气) , 在恒温下已达平衡状态的是
( )
R(气)+S(气) , 在恒温下已达平衡状态的是
( )
A、反应容器内压强不随时间变化
B、P和S的生成速率相等
C、反应容器内P、Q、R、S四者共存
D、反应容器内总物质的量不随时间而变化
23.密闭容器中发生可逆反应:X2(g) + Y2(g)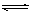 2Z(g)。已知起始时X2、Y2、Z各物质的浓度分别为0.1 mol/L、0.3mol/L、0.2mol/L,反应在一定条件下达平衡时,各物质的浓度可能是(
)
2Z(g)。已知起始时X2、Y2、Z各物质的浓度分别为0.1 mol/L、0.3mol/L、0.2mol/L,反应在一定条件下达平衡时,各物质的浓度可能是(
)
A.c(Z) = 0.3mol/L B.c(Y2) = 0.15mol/L
C.c(Y2) = 0.2mol/L D.c(Z) = 0.4mol/L
22.可逆:反应:2NO2≒2NO+O2在定容密闭容器中反应,达到平衡状态的标志是( )
A、单位时间内生成nmol O2的同时生成2nmolNO
B、用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态
C、混合气体的颜色不再改变的状态
D、混合气体的密度不再改变的状态
21、C+CO2  2CO(正反应吸热),反应速率为v1:N2+3H2
2CO(正反应吸热),反应速率为v1:N2+3H2  2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况是
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况是
A.同时增大 B.同时减小
C.v1增加,v2减小 D.v1减小,v2增大
20、在反应:C+CO2 2CO中,可使反应速率增大的措施是(
)。
2CO中,可使反应速率增大的措施是(
)。
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强
A.①②③④ B.②③④⑤ C.①②③ D.②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com