
题目列表(包括答案和解析)
3.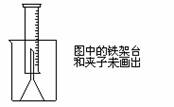 测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:中学化学实验常用仪器、800毫升烧杯、100毫升量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100毫升)
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:中学化学实验常用仪器、800毫升烧杯、100毫升量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100毫升)
(1)补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800毫升烧杯底部,把短颈漏斗倒扣在样品上面。
② ,
③ ,
④ 。
(2)合金样品用铜网包裹的目的是: 。
2.以下气体:①H2 ②Cl2 ③CH4 ④NO ⑤SO2 ,(烧瓶的位置不能移动)
 (1). 若烧瓶是干燥的,则由A口进气,可收集的气体是 ,由B口进气,可收集的气体是 。
(1). 若烧瓶是干燥的,则由A口进气,可收集的气体是 ,由B口进气,可收集的气体是 。
(2). 若烧瓶内充满水,可收集到的气体是 ,气体应由 口进入(填A或B) (3). 若在烧瓶内装有一定量的溶液,用以洗气,则气体应从 口进入 (填A或B)
1.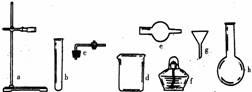 在没有现成的 CO2气体发生器的情况下,请你选用右图中的部分仪器,装配成一个简易的,能随开随用,随关随停的 CO2气体发生装置。应选用的仪器是(填入仪器的编号)(
)
在没有现成的 CO2气体发生器的情况下,请你选用右图中的部分仪器,装配成一个简易的,能随开随用,随关随停的 CO2气体发生装置。应选用的仪器是(填入仪器的编号)(
)
A.abcd B.degh C.bcd D.acde
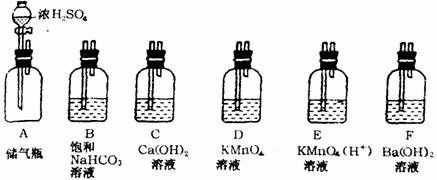
8.CO2气体是大气产生温室效应、使地球变暖的气体之一。某学生参加课外环保小组,测定校办工厂排出废气中CO2(含杂质SO2)的含量,他准备将CO2变成沉淀,然后测沉淀质量,通过计算求出CO2的含量。图中表示主要装置,其他胶管、导管略去。
(1)下列设计主要仪器装置使用的顺序有两种,其中 方案较为合理。
甲方案;A→D→E→F→C 乙方案:A→D→F→E→C
(2)为什么要使气体两次通过酸性KMnO4溶液
(3)为什么没有选B装置
(4)CO2是被转化成 沉淀而计算出质量来的。
(5)要测得沉淀物质量需进行 、 、干燥、 操作。
课后练习
7.用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.lmol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处 、 。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
6.某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量.实验步骤如下:①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为 ag.②装好实验装置。③检查装置气密性。④加热,开始反应,直到产生一定量的气体。⑤停止加热(如图,导管出口高于液面)。⑥测量收集到气体的体积。⑦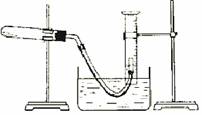 准确称量试管和残留物的质量为bg.⑧测量实验室的温度。⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。⑩处理实验数据,求出氧气的摩尔质量。回答下列问题:
准确称量试管和残留物的质量为bg.⑧测量实验室的温度。⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。⑩处理实验数据,求出氧气的摩尔质量。回答下列问题:
⑴如何检查装置的气密性? 。
⑵以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是:
(请填写步骤代号)。
⑶测量收集到气体体积时,如何使量筒内外液面的高度相同?
。
5.某研究性学习小组在做Na2O2与水反应实验时,发现Na2O2与水反应后的溶液中滴加酚酞试液溶液呈现红色,但红色很快褪色,甲、乙、丙三同学对此现象分别做了如下推测:
甲:因为反应后试管很热,所以可能是溶液温度较高使红色褪去。
乙:因为所加水的量较少,红色褪去可能是生成的NaOH溶液浓度较大的影响。
丙:Na2O2具有强氧化性,生成物中O2、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
⑴验证甲同学的推测是否正确的方法是_____________________________,验证乙同学的推测是否正确的方法是_____________________________________;当出现_________________________________________现象时,即可说明丙同学的推测正确。
 ⑵有同学提出用定量的方法探究丙同学方案中是否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积,与理论值比较,即可得出结论。
⑵有同学提出用定量的方法探究丙同学方案中是否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积,与理论值比较,即可得出结论。
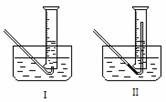
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用右图装置中的______,理由是__________________________。
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为________(选填“100mL”、“200mL”、“500mL”或“1000mL”)。
4.某溶液中含有OH-、CO32-、SO42-三种阴离子,要求只取一次待测液就能将阴离子都检验出来,试设计一种简便的检验方法。
3.某溶液含有较多的 Na2SO4 和少量的 Fe2(SO4)3 ,若用该溶液制取芒硝,可供选择的操作有:①加适量 H2SO4 溶液②加金属 Na ③结晶④加过量 NaOH ⑤加强热脱结晶水⑥过滤。正确的操作步聚是 ( )
A.②⑥③ B.④⑥①③ C.④⑥③② D.②⑥①③⑤
2.提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为 ( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com