
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
4.ЙигкФГШмвКжаЫљКЌРызгЕФМјБ№ЃЌЯТСаХаЖЯе§ШЗЕФЪЧ(ЁЁЁЁ )
A.МгШыAgNO3ШмвКЩњГЩАзЩЋГСЕэЃЌМгЯЁбЮЫсГСЕэВЛЯћЪЇЃЌдђвЛЖЈгаClЃДцдк
B.МгШыNaOHШмвКФмЩњГЩАзЩЋГСЕэЃЌNaOHЙ§СПЪБГСЕэгжЯћЪЇЃЌдђдШмвКвЛЖЈгаAl3+
C.МгШыNaOHВЂМгШШгаФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЕФЦјЬхЩњГЩЃЌдђдШмвКвЛЖЈга
D.МгШыбЮЫсгаФмЪЙГЮЧхЪЏЛвЫЎЛызЧЕФЦјЬхЩњГЩЃЌдђдШмвКвЛЖЈгаДѓСП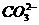
3.НёгаЯТСаЪЕбщЃКЂйЮЊМгПьЯИЭЫПКЭСђеєЦјЕФЗДгІЃЌЯШНЋЭЫПНјаазЦЩеЃЛЂкНЋ0.01 mol/LЃ1KIШмвК8-10ЕЮЃЌЕЮШы10 mLЯрЭЌХЈЖШЕФЯѕЫсвјШмвКжаЃЌПЩжЦШЁЕтЛЏвјНКЬхЃЛЂл2%ЧтбѕЛЏФЦШмвК4-6ЕЮЃЌЕЮШы10%CuSO4ШмвК2 mLжажЦШЁCu(OH)2аќзЧвКЃЌПЩжБНггУгкМьбщШЉЛљЃЛЂмНЋЕШЬхЛ§ввДМКЭХЈСђЫсЛьКЯЙВШШжЦввЯЉЁЃЩЯЪіЪЕбщЗНЗЈжа(ЁЁЁЁ )
A.ЂйЂке§ШЗЁЁЁЁЁЁЁЁЁЁ B.ЂкЂле§ШЗЁЁЁЁЁЁЁЁЁЁ C.ЖМе§ШЗЁЁЁЁЁЁЁЁ D.ЖМВЛе§ШЗ
2.ЪЕбщЪвБЃДцЯТСавЉЦЗЕФЗНЗЈЃЌе§ШЗЕФЪЧ(ЁЁЁЁ )
A.ЧтЗњЫсжќДцдкЬижЦЕФЫмСЯЦПРя
B.ЪЂЗХХЈСђЫсЕФЙуПкЦПгІЕБгУФЅПкВЃСЇШћЃЌВЛФмгУЯ№ЦЄШћ
C.ЪЂфхЕФЪдМСЦПРяМгвЛаЉЫЎРДЗРжЙфхЛгЗЂ
D.дкЭЌвЛВувЉЦЗГїРяДцЗХХЈАБЫЎКЭХЈбЮЫс
1.гУpHЪджНВтЖЈФГЮоЩЋШмвКЕФpHЪБЃЌЙцЗЖЕФВйзїЪЧ(ЁЁЁЁ )
A.НЋpHЪджНЗХШыШмвКжаЙлВьЦфбеЩЋЕФБфЛЏЃЌИњБъзМБШЩЋПЈБШНЯ
B.НЋШмвКЕЙдкpHЪджНЩЯЃЌИњБъзМБШЩЋПЈБШНЯ
C.гУИЩдяЕФНрОЛВЃСЇАєеКШЁШмвКЃЌЕЮЕНpHЪджНЩЯЃЌИњБъзМБШЩЋПЈБШНЯ
D.дкЪдЙмФкЗХШыЩйСПШмвКЃЌжѓЗаЃЌАбpHЪджНЗХдкЙмПкЃЌЙлВьбеЩЋБфЛЏЃЌИњБъзМБШЩЋПЈБШНЯ
4ЃЎЪЕеНбнСЗ
2ЁЂаДГігаЙиЕФЛЏбЇЗНГЬЪНЃК
AгыB____________________________________________________________;CгыD_______________________________________________________________;EгыЮоЫЎСђЫсЭ_____________________________________________________________;FгыMg_________________________________________________________________;FгыMgЕФЗДгІВњЮягыЫЎ___________________________________________________________
_________________________________________________.
[НтЮі]ЁАИУЦјЬхОпгаДЬМЄадЦјЮЖЃЌВЂФмЪЙШѓЪЊЕФКьЩЋЪЏШяЪджНБфРЖЁБЪЧНтД№ДЫЬтЕФЭЛЦЦПкЃЌДЫЦјЬхжЛФмЪЧNH3ЃЌНсКЯЬтвтЃЌFОЭЪЧN2ЁЃвђДЫЃЌДгЯоЖЈЕФЗДгІЮяжаЃЌжЛФмЩшЗЈДгАБЫЎжаЛёШЁЃЌШЛКѓНсКЯЗЂЩњзАжУЬиЕу(ЙЬЁЂвКЁЂВЛМгШШ)МАЦфЫћЪЕбщЯжЯѓЃЌБуПЩЭЦЖЯЦфЫћЕФЮяжЪЁЃ
[НтД№]1ЁЂA ХЈАБЫЎЃЛЁЁ BЁЂбѕЛЏИЦЃЛ CЁЂАБЦјЃЛ DЁЂбѕЛЏЭЃЛ EЁЂЫЎЃЛ FЁЂАБЦјЁЃ2ЁЂТдЁЃ
[Р§8]Cu+дкЫсадШмвКжаВЛЮШЖЈЃЌПЩЗЂЩњздЩэбѕЛЏЛЙдЗДгІЩњГЩCu2+КЭCuЁЃЯжгаХЈЯѕЫсЁЂЯЁСђЫсЁЂЯЁЯѕЫсЁЂFeCl3ЯЁШмвКМАpHЪджНЃЌЖјУЛгаЦфЫќЪдМСЁЃМђЪіШчКЮгУзюМђБуЕФЪЕбщЗНЗЈРДМьбщCuOОЧтЦјЛЙдЫљЕУЕНЕФКьЩЋВњЮяжаЪЧЗёКЌгаМюадбѕЛЏЮяCu2O.
[НтЮі] Cu2OЪЧМюадбѕЛЏЮяЃЌвЛЖЈПЩвдИњЯЁСђЫсЗДгІЃЌCu+НјШыШмвККѓгжПЩздЗЂЩњГЩCu2+КЭCu+ЃЌCu2+дкЫЎШмвКжаГЪРЖЩЋЃЌЖјCuВЛИњЯЁСђЫсЗДгІЁЃвђДЫПЩвдЩшЯыЃЌШєCuOБЛH2ЛЙдЕФВњЮяШЋВПЪЧCuЃЌНЋЦфЗХШыЯЁH2SO4жаЃЌЮоБфЛЏЃЛШєКьЩЋВњЮяжаКЌгаCu2OЃЌНЋЦфЗХШыЯЁH2SO4жаЃЌШмвКЛсБфГЩРЖЩЋЁЃ
дЫгУвббЇЙ§ЕФжЊЪЖЗжЮіЦфЫќЪдМСЪЧЗёПЩгУЃЌШчХЈH2SO4ЁЂХЈHNO3ЁЂЯЁHNO3ЃЌвђЮЊЫќУЧЖМгаНЯЧПЕФбѕЛЏадЃЌВЛТлКьЩЋВњЮяЪЧCuЛЙЪЧCuКЭCu2OЕФЛьКЯЮяЃЌНЋЦфЗжБ№ЗХШыет3жжЫсжаОљБЛбѕЛЏЮЊCu2+ЃЌвВЮоЗЈМьбщЁЃЖјpHЪджНдђВЛФмгУЁЃЫљвдМьбщЗНЗЈЪЧШЁЩйСПИУКьЩЋЮяжЪЗХШыЯЁH2SO4жаЃЌеёЕДЃЌШєШмвКБфЮЊРЖЩЋЃЌЫЕУїВњЮяжагаCu2OЃЛШєШмвКВЛБфЩЋЃЌЫЕУїВњЮяжаЮоCu2OЁЃ
1ЁЂаДГіA-FЕФЮяжЪУћГЦЃК
A______________________,B__________________,C___________________
D______________________,E__________________,F___________________.
8ЃЎ4gЁЁЁЁЂЊЃН4gЁЃ
ЙЪШмвКжаNaOHЕФжЪСПЗжЪ§йМДѓгкЁС100%ЃН3ЃЎ85%ЪБЃЌдкВНжшЂкжаЛсгаNaHCO3ОЇЬхЮіГіЁЃ
ЃлР§5ЃнЁЁ ФГПЮЭтЛюЖЏаЁзщбЇЩњФЃФтКєЮќУцОпжаЕФдРэ(Й§бѕЛЏФЦгыГБЪЊЖўбѕЛЏЬМЗДгІ),ЩшМЦгУЭМ2-7-13ЫљЪОЕФвЧЦїРДжЦШЁбѕЦјВЂВтСПбѕЦјЕФЬхЛ§ЁЃЭМжаСПЦјзАжУEЪЧгЩМзЁЂввСНИљВЃСЇЙмзщГЩЃЌЫћУЧгУЯ№ЦЄЙмНгЭЈЃЌВЂзАШыЪЪСПЫЎЁЃМзЙмгаПЬЖШ(0~15ml)ЃЌЙЉСПЦјгУЃЛввЙмПЩЩЯЯТвЦЖЏЃЌвдЕїНквКУцИпЕЭЁЃЪЕбщЪвПЩЙЉбЁгУЕФвЉЦЗЛЙгаЃКЯЁСђЫсЁЂбЮЫсЁЂЙ§бѕЛЏФЩЁЂЬМЫсФЦЁЂДѓРэЪЏЁЂЫЎЁЃЛиД№ЯТСаЮЪЬтЁЃ
(1)ЭМжаЫљЪОзАжУЕФСЌНгЫГађЪЧ(ЬюИїНгПкЕФБрКХЃЌЦфжаСЌНгНКЙмМАМаГжзАжУОљЪЁТд)ЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(2)зАжУCжаЗХШыЕФЗДгІЮяЪЧЁЁЁЁЁЁЁЁЁЁЁЁ КЭ ЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)зАжУAЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛзАжУBЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(4)ЮЊСЫНЯзМШЗЕиВтСПбѕЦјЕФЬхЛ§ЃЌГ§СЫБиаыМьВщећИізАжУЕФЦјУмаджЎЭтЃЌдкЖСШЁЗДгІЧАКѓМзЙмжавКУцЕФЖСЪ§ЁЂЧѓЦфВюжЕЕФЙ§ГЬжаЃЌгІзЂвт ЁЁЁЁЁЁЁЁЁЁЁЁЁЁКЭЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюаДзжФИБрКХ)ЁЃ
ЁЁЁЁ a.ЪгЯпгыАМвКУцзюЕЭДІЯрЦНЁЃЁЁЁЁЁЁ b.ЕШД§ЦЌПЬЃЌД§ввЙмжавКУцВЛдйЩЯЩ§ЪБЃЌСЂМДЖСЪ§ЁЃ
c.ЖСЪ§ЪБгІЩЯЯТвЦЖЏввЙмЃЌЪЙМзЁЂввСНЙмвКУцЯрЦНЁЃЁЁ d.ЖСЪ§ЪБВЛвЛЖЈЪЙМзЁЂввСНЙмвКУцЯрЦНЁЃ
[НтЮі]ЁЁ EзАжУЮЊВтСПЦјЬхЬхЛ§ЕФзАжУЃЌе§ШЗЖСЪ§ЪБгІЪЙМзЁЂввСНЙмвКУцЯрЦНЁЃ
Д№ЃК(1)ЂнЁЂЂлЁЂЂмЁЂЂоЁЂЂпЁЂЂкЁЂЂйЁЂЂр(ЂоЁЂЂпПЩЛЅЛЛ)ЁЃ(2)ДѓРэЪЏЃЛбЮЫсЁЃ(3)ЮќЪеЛьдкбѕЦјжаЮДЗДгІЕФCO2ЃЌЮќЪеCO2жаЕФHClЦјЬх(4)a;cЁЃ
[Р§6]ФГбЇЩњИљОнИпжаПЮБОжаЯѕЫсМиЪмШШЗжНтЕФЪЕбщВйзїРДХаЖЯЯѕЫсЧІЕФЗжНтВњЮяжЎвЛЪЧбѕЦјЃЛНЋЪдЙмжаЕФЯѕЫсЧІМгШШЕНШлШкЃЌАбДјгаЛ№аЧЕФЯИФОЬѕЩьНјЪдЙмПкЃЌМьбщЗХГіЕФЦјЬхЃЌЕБЗЂЯжФОЬѕИДШМЪБИУбЇЩњМДЖЯбдЃЌЯѕЫсЧІЪмШШЗжНтгабѕЦјЗХГіЁЃЧыФуЖдЩЯЪіЪЕбщМАНсТлЕФКЯРэадзїГіЦРМлЁЃШчгаБивЊЃЌПЩЬсГіИФНјЕФЪЕбщЗНАИЁЃ
[НтЮі]гаЙиЗДгІЕФЗНГЬЪНЮЊЃК
ЁЁЁЁЁЁ ЁїЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ Ёї
Ђй2KNO3ЈT2KN02+O2ЁќЁЁ Ђк2Pb(NO3)2ЈT2PbO+4NO2+02Ёќ
БШНЯЗДгІЪНЂйКЭЂк,ЦфВЛЭЌжЎДІЪЧЂкжаГ§ЩњГЩ02Эт,ЛЙЩњГЩСЫNO2.етвЛВЛЭЌгжВњЩњСЫСНИіНсЙћЁЃвЛЗНУцNO2ЯЁЪЭСЫO2ЃЌO2НіеМЛьКЯЦјЬхЕФ20%ЃЌЖјетгыПеЦјжаO2ЕФКЌСПЯрНќЃЌвђЖјДЫДІO2ВЛПЩФмЪЙДјЛ№аЧЕФФОЬѕИДШМЃЛСэвЛЗНУцNO2БОЩэвВФмЪЙДјЛ№
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ Ёї
аЧЕФФОЬѕИДШМЁЃвђЮЊNO2ЪмШШФмЗХГі02ЃК2NO2ЈT2NO+O2ЁЃЗжЮіЕНДЫЃЌЮЪЬтБувЛЧхЖўГўЁЃ
[Д№АИ]ЩЯЪіЪЕбщМАНсТлдкПЦбЇЩЯЪЧДэЮѓЕФЁЃгЩгкNO2ИЩШХСЫO2ЕФМьбщЃЌвђДЫгІбЁгУNaOHШмвКГ§ЕєNO2КѓдйМьбщжЎЁЃ
[Р§7]баОПФГвЛЛЏбЇЗДгІЕФЪЕбщзАжУШчЯТЭМЫљЪОЃК
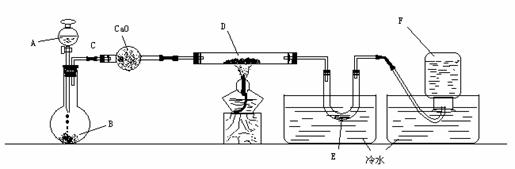
A-FЪєгкЯТСаЮяжЪжаЕФСљжжЮяжЪЃКХЈСђЫсЁЂХЈбЮЫсЁЂХЈАБЫЎЁЂЯЁСђЫсЁЂЯЁбЮЫсЁЂЯЁЕЊЫЎЁЂЫЎЁЂаПСЃЁЂЭЦЌЁЂЪГбЮЁЂИпУЬЫсМиЁЂТШЛЏИЦЁЂбѕЛЏИЦЁЂЫФбѕЛЏШ§ЬњЁЂбѕЛЏЭЁЂЧтЦјЁЂЖўбѕЛЏЕЊЁЂвЛбѕЛЏЬМЁЂТШЦјЁЂТШЦјЁЂТШЛЏЧтЁЂАБЦјЁЂЕЊЦјЁЂбѕЦјЁЃ
ЪЕбщЯжЯѓЃК
(1)DЮяжЪгЩКкЩЋБфЮЊКьЩЋ
(2)ЮоЫЎСђЫсЭЗлФЉЗХШыЮоЩЋЭИУїЕФEжаЕУЕНРЖЩЋШмвК
(3)ЕуШМЕФУОЬѕЩьШыЮоЩЋЮоЮЖЕФFжаЁЃУОЬѕБэУцЩњГЩвЛжжЛвЛЦЩЋвђЬхЮяжЪЁЃНЋИУЛвЛЦЩЋЮяжЪЗХШыЫЎжаЃЌгаЦјЬхЗХГіЃЌИУЦјЬхОпгаДЬМЄадЦјЮЖЁЃВЂФмЪЙШѓЪЊЕФКьЩЋЪЏШяЪджНБфРЖЁЃЭЈЙ§ЗжЮіЛиД№ЃК
3ЃЎР§ЬтОЋНВ
[Р§1]ЃЎЫФТШЛЏЮ§ГЃЮТЯТЪЧЮоЩЋвКЬхЃЌдкПеЦјжаМЋвзЫЎНтЃЌШлЕуЃ36ЁцЃЌЗаЕу114ЁцЃЌН№ЪєЮ§ЕФШлЕуЮЊ231ЁцЃЌФтРћгУЭМжаЕФвЧЦїЃЌЩшМЦзщзАвЛЬзЪЕбщзАжУЃЌгУШлШкЕФН№ЪєЮ§ИњИЩдяЕФТШЦјжБНгзїгУжЦШЁЮоЫЎЫФТШЛЏЮ§(ДЫЗДгІЙ§ГЬЗХГіДѓСПЕФШШ)ЁЃЧыЛиД№ЯТСаИїЮЪЬтЁЃ
ЁЁЁЁ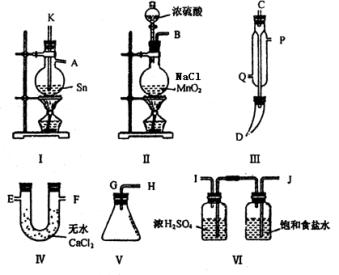 ЁЁ(1)гУВЃЙм(ЮДЛГі)СЌНгЩЯЪізАжУЃЌе§ШЗЕФЫГађЪЧ(ЬюИїНгПкЕФДњТызжФИ)________Нг________ЁЂ________Нг________ЁЂ________
ЁЁ(1)гУВЃЙм(ЮДЛГі)СЌНгЩЯЪізАжУЃЌе§ШЗЕФЫГађЪЧ(ЬюИїНгПкЕФДњТызжФИ)________Нг________ЁЂ________Нг________ЁЂ________
Нг________ЁЂ________Нг________ЁЂ________Нг________ЁЃ ЁЁ(2)зАжУЂіЕФзїгУЪЧ___________ЃЛзАжУЂєЕФзїгУЪЧ_____________ЁЃ ЁЁ(3)РфФ§ЙмРэРфШДЫЎЕФСїЯђЪЧДг__________НјШыЃЌДг__________СїГіЁЃ ЁЁ(4)ЪЕбщЪБгІЯШЕуШМ_____________ДІОЦОЋЕЦЃЌМгШШЮТЖШгІДѓгк______________ЁцЃЌД§__________МДПЩЭЃжЙМгШШЁЃ ЁЁ(5)вбжЊЫФТШЛЏЮ§гіЫЎЧПСвЫЎНтЃЌВњЮяжЎвЛЪЧЙЬЬЌЖўбѕЛЏЮ§ЃЌФЧУДЫФТШЛЏЮ§ЫЎНтЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(6)ШчЙћНЋжЦШЁЕФЫФТШЛЏЮ§ЩйаэБЉТЖгкПеЦјжаЃЌдЄЦкПЩПДЕНЕФЯжЯѓЪЧ____________ЁЃ
ЁЁ(7)ЮЊСЫЗРжЙЮлШОПеЦјЃЌдкзАжУЕФзюКѓгІ____________ЁЃ
[НтЮі]ЃКетЪЧвЛИіжЦБИЪЕбщЁЃ
ЁЁЪЕбщФПЕФЪЧЃКжЦБИЮоЫЎSnCl4
ЁЁЪЕбщдРэЪЧЃКSn+2Cl2  SnCl4
ЁЁЯШжЦБИCl2ЃК2H2SO4(ХЈ)+2NaCl+MnO2
SnCl4
ЁЁЯШжЦБИCl2ЃК2H2SO4(ХЈ)+2NaCl+MnO2  Na2SO4+MnSO4+Cl2Ёќ+2H2O
ЁЁЪЕбщЕФИЩШХвђЫиЪЧЃКSnCl4гіЫЎЧПСвЫЎНтЃЌвђДЫЃЌГ§ШЅЪЕбщжаЫЎеєЦјЕФИЩШХЃЌЪЧЪЕбщГЩАмЕФЙиМќЁЃетРявЊЗжЮіЫЎеєЦјЕФРДдДвдМАГ§ШЅЫЎеєЦјЕФДыЪЉЁЃЫЎеєЦјЕФРДздгкжЦCl2КЭПеЦјжаЕФЫЎеєЦјЁЃ
ЁЁЬтФПжаЬсЙЉЕФаХЯЂЃКSnCl4ЕФаджЪдкЩшМЦЗНАИЪБвЊГфЗжРћгУетаЉаХЯЂЁЃ
ЁЁвдЩЯЮЪЬтЧхГўСЫЃЌЪЕбщЗНАИОЭЛљБОШЗЖЈСЫЁЃ
ЁЁД№АИЃК
ЁЁ(1)BНгJЃЌIНгKЃЌAНгCЃЌDНгGЃЌHНгE(ЛђF)
ЁЁ(2)Г§ШЅCl2жаЛьгаЕФHClКЭЫЎеєЦјЃЌдкжЦCl2ЪБЗЂЩњЕФИБЗДгІ2NaCl+H2SO4
Na2SO4+MnSO4+Cl2Ёќ+2H2O
ЁЁЪЕбщЕФИЩШХвђЫиЪЧЃКSnCl4гіЫЎЧПСвЫЎНтЃЌвђДЫЃЌГ§ШЅЪЕбщжаЫЎеєЦјЕФИЩШХЃЌЪЧЪЕбщГЩАмЕФЙиМќЁЃетРявЊЗжЮіЫЎеєЦјЕФРДдДвдМАГ§ШЅЫЎеєЦјЕФДыЪЉЁЃЫЎеєЦјЕФРДздгкжЦCl2КЭПеЦјжаЕФЫЎеєЦјЁЃ
ЁЁЬтФПжаЬсЙЉЕФаХЯЂЃКSnCl4ЕФаджЪдкЩшМЦЗНАИЪБвЊГфЗжРћгУетаЉаХЯЂЁЃ
ЁЁвдЩЯЮЪЬтЧхГўСЫЃЌЪЕбщЗНАИОЭЛљБОШЗЖЈСЫЁЃ
ЁЁД№АИЃК
ЁЁ(1)BНгJЃЌIНгKЃЌAНгCЃЌDНгGЃЌHНгE(ЛђF)
ЁЁ(2)Г§ШЅCl2жаЛьгаЕФHClКЭЫЎеєЦјЃЌдкжЦCl2ЪБЗЂЩњЕФИБЗДгІ2NaCl+H2SO4  2HClЁќ+Na2SO4ЃЌВњЩњСЫHClЃЛЗРжЙПеЦјжаЕФЫЎеєЦјНјШызЖаЮЦПжаЪЙSnCl4ЗЂЩњЫЎНтЁЃ
ЁЁ(3)aЁЂp (4)I 231Ёц
SnСЃШлЛЏ
ЁЁ(5)SnCl4+2H2O=SnO2+4HCl
(6)ГіЯжАзЩЋбЬЮэ
ЁЁ(7)ЭЈШыNaOHШмвКжаЃЌЮќЪеЖргрCl2
2HClЁќ+Na2SO4ЃЌВњЩњСЫHClЃЛЗРжЙПеЦјжаЕФЫЎеєЦјНјШызЖаЮЦПжаЪЙSnCl4ЗЂЩњЫЎНтЁЃ
ЁЁ(3)aЁЂp (4)I 231Ёц
SnСЃШлЛЏ
ЁЁ(5)SnCl4+2H2O=SnO2+4HCl
(6)ГіЯжАзЩЋбЬЮэ
ЁЁ(7)ЭЈШыNaOHШмвКжаЃЌЮќЪеЖргрCl2
ЁЁ [Р§2]ЃЎЮЊСЫВтЖЈЙЄвЕДПМюжаЬМЫсФЦЕФжЪСПЗжЪ§(ДПМюжаГЃКЌЩйСПNaCl)ЃЌФГбЇЩњЩшМЦСЫЪЕбщзАжУШч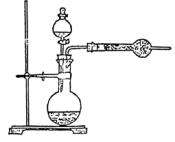 ЭМ
ЁЁ(1)зМШЗГЦШЁЪЂгаМюЪЏЛвЕФИЩдяЙмЕФжЪСП(ЩшЮЊW1)
ЁЁ(2)зМШЗГЦШЁвЛЖЈСПДПМюбљЦЗ(ЩшЮЊW0)ЃЌВЂЗХШыЩеЦПжаЁЃДгЗжвКТЉЖЗЛКЛКЕЮШыЯЁСђЫсЃЌД§ВЛдйЗЂЩњЦјЬхКѓЁЃГЦИЩдяЙмЕФзмжЪСП(ЩшЮЊW2)ЁЃЩшбЇЩњЕМГіЕФМЦЫуЙЋЪНЮЊЃК
ЁЁNa2CO3ЕФжЪСПЗжЪ§ЃН
ЭМ
ЁЁ(1)зМШЗГЦШЁЪЂгаМюЪЏЛвЕФИЩдяЙмЕФжЪСП(ЩшЮЊW1)
ЁЁ(2)зМШЗГЦШЁвЛЖЈСПДПМюбљЦЗ(ЩшЮЊW0)ЃЌВЂЗХШыЩеЦПжаЁЃДгЗжвКТЉЖЗЛКЛКЕЮШыЯЁСђЫсЃЌД§ВЛдйЗЂЩњЦјЬхКѓЁЃГЦИЩдяЙмЕФзмжЪСП(ЩшЮЊW2)ЁЃЩшбЇЩњЕМГіЕФМЦЫуЙЋЪНЮЊЃК
ЁЁNa2CO3ЕФжЪСПЗжЪ§ЃН 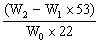 ЁС100%
ЁЁЪдЛиД№ЃК
ЁЁЂйW2ЃW1БэЪОЪВУДЃП
ЁЁЂкШчЙћВЛМЦГЦСПЮѓВюЃЌИУЩњЕФЪЕбщНсЙћгаЮоУїЯдЮѓВюЃПШчгаЃЌЪЧЦЋДѓЛЙЪЧЦЋаЁЃПЧыМђвЊЫЕУїИљОнВЂЬсГіВЙОШДыЪЉЁЃ
ЁЁ[НтЮі]ЃКетЪЧвЛЕРЖЈСПЪЕбщЬт
ЁЁЪЕбщФПЕФЪЧЃКВтЖЈДПМюжа Na2CO3ЕФжЪСПЗжЮі
ЁЁЪЕбщдРэЃКЯЁH2SO4гыNa2CO3ЗДгІЩњГЩCl2ЃЌВтГіCO2ЕФжЪСПМДПЩЧѓГіNa2CO3ЕФжЪСПЃЌМЬЖјЧѓГіNa2CO3ЕФжЪСПЗжЪ§ЁЃ
ЁЁCO2ЕФжЪСПЮЊ(W2ЃW1)gЃЌбљЦЗжЪСПЮЊW0g
ЁЁNa2CO3+H2SO4=Na2SO4+H2O+CO2Ёќ
ЁЁ 106 ЁЁЁЁЁЁЁЁЁЁ 44
ЁЁЁЁx ЁЁЁЁЁЁЁЁЁЁ W2-W1
ЁС100%
ЁЁЪдЛиД№ЃК
ЁЁЂйW2ЃW1БэЪОЪВУДЃП
ЁЁЂкШчЙћВЛМЦГЦСПЮѓВюЃЌИУЩњЕФЪЕбщНсЙћгаЮоУїЯдЮѓВюЃПШчгаЃЌЪЧЦЋДѓЛЙЪЧЦЋаЁЃПЧыМђвЊЫЕУїИљОнВЂЬсГіВЙОШДыЪЉЁЃ
ЁЁ[НтЮі]ЃКетЪЧвЛЕРЖЈСПЪЕбщЬт
ЁЁЪЕбщФПЕФЪЧЃКВтЖЈДПМюжа Na2CO3ЕФжЪСПЗжЮі
ЁЁЪЕбщдРэЃКЯЁH2SO4гыNa2CO3ЗДгІЩњГЩCl2ЃЌВтГіCO2ЕФжЪСПМДПЩЧѓГіNa2CO3ЕФжЪСПЃЌМЬЖјЧѓГіNa2CO3ЕФжЪСПЗжЪ§ЁЃ
ЁЁCO2ЕФжЪСПЮЊ(W2ЃW1)gЃЌбљЦЗжЪСПЮЊW0g
ЁЁNa2CO3+H2SO4=Na2SO4+H2O+CO2Ёќ
ЁЁ 106 ЁЁЁЁЁЁЁЁЁЁ 44
ЁЁЁЁx ЁЁЁЁЁЁЁЁЁЁ W2-W1
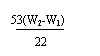
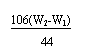 ЁЁ
ЁЁ
ЁЁ x=ЁЁ =ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ

Na2CO3%=ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁС100%
ЁЁВњЩњЮѓВюЕФдвђ(МДИЩШХвђЫи)гаЩеЦПЕФCO2ВЛФмЖМБЛМюЪЏЛвЮќЪеЃЌЪЕбщжЕЦЋЕЭЁЃCO2ЦјЬхЛьгаЕФЫЎеєЦјКЭПеЦјжаЕФЫЎеєЦјБЛМюЪЏЛвЮќЪеЃЌЪЙЪЕбщжЕЦЋИпЃЌСНИівђЫизлКЯПМТЧЃЌCO2ЕФгАЯьЪЧжївЊЕФЃЌЫљвд ЪЕбщжЕЦЋЕЭЁЃ
ЁЁВЙОШЕФАьЗЈЃКШчЭМ
ЁЁ 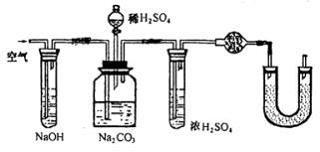 ЁЁЂйНЋеєСѓЩеЦПИФЮЊМЏЦјЦПЃЌРћгкХХГіCO2ЁЃ
ЁЁЂкЯђМЏЦјЦПжаЭЈШы(вбГ§ШЅCO2)ПеЦјЃЌгУПеЦјНЋЩеЦПжаCl2ОЁСПХХГіШЅЁЃ
ЁЁЂлдкИЩдяЙмЧАСЌНгЪЂгаХЈH2SO4ЕФЪдЙмЃЌвдГ§ШЅЫЎеєЦјЃЛ
ЁЁЂмдкUаЭЙмжазАгаМюЪЏЛвЃЌвдЮќЪеПеЦјжаЕФCO2ЦјЬхЃЌОЙ§етаЉВЙОШДыЪЉЃЌЪЕбщЮѓВюПЩвдНЕЕЭЁЃ
ЁЁ [Р§3]ЃЎЪЕбщЪвжагУХЈбЮЫсгыMnO2жЦCl2ЃЌдйгУCl2КЭCa(OH)2ЗДгІжЦЩйСПЦЏАзЗлЃЌвбжЊCl2КЭCa(OH)2жЦЦЏАзЗлЪЧЗХШШЗДгІЃЌЮТЖШЩдИпМДЗЂЩњИБЗДгІЃК6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2OЃЌЯжгаШ§ЮЛЭЌбЇЩшМЦЕФШ§ЬззАжУШчЭМ(UаЮЙмжаЗХгаВЃСЇЯЫЮЌЃЌПЩЪЙЦјЬхЫГРћЭЈЙ§)ЃК
ЁЁ
ЁЁЂйНЋеєСѓЩеЦПИФЮЊМЏЦјЦПЃЌРћгкХХГіCO2ЁЃ
ЁЁЂкЯђМЏЦјЦПжаЭЈШы(вбГ§ШЅCO2)ПеЦјЃЌгУПеЦјНЋЩеЦПжаCl2ОЁСПХХГіШЅЁЃ
ЁЁЂлдкИЩдяЙмЧАСЌНгЪЂгаХЈH2SO4ЕФЪдЙмЃЌвдГ§ШЅЫЎеєЦјЃЛ
ЁЁЂмдкUаЭЙмжазАгаМюЪЏЛвЃЌвдЮќЪеПеЦјжаЕФCO2ЦјЬхЃЌОЙ§етаЉВЙОШДыЪЉЃЌЪЕбщЮѓВюПЩвдНЕЕЭЁЃ
ЁЁ [Р§3]ЃЎЪЕбщЪвжагУХЈбЮЫсгыMnO2жЦCl2ЃЌдйгУCl2КЭCa(OH)2ЗДгІжЦЩйСПЦЏАзЗлЃЌвбжЊCl2КЭCa(OH)2жЦЦЏАзЗлЪЧЗХШШЗДгІЃЌЮТЖШЩдИпМДЗЂЩњИБЗДгІЃК6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2OЃЌЯжгаШ§ЮЛЭЌбЇЩшМЦЕФШ§ЬззАжУШчЭМ(UаЮЙмжаЗХгаВЃСЇЯЫЮЌЃЌПЩЪЙЦјЬхЫГРћЭЈЙ§)ЃК
ЁЁ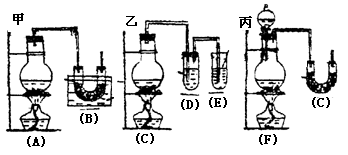 ЁЁ
ЁЁ
(1)ЧыДгвдЯТСљЗНУцЖдЩЯЪіМзЁЂввЁЂБћШ§ЬззАжУЕФгХШБЕуНјааЦРМлЃЌНЋЪЪЕБЕФбЁЯюађКХЬюгкЯТБэФк(ДэбЁЁЂТЉбЁЁЂЖрбЁОљЕЙПлЗж) ЁЁaЃЎВЛвзПижЦЗДгІЫйТЪ ЁЁbЃЎШнвзПижЦЗДгІЫйТЪ ЁЁcЃЎгаИБЗДгІЗЂЩњ ЁЁЁЁdЃЎПЩЗРжЙИБЗДгІЗЂЩњ ЁЁeЃЎШнвзЮлШОЛЗОГ ЁЁЁЁfЃЎПЩЗРжЙЮлШОЛЗОГ
|
1 |
гХЕу |
ШБЕу |
|
ЁЁМззАжУ |
1
|
1
|
|
ЁЁввзАжУ |
1
|
1
|
|
ЁЁБћзАжУ |
1
|
1
|
ЁЁ(2)ЧыДгМзЁЂввЁЂБћШ§зАжУжаЃЌбЁШЁКЯРэЕФзщГЩВПЗж(AЁЂBЁЂCЁЂDЁЂEЁЂFЁЂG)ЃЌзщзАвЛЬзФуШЯЮЊИќЭъЩЦЕФЪЕбщзАжУЃЌСЌНгЫГађ(АДЦјСїзѓЕНгвЗНЯђ)ЮЊ_____________ЃЌдкДЫзАжУМАМзЁЂввЁЂБћШ§зАжУжаЃЌФуШЯЮЊЪЧЗёЛЙШБЩйБивЊЕФзАжУЃЌЫЕУїдвђ_____________________ЁЃ [НтЮі]ЃКетЪЧвЛЕРЦРМлЪЕбщЗНАИЕФЬтЁЃИУЬтДгЪЧЗёгаИБЗДгІЗЂЩњЃЌЪЧЗёвзПижЦЗДгІЫйТЪЃЌЪЧЗёЗРжЙЮлШОЃЌЪЧЗёИЩШХЗДгІВњЮяЕШЗНУцНјааЦРМлЁЃ ЁЁД№АИЃК ЁЁ(1)гХЕу ЁЁЁЁШБЕу ЁЁЁЁ МззАжУd ЁЁ aЁЂe ЁЁЁЁ ввзАжУf ЁЁ aЁЂc ЁЁЁЁ БћзАжУb ЁЁ eЁЂc ЁЁ(2)F-B-E ЁЁдкCl2жаЛьгаHClЃЌгІдкЩеЦПКЭАМаЮЙмжЎМфСЌНгвЛИіЪЂгаБЅКЭЪГбЮЫЎЕФЪдЙмЃЌвдГ§ШЅHClЦјЬхЁЃ
ЂйвЧЦїСЌНгЕФЫГађ(ЬюБрКХЃЛвЛЦ№ПЩжиИДЪЙгУ)ЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЃDжаХЈСђЫсЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЃЪЕбщЭъБЯЪБЃЌЙлВьЕНAжаЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂкСаГіМЦЫуCuЕФдзгСПЕФБэДяЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂлЯТСаЧщПіНЋЪЙВтЖЈНсЙћЦЋДѓЕФЪЧЁЁЁЁЁЁЁЁЁЃ
(a)CuOЮДШЋВПЛЙдЮЊCuЃЛЁЁЁЁ (b)CuOЪмГБЃЛЁЁЁЁ (c)CuOжаЛьгаCuЁЃ
(2)ШчЙћШдВЩгУЩЯЭМЫљЪОЕФвЧЦїзАжУЃЌЩцМАЦфЫћЗНАИЃЌЛЙПЩВтЖЈЕФЮяРэСПгаЁЁЁЁЁЁЁЃ
(a)m(Cu)КЭm(CuO)ЃЛЁЁЁЁ(b)m(N2)КЭm(H2O)ЃЛ
(c)m(Cu)КЭm(H2O)ЃЛЁЁЁЁ(d)m(NH3)КЭm(H2O)
ЃлР§4Ѓн ЪЕбщЪвРяСйЪБашвЊгУNaOHШмвККЭCO2РДжЦШЁДПNa2CO3ШмвКЁЃвбжЊCO2ЦјЬхдкЭЈШыNaOHШмвКЙ§ГЬжаМЋвзЙ§СПЩњГЩNaHCO3ЃЌЧвЮоУїЯдЯжЯѓЁЃ
ЪЕбщЪвгаЯТСаЪдМСЃКЂйЮДжЊХЈЖШЕФNaOHЁЂЂк37%ЕФбЮЫсЁЂЂл37%ЕФСђЫсЁЂЂм14%ЕФбЮЫсЁЂЂнДѓРэЪЏЁЂЂоK2CO3ЙЬЬхЂпCu2(OH)2CO3ЁЃ
ЪЕбщЪвгаЯТСавЧЦїЃКЬњМмЬЈЁЂЦєЦеЗЂЩњЦїЁЂСПЭВЁЂЩеБЁЂЯ№ЦЄЙмЁЂВЃСЇЕМЙмЁЂЗжвКТЉЖЗЁЃ
вбжЊЯТБэжаИїЮяжЪдкГЃЮТЪБЕФШмНтЖШ(gЃЏ100gH2O)ЁЃ
|
Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
|
15ЃЎ9 |
8ЃЎ4 |
35 |
5ЃЎ5 |
20 |
40 |
(1)БОЪЕбщгІбЁгУЕФвЧЦїГ§ЦєЦеЗЂЩњЦїЁЂЯ№ЦЄЙмЁЂВЃСЇЕМЙмЭтЃЌЛЙашвЊЁЁЁЁЁЁЁЁ.
(2)ЮЊБЃжЄжЦЕУЕФNa2CO3ШмвКОЁСПДПЃЌгІбЁгУЕФвЉЦЗ(ЬюБрКХ)Г§ЂйЭтЃЌЛЙашвЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)МђвЊа№ЪіЪЕбщВНжшЃЌжБЕНжЦЕУДПNa2CO3ШмвК(вЧЦїАВзАПЩЪЁТд)ЁЃ
(4)ИљОнИјГіЕФШмНтЖШБэЃЌЧѓГіЕБNaOHШмвКжаШмжЪЕФжЪСПЗжЪ§ДѓгкЖрЩйЪБЃЌдкХфжУЙ§ГЬжаЛсгаОЇЬхЮіГі(аДГіМЦЫуВНжшКЭБивЊЕФЮФзжЫЕУї)ЃП
[НтЮі] БОЬтЕФФбЕудкЕк(3)ЮЪЁЃЩшМЦвРОнЪЧвРЯТСаЗДгІдРэЃК
CO2+NaOHЃНNaHCO3ЁЁ
NaOH+NaHCO3ЃНNa2CO3+H2O
РћгУЖЈСПЙиЯЕМАЛЏбЇЗДгІжЦЕУШмвКЃЌвђЬтаЭаТгБЃЌЫМТЗаТЧЩЃЌЙЪФбЖШНЯДѓЁЃ
Д№ЃК(1)ЩеБЁЂСПЭВЁЃ(2)ЂмЁЂЂнЁЃ(3)ЂйСПШЁвЛЖЈСПЕФЁЁNaOHШмвКЃЌЗжГЩСНЕШЗжЃЛжЦШЁCO2ЃЌЯђЦфжавЛЗнNaOHШмвКжаЭЈШыЙ§СПЕФCO2ЦјЬхЂлЃЛНЋСНЗнШмвКЛьдШЃЌвЁдШЁЃ(4)ДгБэжаПЩжЊЃЌNaHCO3ГЃЮТЯТШмНтЖШЮЊ8ЃЎ4gЁЃ
ЩшГЃЮТЯТ100gЫЎжаШмНтЕФNaOHжЪСПЮЊЂЊЪБЃЌДяЕНБЅКЭЁЃ
NaOHЁЁ+ЁЁCO2ЁЁЃНЁЁNaHCO3ЁЁ
40ЁЁЁЁЁЁЁЁЁЁЁЁ84
2ЁЂбЕСЗЗЂЩЂЫМЮЌвддіЧПЪЕбщЩшМЦФмСІЃЌЬсИпаХЯЂЧЈвЦЫЎЦН
ЪЕбщЗНАИЕФЩшМЦЭљЭљгааэЖрЭООЖЁЃЮЊСЫЪЪгІжабЇЩњЕФжЊЪЖФмСІЫЎЦНЃЌжабЇПЮБОжаЕФФГаЉЪЕбщПЩФмВЛЪЧзюгХЕФЗНАИЁЃЫљвддкЪЕбщИДЯАжавЊИљОнЪЕбщдРэРДЩшМЦЪЕбщВНжшКЭзАжУЃЌеЦЮевЛаЉзАжУКЭвЧЦївЉЦЗЕФЬцДњЗНЗЈЃЌСІЧѓЪЙЩшМЦЕФЪЕбщвЧЦїМђЕЅЁЂВйзїБуНнЁЂНкЪЁЪдМСЁЂЯжЯѓУїЯдЁЂАВШЋЗРЮлЕШЃЌХрбјКЭдіЧПЪЕбщЩшМЦФмСІКЭДДдьадЫМЮЌФмСІЁЃНќФъРДЃЌЪЕбщЬтжааТЧщОГЪдЬтВЛЖЯдіЖрЃЌетРрЪдЬтЕФЬиЕуЪЧНЋЛљБОЕФЪЕбщВйзїЩшМЦжУгкаТЕФЧщОГжа(жївЊЪЧжабЇПЮБОУЛгаЕФаТЗДгІЛђаТзАжУЛђЪЧФмЪЙжабЇЩњРэНтЕФзюаТПЦММжЊЪЖЁЂМђЛЏЕФИФНјЕФзАжУЕШ)ЃЌНсКЯбЇЩњдгаЕФжЊЪЖКЭФмСІЃЌРДНјаавЧЦїзщзАЁЂЯжЯѓУшЪіЁЂЪ§ОнЗжЮіЁЂПМТЧАВШЋКЭЗРЮлЕШЃЌгУРДПМВщПМЩњздбЇФмСІЁЂЫМЮЌФмСІЁЂЗжЮізлКЯМАЦРМлЕФФмСІЁЃгЩгкетРрЪЕбщЪдЬтЧщОГаТгБЁЂЩшЮЪЧЩУюЁЂЦЬЕцЕУЕБЁЂжЊЪЖаТЁЂЫМЮЌСПДѓЁЂЫљвдЧјЗжЖШКмКУЃЌФмШЗЪЕНЋвЛаЉЛљДЁдњЪЕЁЂздбЇФмСІЧПЁЂЫМЮЌУєНнЁЂаФРэЫижЪКУЕФПМЩњбЁВІГіРДЁЃЫљвдЃЌаТЧщОГЪЕбщЪдЬтНЋЪЧНёКѓЪЕбщЪдЬтЕФУќЬтЗНЯђЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com