
题目列表(包括答案和解析)
5、取5克含少量杂质的某金属R的样品,将其投入到73克溶质质量分数为20%的盐酸中,金属与盐酸恰好完全反应(杂质不反应),测得所生成的金属氯化物中氯元素的质量分数为74.7%,计算:
①样品中金属R的质量分数;
②反应所得溶液中溶质的质量分数。
4、现有铜、锌混合物5克,与48.74克某未知溶质质量分数的稀硫酸恰好完全反应,制得氢气0.04克,求:
①原混合物中锌的质量分数?
②反应所得溶液中溶质质量分数?
3、140g某物质的溶液蒸发70g水或者加入30克溶质,均得到同温度、同溶质质量分数的不饱和溶液,则原溶液中有溶质多少克?
2、某氯化铵中,可能混入了另一种氮肥,经测定该氯化铵中氮的质量分数为35%,又知在生产过程中只可能混入NH4NO3、NH4HCO3、(NH4)2SO4、CO(NH2)2中的一种,经分析,混入的杂质可能是什么?
1、葡萄糖(C6H12O6)中各元素的质量比为 。
9、有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。将其任意编号:A、B、C、D、E,进行两两混合,其现象如下表:
|
实 验 |
A+B |
A+E |
B+C |
B+E |
|
现 象 |
产生沉淀 |
产生沉淀 |
产生沉淀 |
产生气泡 |
(1)试推断并写出五种溶液中溶质的化学式。
A ,B ,C ,D ,E 。
8、欲除去下列物质中的杂质(括号里的物质),请在空格上填写选用的物质和有关化学方程式:
①NaCl(Na2CO3): , 。
②KCl(K2SO4): , 。
③Na2SO4(CuSO4): , 。
④NaNO3(CuSO4): , 。
⑤KNO3(KOH): , 。
⑥Na2SO4(NaOH): , 。
7、已知常用的强酸(H2SO4、HCI、HNO3)跟常用的强碱(NaOH、KOH)反应生成的盐的水溶液呈中性,现将某白色粉末溶人一无色中性液体中,按以下图示进行实验:
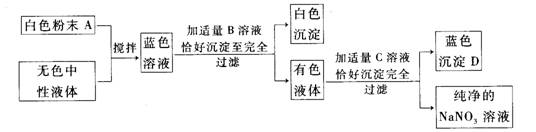
试按下列要求推断未知物。
(1)用化学式写出:B ,C ,D 。
(2)若A是纯净物,无色中性液体也是纯净物,则中性液体是 。(填化
学式)
(3)若A是纯净物,无色中性液体是只含一种溶质的溶液,则中性液体是 溶液或 溶液。(均填化学式)
6、用含有二氧化碳和水蒸气杂质的某种还原性气体测定一种铁的氧化物(FexOy)的组成,实验装置如图所示。

根据上图试回答:
(1)甲装置的作用是 ,反应的化学方程式是 。
(2)如果将甲装置和乙装置位置的顺序调换,对实验有无影响? 。
(3)实验过程中丁装置没有明显变化,而戊装置中溶液出现了白色沉淀,则该还原性气体是 。
(4)当丙装置中的FexOy,全部被还原后,称量剩余固体的质量为16.8g,同时测得戊装置的质量增加了17.6g。则FexOy中,铁元素与氧元素的质量比为 ,该铁的氧化物的化学式为 。
(5)上述实验装置中,如果没有甲装置,将使测定结果中铁元素与氧元素的质量的比值(填“偏大”、“偏小”或“无影响”) ;如果没有己装置,可能产生的后果是 。
5、 南京著名的风景点珍珠泉,水底有大量气泡冒出,像串
串珍珠,珍珠泉由此得名。某学生推测这种气体可能是沼气,查资料得知沼气中含60%-70%的CH4,还含有CO2、N2和CO等。他想用实验检验珍珠泉冒出气体的组成,设计了如图甲所示的取气方法:将空的雪碧汽水塑料瓶装满水,倒放在泉水中,瓶口对准水底冒出的气泡收集。
南京著名的风景点珍珠泉,水底有大量气泡冒出,像串
串珍珠,珍珠泉由此得名。某学生推测这种气体可能是沼气,查资料得知沼气中含60%-70%的CH4,还含有CO2、N2和CO等。他想用实验检验珍珠泉冒出气体的组成,设计了如图甲所示的取气方法:将空的雪碧汽水塑料瓶装满水,倒放在泉水中,瓶口对准水底冒出的气泡收集。
(1)这种集气方法叫 。针对瓶口太小不便于收集的特点,在不换瓶的情况下你的改进方法是 。
(2)如图乙所示,若用水将瓶中的气体排出,水龙头应接 导管。
(3)假设将这种未知气体通过澄清石灰水,石灰水变浑浊,剩余气体通过浓硫酸(以上两步,能被吸收的气体均被完全吸收),再通人纯氧气中点燃,将燃烧后生成的气体依次通过无水硫酸铜、澄清石灰水,观察到无水硫酸铜变蓝,石灰水变浑浊。仅由以上实验现象分析此未知气体的组成,结论是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com