
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
17ЃЎ (10Зж)ЁАЙизЂУёЩњЁБКЭЁАПЦбЇЗЂеЙЁБЪЧЁАЪЎЦпДѓЁББЈИцЕФжї
(10Зж)ЁАЙизЂУёЩњЁБКЭЁАПЦбЇЗЂеЙЁБЪЧЁАЪЎЦпДѓЁББЈИцЕФжї
ЬтжЎвЛЃЌЛЗОГЮЪЬтгыЁАУёЩњЁБКЭЁАПЦбЇЗЂеЙЁБУмЧаЯрЙиЁЃЪРНч
ЛЗБЃзщжЏ2006ФъЖШБЈИцжИГіЃЌдкЫљгаКтСПЕиЧђНЁПЕзДПіЕФжИБъ
жаЃЌШЫРрНіГЩЙІЕиХЄзЊСЫвЛЯюжИБъЕФЖёЛЏЃДѓЦјжаТШЗњЬўМѕЩйЃЌ
ЖјCЁЂSЁЂNбѕЛЏЮяЕФХХЗХгадіЮоМѕЃЌЫЎзЪдДЕФНєШБКЭЮлШОМгОчЁЃ
БЃжЄОМУзпПЩГжајЗЂеЙЕФЕРТЗЃЌЪЧЛЏбЇЙЄзїепгІОЁЕФжАд№ЫљдкЁЃ
ЁЁ ЛиД№ЯТСаЮЪЬтЃК
ЂХ ДѓЦјжаТШЗњЬўЕФМѕЩйДјРДЕФЛ§МЋаЇЙћЪЧЁЁЁЁЁЁЁЁ ЃЛ
ЂЦ ЫсгъЕФЛЏбЇЬиеїЪЧЁЁЁЁЁЁЁЁ ЁЃПеЦјжаСђбѕЛЏЮяКЭЕЊбѕЛЏЮяЪЧаЮГЩЫсгъЕФжївЊЮяжЪЁЃШєгУNOxБэЪОЕЊбѕЛЏЮяЃЌЧыаДГіПеЦјжаЕЊбѕЛЏЮяаЮГЩЫсгъЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂЧ SO2ЪЧгагУЕФЛЏЙЄдСЯЃЌЛиЪеРћгУSO2МШФмМѕЩйДѓЦјЮлШОЃЌгжФмГфЗжРћгУзЪдДЁЃгабЇепЬсГіРћгУFe2+ЁЂFe3+ЕШРызгЕФДпЛЏзїгУЃЌГЃЮТЯТНЋSO2бѕЛЏГЩSO42ЃЖјЪЕЯжSO2ЕФЛиЪеРћгУЁЃФГбаОПадбЇЯАаЁзщЩшМЦШчЯТЗНАИЃЌдкЪЕбщЪвЬѕМўЯТВтЖЈзЊЛЏЦїЕФЭбСђаЇТЪЃК
 ЁЁ
ЁЁ
Ђй дкЪЕбщЪвВтЖЈФЃФтбЬЦјжаSO2ЕФЬхЛ§ЗжЪ§ЃЌЯжгазЂЩфЦїЁЂЯДЦјЦПЁЂЕМЙмЁЂСПЭВЕШвЧЦїЃЌ
ашвЊЕФвЉЦЗгаЁЁЁЁЁЁЁЁЁЁ ЃЛ
Ђк ШєЩЯЪіЪЕбщЪЧдкБъзМзДПіЯТНјааЕФЃЌгћВтЖЈзЊЛЏЦїжаЕФЭбСђаЇТЪЃЌвбжЊЦјЬхСїЫйЃЌЛЙ
ЁЁ ашВтЖЈЕФЪ§ОнЪЧЁЁЁЁЁЁЁЁ ЃЛ
ЂШ ЫЎЬхИЛгЊбјЛЏЪЧЕМжТЫЎЬхдхРрДѓСПЗБжГЕФжївЊвђЫиЁЃ2007ФъДКЯФжЎНЛЮвЪЁЮоЮ§ЬЋКўРЖ
дхЪТМўдйДЮИјЫЎзЪдДБЃЛЄЧУЯьОЏжгЁЃМьВтЯдЪОЃЌРЖдхБЌЗЂЪБЬЋКўШЋКўNЁЂPЦНОљКЌСПЗжБ№ИпДя4.0КЭ0.13ЁЁmg/LЁЃЛЗОГзЈМвНЈвщгУН№ЪєУОНЋЫЎЬхжаЕФNO3ЃЛЙдЮЊN2ЖјЯћГ§ЮлШОЃЌMgдђзЊБфЮЊMg(OH)2ГСНЕКўЕзЁЃвЊЪЙЬЋКўЫЎжаNЕФЦНОљКЌСПЯТНЕжС0.20ЁЁmg/LЃЌдђУПСЂЗНУзЫЎЬхжагІЭЖШыЕФУОЗлгІВЛЩйгкЁЁЁЁ gЁЃ
ЮхЃК(БОЬтАќРЈСНДѓЬтЃЌЙВ20Зж)
16ЃЎ(10Зж)вбжЊЙЬЬхМзЁЂEЁЂIЁЂFОљЮЊГЃМћЕФЕЅжЪЃЌЦфжаEдкГЃЮТЯТЮЊЦјЬЌЁЃGЮЊАзЩЋНК
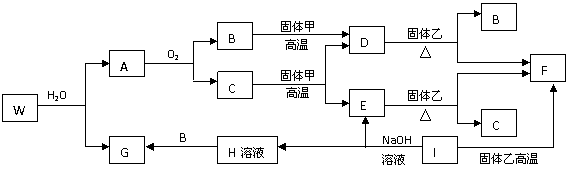 зДГСЕэЃЌМШФмШмНтгкбЮЫсЃЌгжФмШмНтгкЧтбѕЛЏФЦШмвКЁЃAдкГЃЮТЯТЮЊЦјЬЌЃЌгыбѕЦјЭъШЋЗДгІЪБЕФЬхЛ§БШЪЧ1:2ЁЃWЪЧгЩШ§жжДІдкВЛЭЌЖЬжмЦкЕФдЊЫизщГЩЕФЛЏКЯЮяЃЌгыЫЎЗДгІЩњГЩAКЭGЪБЕФЛЏбЇМЦСПЪ§жЎБШЮЊ1:3:3:1ЁЃИїЮяжЪгаШчЯТЭМЫљЪОЕФзЊЛЏЙиЯЕ(ВПЗжЗДгІЕФВњЮяЮДШЋВПБэЪО)ЁЃЪдЛиД№ЯТСаЮЪЬтЃК
зДГСЕэЃЌМШФмШмНтгкбЮЫсЃЌгжФмШмНтгкЧтбѕЛЏФЦШмвКЁЃAдкГЃЮТЯТЮЊЦјЬЌЃЌгыбѕЦјЭъШЋЗДгІЪБЕФЬхЛ§БШЪЧ1:2ЁЃWЪЧгЩШ§жжДІдкВЛЭЌЖЬжмЦкЕФдЊЫизщГЩЕФЛЏКЯЮяЃЌгыЫЎЗДгІЩњГЩAКЭGЪБЕФЛЏбЇМЦСПЪ§жЎБШЮЊ1:3:3:1ЁЃИїЮяжЪгаШчЯТЭМЫљЪОЕФзЊЛЏЙиЯЕ(ВПЗжЗДгІЕФВњЮяЮДШЋВПБэЪО)ЁЃЪдЛиД№ЯТСаЮЪЬтЃК
ЁЁ
 (1)BЕФЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЌЙЬЬхввЕФЛЏбЇЪНПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЛ
(1)BЕФЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЌЙЬЬхввЕФЛЏбЇЪНПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЛ
ЁЁ (2)ЩЯЪізЊЛЏжаЃЌЂйCЁњEЁЁ ЂкDЁњFЁЁ ЂлEЁњFЁЁ ЂмIЁњFЁЁ ЂнIЁњEЁЁ ЂоAЁњB ЦфжаЪє
жУЛЛЗДгІЕФЪЧ(ЬюађКХ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁ (3)аДГіWКЭЫЎЗДгІЕФЛЏбЇЗНГЬЪН____________________________________________,
IКЭNaOHШмвКЗДгІЕФРызгЗНГЬЪН________________________________________ЁЃ
15ЃЎ(10Зж) ЁАРУАцвКЁБЪЧжЦгЁЫЂаПАцЪБЃЌгУЯЁЯѕЫсИЏЪДаПАцКѓЕУЕНЕФЁАЗЯвКЁБЁЃЁАРУАцвКЁБЕФ
жївЊГЩЗжЪЧZn(NO3)2КЭгЩздРДЫЎДјНјЕФClЃЁЂFe3+ЕШдгжЪРызгЁЃ
дкЪЕбщЪвжаЃЌгЩЁАРУАцвКЁБжЦШЁZnSO4ЁЄ7H2OЕФЙ§ГЬШчЯТЃК
Ђй дкЁАРУАцвКЁБжаж№НЅМгШы6molЁЄLЃ1NaOHШмвКЃЌжСpH=8ЮЊжЙЁЃ
Ђк Й§ТЫКѓЕУЕНZn(OH)2ЕШГСЕэЃЌгУШЅРызгЫЎЖрДЮЯДЕгГСЕэЁЃ
Ђл гУ2molЁЄLЃ1ЕФСђЫсЃЌТ§Т§НЋЯДОЛЕФZn(OH)2ШмНтЃЌБЃГжвЛЖЈЕФpHЃЌМгШШжѓЗаЃЌГУШШЙ§ТЫЃЌТЫвКМДЮЊZnSO4ШмвКЁЃ
Ђм ШмвКжазЂШы2 molЁЄLЃ1ЕФСђЫсЃЌЪЙЦфpHБЃГжЮЊ2ЁЁ
ЂХВНжшЂйжаПижЦШмвКpH=8ЕФВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛВНжшЂкжаШчКЮМьбщГСЕэвбОЯДЕгИЩОЛЃПЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЦВНжшЂлжаБЃГжвЛЖЈЕФpHЁЂМгШШЕФФПЕФЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛГУШШЙ§ТЫЕФФПЕФ
ЁЁ ЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЧВНжшЂмЛЙШБЩйЕФВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЫљгУЕФжївЊ
ЁЁ вЧЦїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
14ЃЎЕБЯђРЖЩЋЕФCuSO4ШмвКжаж№ЕЮМгШыАБЫЎЪБЃЌЙлВьЕНЪзЯШЩњГЩРЖЩЋГСЕэЃЌЖјКѓГСЕэгжж№НЅШмНтГЩЮЊЩюРЖЩЋЕФШмвКЃЌЯђЩюРЖЩЋШмвКжаЭЈШыSO2ЦјЬхЃЌгжЩњГЩСЫАзЩЋГСЕэЃКНЋАзЩЋГСЕэМгШыЯЁСђЫсжаЃЌгжЩњГЩСЫКьЩЋЗлФЉзДЙЬЬхКЭSO2ЦјЬхЃЌЭЌЪБШмвКГЪРЖЩЋЃЌИљОнЩЯЪіЪЕбщЯжЯѓЗжЮіЭЦВтЃЌЯТСаУшЪіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎCu2+КЭAg+ЯрЫЦЃЌФмгыNH3НсКЯЩњГЩЭАБТчРызг
BЃЎАзЩЋГСЕэЮЊ+2МлЭЕФФГжжбЧСђЫсбЮЃЌШмгкH2SO4ЗЂЩњИДЗжНтЗДгІ
CЃЎАзЩЋГСЕэЮЊ+1МлЭЕФФГжжбЧСђЫсбЮЃЌдкЫсадЬѕМўЯТЃЌCu+жЛБЛбѕЛЏ
DЃЎЗДгІЙ§ГЬжаЯћКФЕФSO2гыЩњГЩЕФSO2ЕФЮяжЪЕФСПЯрЕШ
ЕкЂђОэЁЁ ЗЧбЁдёЬт(ЙВ72Зж)
13ЃЎИљОнЯТСагаЙиЭМЯѓЃЌХаЖЯЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ )
 ЁЁ
ЁЁ
|


AЃЎгЩЭМЯѓЂёПЩжЊЃЌИУЗДгІдкT1ЁЂT3ДІДяЕНЦНКтЃЌЧвИУЗДгІЕФЁїHЃМ0
BЃЎгЩЭМЯѓЂђПЩжЊЃЌИУЗДгІдкt5НзЖЮNH3ЬхЛ§ЗжЪ§зюДѓ
CЃЎЭМЯѓЂѓЪЧдк10LШнЦїжа850ЁцЪБЗДгІЃЌгЩЭМПЩжЊЕН4minЪБЃЌЗДгІЗХГі51.6kJЕФШШСП
DЃЎгЩЭМЯѓЂєПЩжЊЃЌЯрЭЌЬѕМўЯТЦ№ЪМЪБЭЖШы0.3mol/LXЁЂ0.1mol/LYКЭ0.4mol/LZЗДгІЃЌДяЕНЦНКтКѓЃЌZЕФХЈЖШЮЊ0.4mol/L
11ЃЎФме§ШЗБэЪОЯТСаЗДгІРызгЗНГЬЪНЕФЪЧ(ЁЁ )
ЁЁ ЁЁAЃЎЙ§бѕЛЏФЦЙЬЬхгыЫЎЗДгІЃК2O22-+2H2O == 4OHЃ+O2Ёќ
BЃЎЯђУїЗЏ[KAl(SO4)2]ШмвКжаж№ЕЮМгШыBa(OH)2ШмвКжСSO42ЃЧЁКУГСЕэЭъШЋЃК
2Al3++3SO42Ѓ+3Ba2++6OHЃЃН2Al(OH)3Ё§+3BaSO4Ё§
ЁЁ CЃЎЯђДЮТШЫсФЦШмвКжаЭЈШыЩйСПSO2ЃКClOЃ+SO2+H2OЃНCl-+SO42Ѓ+2H+
DЃЎFeSO4ЫсадШмвКБЉТЖдкПеЦјжаЃК4Fe2++O2+4H+ЃН4Fe3++2H2O
|
|
 ЁЁLaNi5+6Ni(OH)2ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ
)
ЁЁLaNi5+6Ni(OH)2ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ
)
AЃЎЗХЕчЪБДЂЧтКЯН№зїе§МЋ
BЃЎЗХЕчЪБИКМЋЗДгІЃКLaNi5H6+6OHЃЃ6eЃ = LaNi5+6H2O
CЃЎГфЕчЪБбєМЋжмЮЇc(OHЃ)діДѓЁЁЁЁЁЁ DЃЎГфЕчЪБДЂЧтКЯН№зївѕМЋ
10ЃЎДзЫсБЕ[(CH3COO)2BaЁЄH2O]ЪЧвЛжжУНШОМСЃЌгаЙи0.1mol/LДзЫсБЕШмвКжаСЃзгХЈЖШЙиЯЕВЛе§ШЗЕФЪЧ(ЁЁЁЁ )
A.c(Ba2+) ЃОc(CH3COOЃ)ЃОc(OHЃ)ЃОc(H+)
B.c(H+)+2c(Ba2+)= c(CH3COOЃ) +c(OHЃ)
C. c(H+) = c(OHЃ)- c(CH3COOH)ЁЁЁЁЁЁЁЁ ЁЁЁЁ
D. 2c(Ba2+)= c(CH3COOЃ)+ c(CH3COOH)
КЯЬтвтЁЃШєе§ШЗД№АИжЛАќРЈвЛИібЁЯюЃЌЖрбЁЪБЃЌИУаЁЬтЮЊ0ЗжЃЛШєе§ШЗД№АИАќРЈСНИібЁ
ЯюЃЌжЛбЁвЛИіЧве§ШЗЕФЕУ2ЗжЃЌбЁСНИіЧвЖМе§ШЗЕФЕУТњЗжЃЌЕЋжЛвЊбЁДэвЛИіЃЌИУаЁЬтОЭ
ЮЊ0Зж)
9. АЂЗќМгЕТТоГЃЪ§дМЮЊ6.02ЁС1023molЃ1ЃЌЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎ100g98%ЕФХЈСђЫсжаКЌбѕдзгИіЪ§ЮЊ4ЁС6.02ЁС1023
BЃЎ5.6 gЬњЗлгыЯѕЫсЗДгІЪЇШЅЕФЕчзгЪ§вЛЖЈЮЊ0.3ЁС6.02ЁС1023
CЃЎБъзМзДПіЯТЃЌ22.4LCH4КЭCH3ClЕФЛьКЯЮяЫљКЌгаЕФЗжзгЪ§ФПЮЊ6.02ЁС1023
DЃЎ6.2gбѕЛЏФЦКЭ7.8gЙ§бѕЛЏФЦЛьКЯЮяжаЫљКЌгаЕФРызгЪ§дМЮЊ0.7ЁС6.02ЁС1023
8.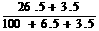
 ЁЁ ФГЮТЖШЯТ100gБЅКЭТШЛЏФЦШмвКжаКЌга26.5gТШЛЏФЦЃЌШєЯђДЫШмвКжаЬэМг3.5gТШЛЏ
ЁЁ ФГЮТЖШЯТ100gБЅКЭТШЛЏФЦШмвКжаКЌга26.5gТШЛЏФЦЃЌШєЯђДЫШмвКжаЬэМг3.5gТШЛЏ
ЁЁЁЁ ФЦКЭ6.5gЫЎЃЌдђЫљЕУШмвКжаШмжЪЕФжЪСПЗжЪ§ЮЊ(ЁЁЁЁ )
AЁЂ30%ЁЁ BЁЂ26.5%ЁЁ CЁЂЁЁЁЁ ЁЁЁЁЁС100%ЁЁ DЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁС100%
7ЃЎ ДгКЃЫЎжаЬсШЁУОЃЌПЩАДШчЯТВНжшНјааЃКЂйАбБДПЧжЦГЩЪЏЛвШщЃЛ Ђкдкв§ШыЕФКЃЫЎжаМгШы
ЪЏЛвШщЃЌГСНЕЁЂЙ§ТЫЁЂЯДЕгГСЕэЮяЃЛ ЂлНЋГСЕэЮягыбЮЫсЗДгІЃЌНсОЇЙ§ТЫЁЂдкHClЦјЬх
ЗеЮЇжаИЩдяВњЮяЃЛ ЂмНЋЕУЕНЕФВњЮяШлШкЕчНтЕУЕНУОЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ AЃЎДЫЗЈЕФгХЕужЎвЛЪЧдСЯРДдДЗсИЛ
BЃЎЂйЂкЂлВНжшЕФФПЕФЪЧДгКЃЫЎжаЬсШЁMgCl2
CЃЎвдЩЯЬсШЁУОЕФЙ§ГЬжаЩцМАЛЏКЯЁЂЗжНтКЭИДЗжНтЗДгІ
DЃЎЕкЂмВНЕчНтЪБвѕМЋВњЩњТШЦј
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com