
题目列表(包括答案和解析)
14.有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些认识,某教师设计了如图所示装置(夹持装置等已省略),其实验操作为:先按图安装好装置,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。试回答下列问题:
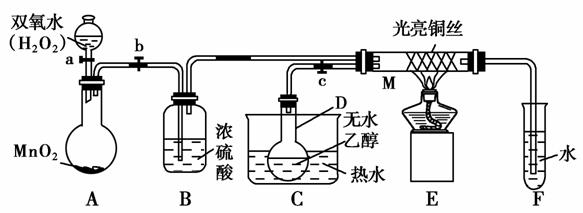
(1)A中发生反应的化学方程式:________________________________________________________________________;
B的作用:________;C中热水的作用:__________________________________________________。
(2)M处发生反应的化学方程式:________________________________________________________________________
____________。
(3)从M管中可观察到的现象:________________________________________________________________________
________________________________________________________________________。
从中可认识到该实验过程中催化剂________化学反应(填“参加”或“不参加”),还可以认识到催化剂起催化作用需要一定的________。
(4)实验进行一段时间后,如果撤掉酒精灯,反应______继续进行(填“能”或“不能”),其原因是________________________________________________________________________
________________________________________________________________________。
[解析] 通过控制氧气的用量,探究乙醇的催化氧化中催化剂Cu的催化机理。乙醇的催化氧化过程实际为O2与Cu在加热时反应生成CuO,CuO再将乙醇氧化为乙醛,且自身被还原为Cu的过程。
[答案] (1)2H2O22H2O+O2↑ 干燥O2 使D中乙醇变为蒸气进入M参加反应,用水浴加热使乙醇气流较平稳
(2)2CH3CH2OH+O2Cu△2CH3CHO+2H2O
(3)受热部分的铜丝由于间歇性地鼓入氧气而交替出现变黑、变红的现象 参加 温度
(4)能 乙醇的催化氧化反应是放热反应,反应放出的热量能维持反应继续进行
13.可用下图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
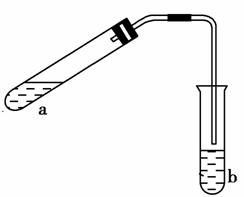
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是____________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是____________________。
(3)实验中加热试管a的目的是:
①________________________________________________________________________;
②________________________________________________________________________。
(4)试管b中加有饱和Na2CO3溶液,其作用是____________________。
(5)反应结束后,振荡试管b,静置。观察到的现象是____________________。
[解析] (1)液体混合一般应将密度大的液体加入到密度小的液体中。(2)加沸石或碎瓷片防止液体暴沸。(3)该酯化反应为可逆反应,升温可加快反应速率。及时将乙酸乙酯蒸出,减小生成物浓度,使平衡向正反应方向移动,有利于乙酸乙酯的生成。(4)挥发出的乙酸与碳酸钠溶液反应,乙醇溶于水。用碳酸钠溶液吸收乙酸和乙醇。且乙酸乙酯在饱和碳酸钠溶液中溶解度更小,利于乙酸乙酯的分层析出。(5)乙酸乙酯为透明状液体,不溶于水且比水轻。
[答案] (1)先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后再加入冰醋酸
(2)在试管a中加入几粒沸石(或碎瓷片)
(3)①加快反应速率 ②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动
(4)吸收随乙酸乙酯蒸出的少量酸性物质和乙醇
(5)b中的液体分层,上层是透明的油状液体
12.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水________。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为__________________________________(不用写反应条件),原子利用率是________。
(3)下列属于乙醇的同系物的是________,属于乙醇的同分异构体的是________。(选填编号)
A.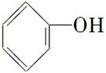 B.
B.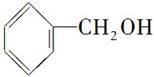
C.乙醚 D.甲醇
E.CH3-O-CH3 F.HO-CH2CH2-OH
(4)乙醇能够发生氧化反应:
①46 g乙醇完全燃烧消耗________mol氧气。
②乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为__________________________________________。
③下列说法正确的是________(选填字母)。
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了乙酸乙酯
[答案] (1)小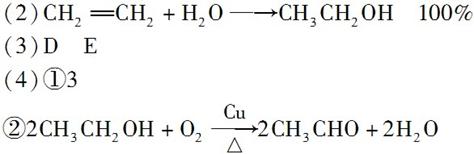
③BCD
11.到目前为止,我国已有上百个地市使用乙醇汽油。
(1)为了便于区分燃料乙醇和食用乙醇,常在燃料乙醇中添加少量煤油,这里利用了煤油的物理性质是________________。
(2)含10%乙醇的汽油在储存和运输过程中应特别注意防水,如果混入了水,汽油中会出现的现象是__________________。
[答案] (1)煤油有特殊气味
(2)混合燃料发生分层
17.(10分)溴酸钾能够作为面粉的增白剂,但已发现溴酸钾是一种致癌物质,过量食用会损害人的中枢神经、血液及肾脏,我国卫生部已经紧急叫停使用溴酸钾作为食品添加剂。已知在酸性条件下有以下反应关系:
①KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2;
②Br2能将I-氧化为I2;
③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其自身被还原为I2。
(1)KBrO3、Br2、KIO3、I2氧化能力由强到弱的顺序为______________________________________________。
(2)请你分析为何溴酸钾具有漂白性?________________________________________________________________________。
(3)向含有1 mol KI的H2SO4溶液中加入含a mol KBrO3的溶液,a的取值不同,所得的产物也不同。
①开始滴加KBrO3溶液时发生反应:6KI+KBrO3+3H2SO4===3K2SO4+3I2+KBr+3H2O,则该反应中氧化剂与还原剂的物质的量之比为________。
②当产物只有I2和Br2时,反应的离子方程式为________________________________________________________________________
________________________________________________________________________。
③我们不能用肉眼看出面包中是否含有KBrO3,请你设计一个检验方案来检验之。
[解析] (1)由①可知氧化性:KBrO3>KIO3,由②可知氧化性:Br2>I2,由③可知氧化性:KIO3>I2,KIO3>Br2,故KBrO3、Br2、KIO3、I2氧化能力由强到弱的顺序为KBrO3>KIO3>Br2>I2。
(2)根据HClO的漂白原理分析解答。
(3)①在反应6KI+KBrO3+3H2SO4===3K2SO4+3I2+KBr+3H2O中,氧化剂为KBrO3,还原剂为KI,可见它们的物质的量之比为1∶6。
②根据题述信息,I-被氧化为I2,BrO3-被还原为Br2,H2SO4提供酸性介质不参与氧化还原反应,且H+转化为H2O,即有:I-+BrO3-+H+―→I2+Br2+H2O,将该离子方程式配平即可。
③根据①提供的反应原理,结合实验设计的基本原则即可解答。
[答案] (1)KBrO3>KIO3>Br2>I2
(2)因KBrO3具有强氧化性
(3)①1∶6 ②10I-+2BrO3-+12H+===5I2+Br2+6H2O ③取一片面包将其用蒸馏水溶解,向其中加入碘化钾淀粉溶液和稀硫酸,如出现蓝色现象,说明面包中含有KBrO3,如无蓝色现象,则无KBrO3。
16.(9分)(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+________―→________+________+________+H2O
(2)反应物中发生氧化反应的物质是________,被还原的元素是________。
(3)反应中1 mol氧化剂________(填“得到”或“失去”)________mol电子。
(4)请将反应物的化学式配平后的化学计量数填入下列相应的位置中。
________+________―→
[解析] (1)根据氧化还原反应的原理是由强氧化性的物质和强还原性的物质反应生成弱氧化性物质和弱还原性物质,在所有物质中氧化性最强的是HNO3,还原性最强的是FeSO4,所以确定此两种物质为该反应的两种反应物,其余为生成物。
其余各部分都可通过配平化学方程式求得:
24+30HNO3===8Fe(NO3)3+8Fe2(SO4)3++15H2O
被氧化元素 ―→ 化合价升高1×8
被还原元素2 ―→2O 化合价降低4×2
然后通过观察法配平其他化学计量数。解答本题的关键是熟悉氧化还原反应的原理。1 mol氧化剂HNO3转化为0.5 mol N2O得到4 mol e-,易忽视。
[答案] (1)FeSO4+HNO3―→Fe(NO3)3+Fe2(SO4)3+N2O+H2O
(2)FeSO4 (3)得到 4
(4)24FeSO4+30HNO3―→
15.(12分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应。又知E溶液是无色的,请回答:
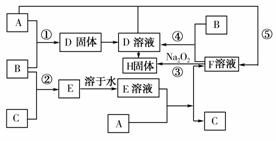
(1)A是______,B是______,C是______,H是________(请填化学式)。
(2)反应①的化学方程式为________________________________________________________________________。
(3)反应③的离子方程式为________________________________________________________________________
____________________________。
(4)反应④的化学方程式为________________________________________________________________________
________________________________________________________________________。
(5)反应⑤的离子方程式为________________________________________________________________________。
[解析] 若猜测A、B、C分别为Fe、Cl2、H2,则A、B反应生成FeCl3,B、C反应生成HCl,盐酸与铁反应生成FeCl2和H2,FeCl2溶液再通入Cl2生成FeCl3,FeCl3与Fe又生成FeCl2,FeCl3与碱液反应生成Fe(OH)3,FeCl2在Na2O2作用下恰好也生成Fe(OH)3,完全符合题目中变化关系。
[答案] (1)Fe Cl2 H2 Fe(OH)3
(2)2Fe+3Cl22FeCl3
(3)4Fe2++4Na2O2+6H2O===4Fe(OH)3↓+O2↑+8Na+
(4)2FeCl2+Cl2===2FeCl3
(5)Fe+2Fe3+===3Fe2+
14.(10分)A、B、C、D、E均为可溶于水的固体,组成它们的离子有:
|
阳离子 |
Na+ Mg2+ Al3+ Ba2+ |
|
阴离子 |
OH- Cl- CO32- SO42- HSO4- |
分别取它们的水溶液进行实验,结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
据此推断它们是
A________;B________;C________;D________;E________。
[解析] 阴、阳离子可能组成的沉淀有:Mg(OH)2↓,Al(OH)3↓,MgCO3↓,BaCO3↓,BaSO4↓。Al3+和CO32-发生反应可生成Al(OH)3↓,能与其他溶液反应产生三种沉淀的A溶液只能是碳酸盐--Na2CO3(因为CO32-不能与Mg2+、Al3+、Ba2+形成可溶性盐),这样就找到了本题的突破口。而能溶解上面两种沉淀的E溶液一定是呈酸性的硫酸氢盐,因为只有HSO4-能电离出H+呈酸性。此外,还有能力能溶解一种沉淀的是强碱,能溶解Al(OH)3↓,所以可推知D为强碱,所以④中应产生两种沉淀,加入过量D溶液溶解的是Al(OH)3,另一种不溶。
[答案] Na2CO3 Al2(SO4)3 MgCl2 Ba(OH)2 NaHSO4
13.(11分)(2010年温州质检)对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。
(1)现有下列6种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2。按照不同的分类标准,它们中有一种物质与其他5种有明显的不同,请找出这种物质,并写出依据(写出两种分类方法):
①________________________________________________________________________。
②________________________________________________________________________。
(2)从上述物质中分别找出两种能相互反应的物质,各写一个非氧化还原反应的方程式和氧化还原反应的方程式:________________________、________________________________________________________________________。
(3)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,请用简单的图示方法表示二者之间的关系:________________________________________________________________________
________________________________________________________________________。
(4)生活中的食醋和淀粉溶液分属于分散系中的________和________,用______________可以鉴别(填化学专用名词)。
[答案] (1)①SO2常温常压下是气体,其余是固体
②Na2O2是过氧化物,其余为酸性氧化物或碱性氧化物(答案不唯一,合理即可)
(2)CaO+SiO2CaSiO3(或MgO+SO2MgSO3等其他合理答案) Na2O2+SO2===Na2SO4
(3)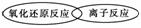
(意思正确、能表示二者的交叉关系即可)
(4)溶液 胶体 丁达尔效应
0.1 mol 0.05 mol 0.1 mol 0.05 mol
可知1 mol Fe可还原2 mol Fe3+,D项正确;
Cu2+、Zn2+均未参加反应,Fe3+的氧化性强于Cu2+,Fe3+可氧化腐蚀铜板,B项不正确,C项正确;据铁原子守恒,可知反应后溶液中n(Fe2+)=0.2 mol,则n(Cu2+)∶n(Fe2+)=0.1 mol∶0.2 mol=1∶2,A项正确。
[答案] B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com