
题目列表(包括答案和解析)
 实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
实验室模拟合成氨和氨催化氧化的流程如下:
 | |||||
 | |||||
 | |||||


已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从上图中选择制取气体的合适装置:
氮气 、氢气 。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有 、 。
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨, (填“会”或“不会”)发生倒吸,原因是: 。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是: ,锥形瓶中还可观察到的现象是: 。
(5)写出乙装置中氨氧化的化学方程式: 。
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。
(B)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:
 |
(1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
 上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在 上,不能直接放在桌面上。
上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在 上,不能直接放在桌面上。
实验所用仪器:A.蒸发皿 B.石棉网 C.泥三角 D.表面皿 E.坩埚钳 F.试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是 。
A.灼烧过程中部分氧化铜被还原 B.灼烧不充分铜未被完全氧化
C.氧化铜在加热过程中分解生成铜 D.该条件下铜无法被氧气氧化
(3)通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、 、冷却结晶、 、自然干燥。
(4)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是: 、 。
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行
次。
(6)若测定结果x值偏高,可能的原因是 。
a.加热温度过高 b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却 d.胆矾晶体部分风化
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如下图所示:
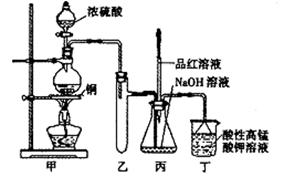
请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,有人认为还有一定量的H2SO4剩余,原因是
,在不增加浓H2SO4的前提下,若使剩余铜片溶解可再加入 (填写两种属于不同类别的物质)。
(2)向反应后的溶液中加入足量的CuO,使剩余的H2SO4全部转化为CuSO4,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①在他们的实验操作中至少称量 次。
②下面是其中一次实验的数据
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
根据上表数据计算判断x的实测值比理论值(x=5) (填“偏大”或“偏小”)。
(3)装置乙的作用是: ;
(4)下列说法正确的是: (填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
f.此装置换上其它药品后,不能制取和收集少量纯净的氯气
第一部分 选择题 (共63分)
1
2
3
4
5
6
7
8
9
B
C
D
D
C
B
A
A
C
10
11
12
13
14
15
16
17
18
C
AD
B
C
B
C
AC
BD
AD
第二部分 非选择题 (共87分)
19.(10分)(1)Mn2++2NH3+CO2+H2O=2NH4++MnCO3↓(2分)
(2)NH3、CO2 (2分) 不需要(2分)
(3)Mn2+(2分) 450(2分)
20.(12分) (l)假设2 :溶液中存在SO32―和HCO3―( 1分)
假设3、溶液中存在HCO3―和SO42―(2和3顺序不限。)(1分)
(2)(10分)
步骤编号
实验操作
预期现象和结论
①
用胶头滴管取少量溶液加入试管A中,再用滴管取过量的lmol/L氯化钡溶液并滴入其中,充分反应后,静置,然后过滤,将沉淀和滤液分别装入另外的两个试管B,C中(3分)
产生白色沉淀,说明原溶液中含有SO42―或SO32―或两者都有(1分)
②
往装有沉淀的试管B中加入过量的2mol/L盐酸,
将产生的气体通入品红溶液(2分)
沉淀部分溶解, 并产生气体.
品红褪色,说明原溶液中一定含有SO42―和SO32―(1分)
③
往装有滤液的试管C中加入2mol/L盐酸;
或加入澄清石灰水(2分)
出现无色气泡,
澄清溶液变浑浊,说明原溶液中含有HCO3―(1分)
④
其它方案合理给分
21(12分)(1)SO2+NaOH=NaHSO3 (1分) HSO3-+H+==SO2+H2O (1分)
(2) AB (2分) 实验时间和加入盐酸酸化的氯化钡溶液后生成沉淀的质量 (2分)
(3)变废为肥,充分利用资源,降低污染 (2分)
(4)+4 (2分)
(5)5CH3OH+6NO3--+6H+ ==5CO2+3N2+13H2O (2分)
22.(10分)⑴MgCl2(熔融)  Mg+Cl2↑
(2分) ⑵Na2S (1分)
Mg+Cl2↑
(2分) ⑵Na2S (1分)
⑶①CO32-+H2O HCO3-+OH-(或2H2SO4)或 HCO3-+H2O
HCO3-+OH-(或2H2SO4)或 HCO3-+H2O H2CO3 +OH- (2分)
H2CO3 +OH- (2分)
②降低含硫烟气的温度(或减小含硫烟气的流速)(2分)
③2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42- (2分)
中和、稀释经氧气氧化后海水中生成的酸(H+),减少污染。(1分)
23.(12分)
⑴.氢氧化钠(或氢氧化钾) (1分)
SO2+2OH?=SO32-+H2O (2分)
2SO32-+O2=2SO42? (2分)
⑵.使SO32-完全氧化为SO42? (2分)
⑶. (或其它合理答案) (2分)
(或其它合理答案) (2分)
⑷.250 mL容量瓶 (1分)
⑸.不合理,会使所测得的铁元素的质量分数偏大(或其它合理答案)(2分)
24.(12分)(1)错误!不能通过编辑域代码创建对象。 (2分)
 (2)9.52 %
(2分)
(2)9.52 %
(2分)
(3)如图所示[注:只要起点在横坐标轴(0,2),
平衡点在横坐标0点后t0前、纵坐标0.2处的示意
图均给分)(4分)
(4)减小 (2分)>(2分)
 25(9分)
25(9分)

26.(1)羟基 羧基 (2分)
错误!不能通过编辑域代码创建对象。 (2分)
(2)
错误!不能通过编辑域代码创建对象。(2分)
(3)A C D (2分)
(4) 错误!不能通过编辑域代码创建对象。 错误!不能通过编辑域代码创建对象。 (2分)
27.⑴分子 (1分) 1s2s22p63s23p63d84s2或[Ar]3d84s2 (2分)
⑵ACD (2分)
⑶①、③、④ (2分)平面三角 (1分)
⑷LaNi5或Ni5La (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com