
题目列表(包括答案和解析)
(1)在一密闭容器中充入1 mol NO2,建立如下平衡:2NO2![]() N2O4,测得NO2的转化率为a%,在其它条件不变的情况下,再充入1 mol NO2,待新平衡建立时,又测得NO2的转化率为b%.试问a、b值的大小关系为________.
N2O4,测得NO2的转化率为a%,在其它条件不变的情况下,再充入1 mol NO2,待新平衡建立时,又测得NO2的转化率为b%.试问a、b值的大小关系为________.
(2)汽车尾气中的主要污染物有CO、NOx,CO分析仪是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是________.

A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,说明汽车尾气中CO的含量越高
(3)阿波罗宇宙飞船上使用的是氢氧燃料电池,试回答下列问题:
①若电解质溶液为KOH溶液,构成燃料电池,则负极反应式为________.
②如把KOH改为稀H2SO4作电解质,则正极反应式为________.
③如把H2改为甲烷,KOH作电解质,则负极反应式为________.
(5分)(1)在一密闭容器中充入1molNO2,建立如下平衡:2NO2 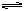 N2O4,测得NO2的转化率为a%,在其它条件不变的情况下,再充入1molNO2,待新平衡建立时,又测得NO2的转化率为b%。试问a、b值的大小关系为___
_。
N2O4,测得NO2的转化率为a%,在其它条件不变的情况下,再充入1molNO2,待新平衡建立时,又测得NO2的转化率为b%。试问a、b值的大小关系为___
_。
(2)汽车尾气中的主要污染物有CO、NOx ,CO分析仪是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是 。

A.负极的电极反应式为:CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,说明汽车尾气中CO的含量越高
(3)阿波罗宇宙飞船上使用的是氢氧燃料电池,试回答下列问题:
①若电解质溶液为KOH溶液,构成燃料电池,则负极反应式为____________ ____,
②如把KOH改为稀H2SO4作电解质,则正极反应式为_____ ___________,
③如把H2改为甲烷,KOH作电解质,则负极反应式为
有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液100mL,并向此稀稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的
 |
试分析NaOH在吸收CO2气体后,在甲、乙两种情况下,所得溶液中存在的溶质是什么?其物质的量之比是多少?产生的CO2气体体积(标况)是多少?
有50 mL NaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液100 mL,并向此稀稀释后的溶液中逐滴加入0.1 mol/L的HCl溶液,产生的CO2气体体积(标况)与所加入的盐酸的体积之间的关系如下图所示:
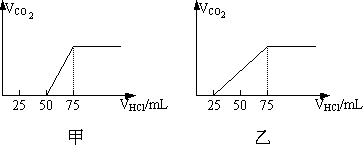
试分析NaOH在吸收CO2气体后,在甲、乙两种情况下,所得溶液中存在的溶质是什么?其物质的量之比是多少?产生的CO2气体体积(标况)是多少?
有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液10mL将其稀释到100mL,并向此稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的CO2气体体积(标准状况下)与所加入的HCl的体积之间的关 系如图所示:试分析:
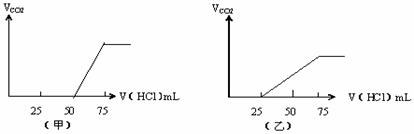
⑴NaOH在吸收CO2气体后,在甲、乙 两种情况下,所得溶液中存在的溶质是
甲: 其物质的量之比是:
乙: 其物质的量之比是:
⑵.且在两种情况下产生的CO2气体(标准状况)
各是甲: mL;乙: mL。
⑶.原NaOH溶液的物质的量浓度是 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com