
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
 »ÁÕº «a°¢b°¢c»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ£Æ
»ÁÕº «a°¢b°¢c»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ£Æ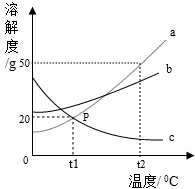 »ÁÕº «a°¢b°¢c»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ£Æ
»ÁÕº «a°¢b°¢c»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ£Æ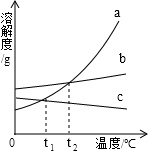
| A°¢‘⁄t2°Ê ±£¨aµƒ»ÐΩ‚∂»µ»”⁄bµƒ»ÐΩ‚∂» | B°¢cµƒ±•∫ջГ∫”…t1°Ê…˝Œ¬÷¡t2°Ê ±£¨±‰≥…≤ª±•∫ջГ∫ | C°¢‘⁄t1°Ê ±£¨a°¢c±•∫ջГ∫÷–»Ð÷ µƒ÷ ¡ø∑÷ ˝œýÕ¨ | D°¢µ±a÷–∫¨”–…Ÿ¡øb ±£¨ø…“‘”√ΩµŒ¬Ω·æßµƒ∑Ω∑®Ã·¥øa |
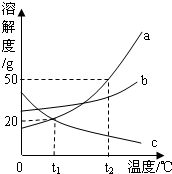 »ÁÕº «a°¢b°¢c»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ£Æ£®1£©0°Ê ±£¨a°¢b°¢c»˝÷÷ŒÔ÷ ÷–£¨»ÐΩ‚∂»◊Ó¥Ûµƒ «
»ÁÕº «a°¢b°¢c»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ£Æ£®1£©0°Ê ±£¨a°¢b°¢c»˝÷÷ŒÔ÷ ÷–£¨»ÐΩ‚∂»◊Ó¥Ûµƒ «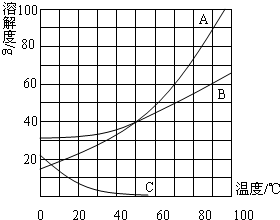 »ÁÕº «A°¢B°¢C»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ æ“‚Õº£¨ ‘ªÿ¥œ¬¡–Œ £Æ
»ÁÕº «A°¢B°¢C»˝÷÷πÃÃÂŒÔ÷ µƒ»ÐΩ‚∂»«˙œþ æ“‚Õº£¨ ‘ªÿ¥œ¬¡–Œ £Ƶ⁄¢ÒæÌ —°‘Ò£®π≤38∑÷£©
“ª°¢£®±æÂ∞¸¿®14–°Ã‚£¨√ø–°Ã‚2∑÷£¨π≤28∑÷°£√ø–°Ã‚÷ª”–“ª∏ˆ—°œÓ∑˚∫œÃ‚“‚°££©
Â∫≈
1
2
3
4
5
6
7
8
9
10
11
12
13
14
¥∞∏
D
D
B
A
A
B
D
B
A
B
B
D
A
B
∂˛°¢£®±æÂ∞¸¿®5–°Ã‚£¨√ø–°Ã‚2∑÷£¨π≤10∑÷°£√ø–°Ã‚÷ª”–“ª∏ˆªÚ¡Ω∏ˆ—°œÓ∑˚∫œÃ‚“‚°£»Ù’˝»∑¥∞∏∞¸¿®“ª∏ˆ—°œÓ£¨∂ý—° ±£¨∏√ÂŒ™0∑÷£ª»Ù’˝»∑¥∞∏∞¸¿®¡Ω∏ˆ—°œÓ£¨÷ª—°“ª∏ˆ«“’˝»∑µƒ∏¯1∑÷£¨—°¡Ω∏ˆ«“∂º’˝»∑µƒ∏¯2∑÷£¨µ´÷ª“™—°¥Ì“ª∏ˆ£¨∏√–°Ã‚æÕŒ™0∑÷°££©
Â∫≈
15
16
17
18
19
¥∞∏
BC
B
A
AB
A
µ⁄¢ÚæÌ ∑«—°‘Ò£®π≤62∑÷£©
»˝°¢£®±æÂ∞¸¿®10–°Ã‚£¨π≤56∑÷£¨√øø’1∑÷£©
|