(2011?宁德一模)某化学研究小组为测定Na
2O
2样品(仅含Na
2O杂质)的纯度,设计了两种实验方案进行探究.
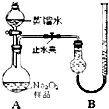
[实验一]取样品0.100g,用如图所示实验装置进行测定.(夹持装置省略)
(1)检查装置A气密性的方法是
夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好;或者关闭分液漏斗活塞,右侧的导管插入水中,用手捂住分液漏斗,看是否有气泡产生,冷却后是否有一段水柱形成
夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好;或者关闭分液漏斗活塞,右侧的导管插入水中,用手捂住分液漏斗,看是否有气泡产生,冷却后是否有一段水柱形成
.
(2)若在实验过程中共产生气体11.20mL(已折算成标准状况),则样品中Na
2O
2的纯度为
78%
78%
.
[实验二]样品溶于水后用盐酸滴定
(3)取一定量样品溶于水并稀释至250mL,配制时,所用到的玻璃仪器除了烧杯和玻璃棒外,还需用到
250 mL容量瓶、胶头滴管
250 mL容量瓶、胶头滴管
.
(4)取上述所配溶液各25.00mL,用一定浓度的标准盐酸滴定,平行实验记录如下表:
| 实验次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 标准盐酸体积(mL) |
23.00 |
24.98 |
25.00 |
25.02 |
由表中数据可知,标准盐酸体积的平均值为
25.00
25.00
mL.若滴定前用上述所配溶液润洗锥形瓶,对实验测定结果产生的影响是
偏高
偏高
(填“偏高”、“偏低”或“无影响”).
[实验分析]实验结果对比分析
(5)小组同学对比两个实验发现,实验一测得的Na
2O
2样品的纯度比理论值明显偏小.经过分析,小组同学认为,明显偏差不是由操作失误和装置缺陷引起的,可能是反应原理上的原因.查阅资料发现:Na
2O
2与水反应产生的H
2O
2未完全分解.
①写出Na
2O
2与水生成H
2O
2的化学方程式
Na2O2+2H2O=2NaOH+H2O2
Na2O2+2H2O=2NaOH+H2O2
.
②若将实验一稍加改进,就能使测定结果接近理论值,写出改进方案:
反应前向Na2O2样品中加入少量MnO2
反应前向Na2O2样品中加入少量MnO2
.


 (2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.
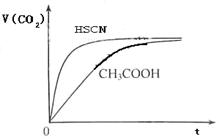
(2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.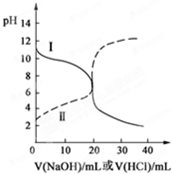 25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1 NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1 NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )