
题目列表(包括答案和解析)
已知E(C-H)=414.4 Kj/mol;E(C![]() C)=615.3 kJ/mol;E(C-C)=347.4kJ/mol;E(H-H)=435.3kJ/mol.
C)=615.3 kJ/mol;E(C-C)=347.4kJ/mol;E(H-H)=435.3kJ/mol.
且已知乙烷(C2H6)可以裂解为乙烯和氢气,请根据化学反应中化学键的改变和键能的变化来推断该反应是放热反应还是吸热反应,并计算反应热的数值.乙烷和乙烯的结构如下:
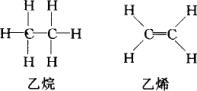
已知E(C-H)=414.4 kJ·mol-1;E(C![]() C)=615.3 kJ·mol-1;E(C-C)=347.4 kJ·mol-1;E(H-H)=435.3 kJ·mol-1
C)=615.3 kJ·mol-1;E(C-C)=347.4 kJ·mol-1;E(H-H)=435.3 kJ·mol-1
且已知乙烷(C2H6)可以裂解为乙烯和氢气,请根据化学反应中化学键的改变和键能的变化来推断该反应是放热反应还是吸热反应,并计算反应热的数值.乙烷和乙烯的结构如下:
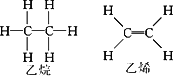
已知E(C-H)=414.4 kJ/mol;E(C![]() C)=615.3 kJ/mol;E(C-C)=347.4 kJ/mol;E(H-H)=435.3 kJ/mol,且已知乙烷(C2H6)可以裂解为乙烯和氢气,请根据化学反应中化学键的改变和键能的变化来推断该反应是放热反应还是吸热反应,并计算反应热的数值.
C)=615.3 kJ/mol;E(C-C)=347.4 kJ/mol;E(H-H)=435.3 kJ/mol,且已知乙烷(C2H6)可以裂解为乙烯和氢气,请根据化学反应中化学键的改变和键能的变化来推断该反应是放热反应还是吸热反应,并计算反应热的数值.
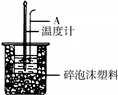 50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在图所示的装置 中进行中和反应,通过测定反应过程中所放出的热量可计算反应热.
50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在图所示的装置 中进行中和反应,通过测定反应过程中所放出的热量可计算反应热.| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com