(2013?泉州)我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na
2CO
3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 |
实验现象 |
实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. |
产生白色沉淀 |
反应的化学方程式:
Na2CO3+CaCl2═CaCO3↓+2NaCl Na2CO3+CaCl2═CaCO3↓+2NaCl |
(2)分析滴加的CaCl
2溶液要过量的原因:
与碳酸钠充分反应
与碳酸钠充分反应
;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na
2CO
3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为
不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大
不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大
.
[方案二]样品与稀盐酸反应,测定Na
2CO
3的质量分数
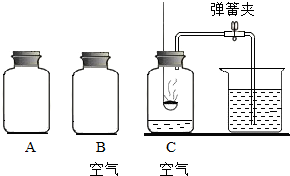
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO
2气体的质量,计算Na
2CO
3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).
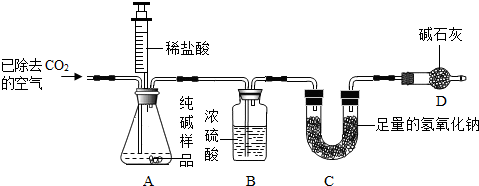
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO
2的空气一会儿,以排尽装置A和B中含有的
二氧化碳
二氧化碳
,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为
Na2CO3+2HCl═2NaCl+H2O+CO2↑
Na2CO3+2HCl═2NaCl+H2O+CO2↑
.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO
2的空气一会儿.根据
质量守恒
质量守恒
定律,装置
C
C
(填标号)在反应前后的质量差就是产生CO
2的质量,由此计算出该样品中Na
2CO
3的质量分数.若没有装置D,将会使测定结果
偏大
偏大
(选填“偏大”或“偏小”).

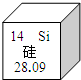 硅元素在现代信息技术产业有着广泛的应用,它在元素周期表中的信息如下图所示.则下列说法正确的是( )
硅元素在现代信息技术产业有着广泛的应用,它在元素周期表中的信息如下图所示.则下列说法正确的是( )
 小红发现切开的苹果会很快变色,于是在老师的指导下,探究氧气是否参与了苹果变色的过程.小红提出假设:氧气参与了苹果变色的过程.老师指导小红要进行对比实验,小红设计并完成了如下2个实验.
小红发现切开的苹果会很快变色,于是在老师的指导下,探究氧气是否参与了苹果变色的过程.小红提出假设:氧气参与了苹果变色的过程.老师指导小红要进行对比实验,小红设计并完成了如下2个实验.