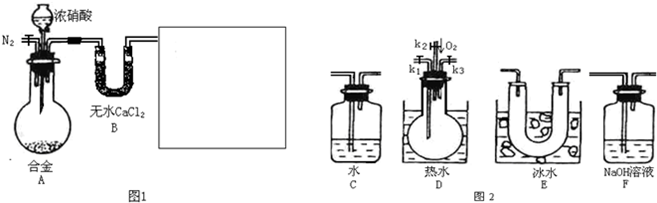
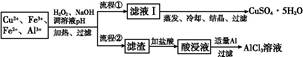
某研究性学习小组对铝热反应(以Al和Fe
2O
3反应为例)实验进行研究.已知Al、Al
2O
3、Fe、Fe
2O
3的熔点、沸点数据如表所示:
| 物质 |
Al |
A12O3 |
Fe |
Fe2O3 |
| 熔点/℃ |
660 |
2054 |
1535 |
1565 |
| 沸点/℃ |
2467 |
2980 |
2750 |
---- |
试回答下列问题:
(1)铝热反应是氧化还原反应,在反应中金属铝表现出
还原
还原
性 (填“氧化”或“还原”).
(2)某同学根据以上数据推测,铝热反应所得到的熔融物中应含有铁、铝两种金属.如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为
氢氧化钠溶液
氢氧化钠溶液
,可观察到的实验现象是
溶液中有气泡出现
溶液中有气泡出现
.
(3)另一同学推测铝热反应得到的熔融物中还含有Fe
2O
3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe
2O
3.则
①物质甲是
KSCN
KSCN
(填化学式).
②该同学的实验方案是否合理?答:
不合理
不合理
(填“合理”或“不合理”).
(4)把l5.12g Fe、Fe
2O
3和Al的混合物与0.5L 2mol?L
-1稀硫酸(足量)充分反应,生成氢气n mol.则
①用浓硫酸配制0.5L 2mol?L
-1的稀硫酸需要的玻璃仪器有烧杯、500mL容量瓶、量筒和
玻璃棒
玻璃棒
、
胶头滴管
胶头滴管
.
②n的取值范围是
0<n<0.84
0<n<0.84
.
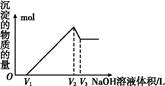
③向反应后的混合溶液中滴加NaOH溶液,当产生沉淀的量达到最大时,参加反应的NaOH的物质的量为
2
2
mol.

 2NO(g)
2NO(g)  H>0
H>0