
题目列表(包括答案和解析)
 某化学兴趣小组对乙酸乙酯的制备实验进行改进,装置如图所示.甲乙丙三个同学看了装置图后有自己的见解:甲认为该实验改进不合理,在实验时会发生倒吸而发生意外;乙认为实验改进后乙酸乙酯中混有的乙酸和乙醇能更好的被饱和碳酸钠溶液所吸收,只要实验结束先把导管从碳酸钠溶液中取出,再停止加热即可防止溶液倒吸;丙认为反应的试管中连接的玻璃导管起到防止倒吸的作用,把导管插入碳酸钠溶液中更有利于杂质被充分吸收.你认为他们中正确的是( )
某化学兴趣小组对乙酸乙酯的制备实验进行改进,装置如图所示.甲乙丙三个同学看了装置图后有自己的见解:甲认为该实验改进不合理,在实验时会发生倒吸而发生意外;乙认为实验改进后乙酸乙酯中混有的乙酸和乙醇能更好的被饱和碳酸钠溶液所吸收,只要实验结束先把导管从碳酸钠溶液中取出,再停止加热即可防止溶液倒吸;丙认为反应的试管中连接的玻璃导管起到防止倒吸的作用,把导管插入碳酸钠溶液中更有利于杂质被充分吸收.你认为他们中正确的是( )| A、甲 | B、乙 | C、丙 | D、都不正确 |
在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定的条件下发生如下反应:
H2(g)+I2(g)![]() 2HI(g)+Q(Q>0)
2HI(g)+Q(Q>0)
反应中各物质的浓度随时间变化情况如图1:
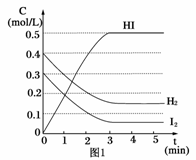
(1)根据图1数据,反应开始至达到平衡时,平衡速率v(HI)为____________。
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K____________(填写增大、减小或不变)
HI浓度的变化正确的是____________(用图2中a-c的编号回答)
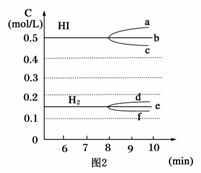
②若加入I2,H2浓度的变化正确的是____________。(用图2中d-f的编号回答)
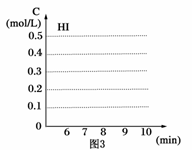
(3)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况。
www.k@s@5@u.com 高#考#资#源#网
(1)现行高中化学课本第一册的学生实验一中设计了CuO对KClO3分解的催化作用的实验,某化学兴趣小组对此产生了兴趣,研究CuO和MnO2对KClO3分解的催化性能。
实验装置:

图4-3
实验记录:
实验序号 | 试管中药品 | 加热时间 | 待测数据 |
1 | 20s |
| |
2 | 20s |
|
问题与讨论
①这里的待测数据是__________________________;
②测气体的体积,是选装置(Ⅰ)还是选装置(Ⅱ)?__________________________;
③实验开始时,是先把导管通入量筒中,还是先加热?理由是什么?
____________________________________________________________________
④实验时间到后,应如何操作?
____________________________________________________________________
(2)已知下列反应:2H2O2+2KMnO4+3H2SO4=K2SO4+MnSO4+5O2↑+8H2O。学生在做此实验时发现:在敞口容器中,当H2O2与酸化的KMnO4溶液混合后,开始产生氧气的速率很慢,一段时间后产生氧气的速率很迅速,经测定溶液的温度基本没变,该学生经过思考认为不可能是温度、浓度、压强的影响,只可能是催化剂的影响。为了证实自己的推断,设计了以下对比实验:
①空白实验 ②起始时加入少量K2SO4固体
③起始时加少量______________ ④起始加入少量水
实验结果:起始反应速率③最快,④最慢,①②基本相同
请解释实验①过程中现象产生的原因:_____________________________________________。
| |||||||||||||||||||||||||||||||
| 选项 | 铝电极 | 电解质 | 负极反应 | 正极反应 |
| A | 负极 | NaOH | 2Al-6e-+8OH-=2AlO2-+4H2O | 6H2O+6e-=6OH-+3H2↑ |
| B | 负极 | 稀盐酸 | 2Al-6e-=2Al3+ | 6H++6e-=3H2↑ |
| C | 正极 | 浓硝酸 | Mg+2e-=Mg2+ | 2NO3-+4H+-4e-=2NO2↑+2H2O |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com