某兴趣小组,对物质A的组成和性质,进行了如下系列研究:
实验1:对A的溶液进行了焰色反应;现象:火焰呈绿色.
实验2:从A的溶液中获取固体A.
实验3:加热干燥的固体A9.4g,出现大量的红棕色气体,经处理集得不溶于水的气体0.56L(标况下),且该气体能使带火星的木条复燃,残留黑色固体4.0g.
实验4:用酒精喷灯再对黑色固体加热,待固体完全变红,又集得能使带火星的木条复燃的气体0.28L(标况下).
资料:①氧化亚铜属碱性氧化物,在酸性介质中能发生自身氧化还原反应;在空气中灼烧会转化为黑色固体,而在高温下较为稳定.②酒精灯的火焰温度一般在400-500℃;酒精喷灯的火焰温度一般在1000℃左右;
根据题中信息,回答下列问题:
(1)实验1中进行焰色反应实验时,一次完整的操作次序为
acaba
acaba
(填序号,可重复);
a.灼烧 b.用盐酸清洗铂丝 c.用铂丝蘸取待测液
(2)实验2中如何从溶液中获取固体A?
蒸发浓缩,冷却结晶
蒸发浓缩,冷却结晶
;
实验中所需主要的仪器有:铁架台(附铁圈)、
蒸发皿、烧杯、玻璃棒、漏斗
蒸发皿、烧杯、玻璃棒、漏斗
;
(3)实验3中
经处理
经处理
集得不溶于水的气体0.56L,这里的“经处理”是将气体通过
碱石灰(或固体氢氧化钠)
碱石灰(或固体氢氧化钠)
,然后用排水法收集气体.
(4)写出实验3中的分解反应式:
;
(5)写出实验4中的分解反应式:
;
(6)实验4中红色固体为纯净物,化学式可以通过计算来确定,也可以通过实验来进一步确定,请设计一个简单的实验确定方案,并写出所发生的反应式.
取红色固体加足量稀硫酸,溶液变蓝且仍有红色固体,可确定原固体为Cu
2O;Cu
2O+H
2SO
4=Cu+CuSO
4+H
2O.或取一定量的红色固体,在空气中充分灼烧,根据灼烧前后固体质量变化来确定;
2Cu
2O+O
2 4CuO
取红色固体加足量稀硫酸,溶液变蓝且仍有红色固体,可确定原固体为Cu
2O;Cu
2O+H
2SO
4=Cu+CuSO
4+H
2O.或取一定量的红色固体,在空气中充分灼烧,根据灼烧前后固体质量变化来确定;
2Cu
2O+O
2 4CuO
.

![]() =
=![]() =
=![]() .
.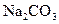 溶液滴入
溶液滴入 溶液中得到蓝色沉淀。
溶液中得到蓝色沉淀。 一种沉淀;
一种沉淀; 一种沉淀;
一种沉淀; 和
和 两种沉淀。
两种沉淀。 和
和 均不带结晶水)
均不带结晶水)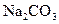 溶液和
溶液和 溶液反应的化学反应方程式为 ;
溶液反应的化学反应方程式为 ;
 的实验现象是 。
的实验现象是 。 和
和 两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。
两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。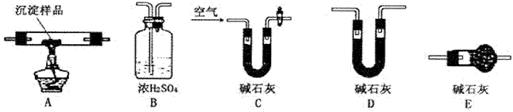
 的质量分数为: 。
的质量分数为: 。