
本章基本线索:做多少功,能量就改变多少;功是能量转化的量度。本章主要概念和规律如下:
多媒体设备
比较、分析、归纳
2.动能定理与机械能守恒定律的区别和联系。
1.功与功率、平均功率与瞬时功率、重力势能与重力做功、动能与动量等概念的理解。
2.对本章所学的基本规律进行复习归纳。
1.对本章所学的基本概念进行复习归纳。
2.熔融盐燃料电池具有高的发电效率,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,制得在650℃下工作的燃料电池。完成有关的电池反应式:
负极反应式:2CO+2CO32--4e-→4CO2
正极反应式:
总反应式:
㈢实验题
有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol·L-1H2SO4溶液中,乙同学将电极放入6mol/L的NaOH溶液中,如下图:
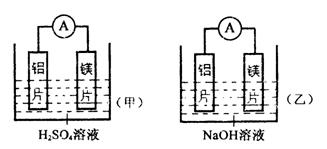
⑴写出甲池中正极的电极反应式: ;
⑵写出乙池中负极的电极反应式和总反应的离子方程式:
负极: ;
总反应的离子方程式: 。
⑶如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出
活动性更强(填元素符号)。
⑷由此实验,可得到如下哪些正确结论?( )
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质。
B.镁的金属性不一定比铝的金属性强。
C.该实验说明金属活动顺序表已过时,已设有实用价值。
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析。
⑸上述实验也反过来证明了“直接利用金属活动性顺序表 判断原电池中的正负极”这种做法 (可靠,或不可靠)。如不可靠,请你提出另一个判断原电池正负极的可行实验方案 (如可靠,此空可不填)。
1.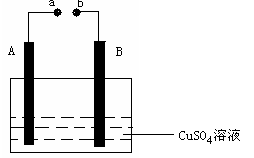 如右图所示装置为在直流电的作用下电解CuSO4溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则:
如右图所示装置为在直流电的作用下电解CuSO4溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则:
⑴a为电源的 极。
⑵写出电极反应方程式:A ,B 。
⑶如果想使反应溶液恢复到原来状态,应该加入 ,加入 g。
6.用Pt电极电解含有各0.1mol Cu2+和X3+的溶液,阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n(mol)关系见下图,则离子的氧化能力由大到小排列正确的是
A.Cu2+>X3+>H+ B.H+>X3+>Cu2+ C.X3+>H+>Cu2+ D.Cu2+>H+>X3+
㈡填空题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com