
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源: 题型:阅读理解
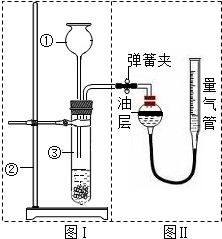 Ⅱ.小明设计了右图实验装置来证明氧化铜能加快双氧水(溶质质量分数约5%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
Ⅱ.小明设计了右图实验装置来证明氧化铜能加快双氧水(溶质质量分数约5%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:| 序号 | 双氧水体积 | 催化剂 | 待测数据 |
| ① | 15mL | 无 | |
| ② | 15mL | CuO(0.5g) | |
| ③ | 15mL | MnO2(0.5g) |
科目:初中化学 来源: 题型:解答题
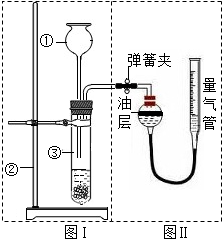 Ⅱ.小明设计了右图实验装置来证明氧化铜能加快双氧水(溶质质量分数约5%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
Ⅱ.小明设计了右图实验装置来证明氧化铜能加快双氧水(溶质质量分数约5%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:| 序号 | 双氧水体积 | 催化剂 | 待测数据 |
| ① | 15mL | 无 | |
| ② | 15mL | CuO(0.5g) | |
| ③ | 15mL | MnO2(0.5g) |
科目:初中化学 来源:柳州 题型:单选题
| A.用pH试纸测得某地水样的pH为6 |
| B.用托盘天平称得某小苏打样品的质量为16.7g |
| C.用烧杯量取了2.5mL的水 |
| D.测得某粗盐中氯化钠的质量分数为90.5% |
科目:初中化学 来源:2010年江苏省镇江市句容市中考化学一模试卷(解析版) 题型:解答题
| 序号 | 双氧水体积 | 催化剂 | 待测数据 |
| ① | 15mL | 无 | |
| ② | 15mL | CuO(0.5g) | |
| ③ | 15mL | MnO2(0.5g) |
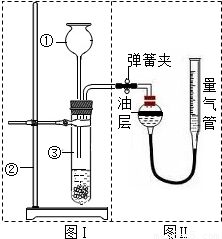
科目:初中化学 来源:四川省中考真题 题型:实验题

科目:初中化学 来源:2008年四川省成都市初中毕业升学统一考试、化学试卷 题型:058
某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学习化学后,同学们意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白.
[提出问题]该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?
[查阅资料]Ⅰ.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表:
Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应).
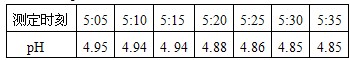
[设计实验1]第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
(1)所降雨水________(填“是”或“不是”)酸雨.
(2)在测定期间内,雨水的酸性________(填“增强”或“减弱”).
[设计实验2]第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2 L的空可乐瓶采集工厂附近的空气样品.采样的具体操作是:________.
(2)向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡.仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:________.
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为:________.
(4)经过过滤、洗涤、烘干,称量固体质量为1.165 mg.
计算:1.165 mg硫酸钡中硫元素的质量为________mg.
由质量守恒定律可知,2 L空气样品中SO2的质量为________mg.
由空气质量标准可得出结论:该厂排放的SO2________.
[发现新问题]考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是________;
你提出的实验改进方案是________.
[反思与应用]为尽快改善该地区的空气质量,请你提出一条合理化建议:________.
科目:初中化学 来源: 题型:阅读理解

科目:初中化学 来源: 题型:计算题
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下: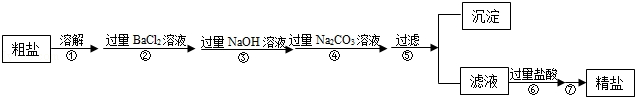
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为 .
(2)请写出实验步骤②中所涉及的化学方程式 .
(3)步骤⑥中加入过量盐酸的目的是 .
(4)步骤②和步骤④ (填“可以”或“不可以”)颠倒,理由是 .
(5)检验步骤④中Na2CO3溶液已过量的方法是 .
(6)加碘食盐相关信息如图所示.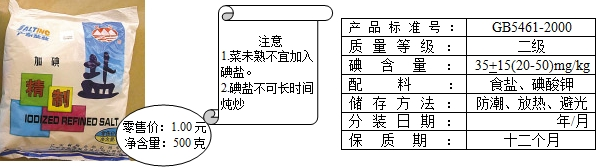
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象 .
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com