
人们的生活质量正在逐步改善,现代厨房中有许多的化学知识.
(1)有的家庭使用的燃料是罐装液化石油气(如图所示),其主要成分有丙烷(化学式为C
3H
8),是石油化工的一种产品,石油不属于
D
D
.
A混合物 B化石能源 C不可再生能源 D 可再生能源
(2)常温下,一个容积为35.5L的液化罐能装下几百升的丙烷,说明丙烷分子
分子之间有间隔
分子之间有间隔
.
(3)丙烷在空气中充分燃烧后生成两种常见氧化物,其化学方程式为:
.
(4)厨房着火,应该立即移走液化罐,这样做的理由是
B
B
.
A.隔绝氧气 B.清除可燃物 C.降低温度到可燃物着火点以下
(5)厨房是同学们的家庭实验室,可以利用许多生活用品进行实验探究.下列实验只利用厨房中的物品不能完成的是
B
B
.
A.鉴别食盐和纯碱 B.检验自来水中是否含有氯离子
C.探究铁制菜刀的生锈条件 D.制取无壳鸡蛋
(6)餐桌上的油污可用酒精除去,其原理是
溶解
溶解
_,也能用洗洁精除去,其原理是
乳化
乳化
.
(7)在冰箱中放入用活性炭制成的“除臭剂”,它对冰箱里的异味具有
吸附
吸附
作用.
(8)切过咸菜的菜刀(未清洗擦干)更易生锈,原因是
铁与氧气和水充分接触时容易生锈,盐溶液能够促进菜刀生锈
铁与氧气和水充分接触时容易生锈,盐溶液能够促进菜刀生锈
.
(9)剖鱼时不小心弄破了鱼胆,胆汁使鱼肉带有苦味,胆汁中产生苦味的主要成分是胆汁酸(属酸类).根据你所掌握的知识,清除苦味,最好使用
D
D
.
(A) 烧碱溶液 (B)食醋 (C)食盐水 (D) 纯碱溶液
(10)做馒头发酵面团时,会产生乳酸等有机酸,蒸馒头前需加进适量的纯碱或小苏打等碱性物质,它们相互作用产生了
二氧化碳
二氧化碳
气体,使蒸出的馒头疏松多孔;若加入的碱性物质过多,可向面团或蒸锅中滴加少许含
醋酸
醋酸
的酸性调味料,否则蒸出的馒头会变涩,颜色发黄.

 人们的生活质量正在逐步改善,现代厨房中有许多的化学知识.
人们的生活质量正在逐步改善,现代厨房中有许多的化学知识. 人们的生活质量正在逐步改善,现代厨房中有许多的化学知识.
人们的生活质量正在逐步改善,现代厨房中有许多的化学知识.

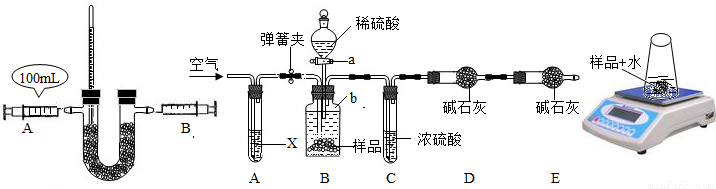
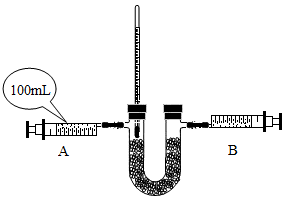 氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.