
üôêÅòçîÕèÒ¥ó¤üâÚçáòúÈ´ÀÀÀÀÈˋ
|
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ2010-2011îÏáõ¡È§´òÀ¡ÈøïòÅ¡Ôà»È´èüÈˋóÖáˋ£₤îÏáÈáãòåƒÚÈ´§ãö—¯ÌÈˋ äãÅëȤîÀåþäã
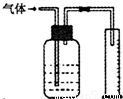 àÓë¥ùªòƒæ¯øûáÉÆûÆÖýãê¢ó½äÍçáäÍ£»
àÓë¥ùªòƒæ¯øûáÉÆûÆÖýãê¢ó½äÍçáäÍ£»¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ2009áõ¡È§´òÀà»û¼òÅ¡Ô¢¥£₤îÏØ£áÈòåƒÚÈ´§ãö—¯ÌÈˋ äãÅëȤîÀåþäã
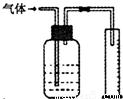 àÓë¥ùªòƒæ¯øûáÉÆûÆÖýãê¢ó½äÍçáäÍ£»
àÓë¥ùªòƒæ¯øûáÉÆûÆÖýãê¢ó½äÍçáäÍ£»¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤà»û¼Ø£áÈ äãÅëȤçËîÀäã
| AÈÛ°»àËÇøîöøÅçáCa2+ÀÂMg2+ÀÂSO42-ȘØâÇö¥ÆàŠH2O¤ëNa2CO3ÀÂBaÈ´OHÈˋ2ÀÂHClàÉؤ |
BÈÛ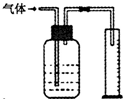 àÓë¥ùªòƒæ¯øûáÉÆûÆÖýãê¢ó½äÍçáäÍ£» |
| CÈÛÆûpHòåø§¢èýãá°ÅôøóôàùÛçápH |
| DÈÛ¤§¤Èǘø£çáǘçæùáøÉüãúÑÅ¢¢ÕâÇÝÈ£ÊǘäÍ |
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤòçîÕäã
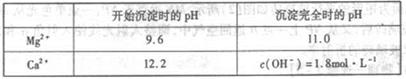
¤ÈùÛòúÆÎÆûú¯ƒ¯¿Ðâ¨çá£₤¿ÊåÙêüæòåÇ,ÇƤÈùÛøÅ¢èäÃàÀ¡¼øø£₤¿ÊåÙêü.àÓë¥òú¿ÊØçèüÑå¤ÈùÛçᥡüŸæܤüâ«ÆûçáòƒØãë¥È´Øîøˆó½äÍXöˆçÓ§ãÝˤëò°îöùÛùªçûÈ£á¡Ø¤¢ÁôÝøÅø¼Øˆ¤˜ÆÅCa2+ÀÂMg2+,Cl-,SO42-ÀÂBr-çàâŠæÆ)úŠ£ÄÇÞȤ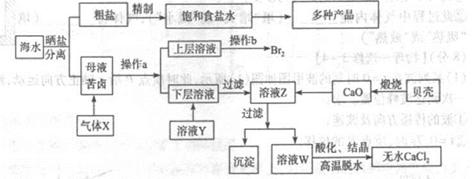
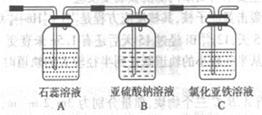
È´1ÈˋåÖÇøîöøŤ˜ÆÅCa2+ÀÂMg2+ÀÂSO42-çàåÆøòȘèØøóòÝùªÆûçáòå¥êöˆ:
| AÈÛîöùà | BÈÛôà£₤ÝçàÉؤ | CÈÛúãî¾£₤áóàÉؤ | DÈÛä¥ùÃáóàÉؤȘ工ÆàŠòå¥êçáù°Å·òú(äŸÝÁ¤é)______ |
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤý£üõ äãÅëȤòçîÕäã

| AÈÛîöùà | BÈÛôà£₤ÝçàÉؤ | CÈÛúãî¾£₤áóàÉؤ | DÈÛä¥ùÃáóàÉؤȘ工ÆàŠòå¥êçáù°Å·òú(äŸÝÁ¤é)______ |


¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ䟢íäã
È´16ñøÈˋ Øåò°îööˆåÙêü§½ÅÅèºýºýÂæܤüâ«Æûçáá°Åˋ¿»°äàÓüôë¥ùªòƒÀÈ
°»àËÇøîöøÅçá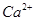 ÀÂ
ÀÂ ¤ë
¤ë âŠæÆȘ¥ÆàŠüôêÅ°êçÚ¥êçáù°Å·òúÈ´äŸÅ·¤éÈˋ_____________ ÀÈ
âŠæÆȘ¥ÆàŠüôêÅ°êçÚ¥êçáù°Å·òúÈ´äŸÅ·¤éÈˋ_____________ ÀÈ
AÈÛ 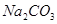 BÈÛ
BÈÛ 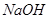 CÈÛ
CÈÛ 
È´2Èˋ§¨ôùؤçá ç¼øêùÃÅå°»àËçáâŠæÆÆÅ___________________ÀÈ
ç¼øêùÃÅå°»àËçáâŠæÆÆÅ___________________ÀÈ
È´3Èˋàùûúü¯¿Ôèü¯îçÓ§ãÝˤëò°îöùÛçá¿ÊØç§Åæ—ôय़¿ÊØçÀÈüôë¥ÝÚòƒçÓ§ãÝˤëNaClàÉؤçáæ¯øûȘXÀÂYòúò₤ᨯ¶ÀÈòçîÕ¢ˆò¥òÝȘåÖê§ÝÔë˜òÝ¡¼çöàŠ¥¡çöñÆäˆàÉؤȘúŠ£ÄÇÞØåüôöòäãȤX¥¨èüçáçÓ¥¨ñÇÆÎò§òú_____ȘåÖX¥¨¡§§■¿Üýšç§çáüøüµòú________________È£YçÓ¥¨èüçáçÓ¥¨ñÇÆÎò§òú______Ș¥šîÕ¡ûçÓ¥¨ñÇÆÎýºöÿçáñ§ñ´òú_______________ ÀÈçÓ§ã àÉؤçáâŠæÆñ§°äò§òú_____________________ÀÈ
àÉؤçáâŠæÆñ§°äò§òú_____________________ÀÈ
È´4Èˋà¶ü·ñø⊰— ƒÏäͤµçáá¡Ø¤øÅ¥ÆàŠ¿»ê¢èºò₤£ØȘ巢è£þçûØ£øø¢èØåîÙ£ñò¿Æûçáó½äÍȘóð£₤îÏò§òú _____________________ ÀÈ
ƒÏäͤµçáá¡Ø¤øÅ¥ÆàŠ¿»ê¢èºò₤£ØȘ巢è£þçûØ£øø¢èØåîÙ£ñò¿Æûçáó½äÍȘóð£₤îÏò§òú _____________________ ÀÈ
È´5Èˋá°ë˜îÏèÒ¥óØ£¡—à¥êüçÓ°ÄÈ´àÓüôë¥ùªòƒÈˋȘá¢çáòú䧃¢ôय़¿ÊØçåÙâÚ¤ëÇøëÙçშêÑåÙâÚȘóðøÅØØæ¯øûøÅXöˆî¶âŠæƧ£££áÊÀÈ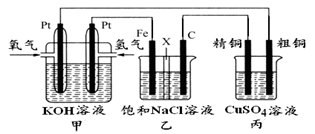
¡ªƒï؈úµ£ÄÇÞüÁ¿ÄöòäãȤ
Âìë´àŠúãó½çáçÓ¥¨öˆ È´äŸÀ¯í»¥¨ÀÝ£·À¯¡¤¥¨ÀÝÈˋȘ¡¤¥¨çáçÓ¥¨ñÇÆÎò§öˆ ÀÈ
ÂÖò₤á¨çÓ¥¨öˆ È´äŸÀ¯î¶¥¨ÀÝ£·À¯Ø¾¥¨ÀÝÈˋȘñÇÆÎØ£ÑöòÝ¥ð¤µÈ˜åÖØØæ¯øûøÅçöàŠñÆäˆàÉؤȘ_ ú½È´äŸÀ¯äº¥¨ÀÝ£·À¯ò₤ᨥ¨ÀÝÈˋçáàÉؤüàÝð¤šÀÈ
ÂÜàÓ¿«ÇøëÙøŤ˜ÆÅÅ¢ÀÂؽçàåÆøòȘݫæ¯øûøÅñÇÆÎØ£ÑöòÝ¥ðȘê·ùÃëÙàÉؤé´Ñ২ ȘäŸÀ¯å—ǵÀÝÀ¯¥¾ ÅÀÀÝ£·À¯ý£ÝðÀÝÈˋÀȃ¨ëÙçÓ¥¨èüçáçÓ¥¨ñÇÆÎò§öˆ______________ÀÈ
ÂÉà¶åÖÝõæ¥æÇ¢—üôȘÆÅ224m Lî¾ó½ýö¥ÆñÇÆÎȘå·ØØæ¯øûøÅäºçÓ¥¨èü躰èçáó½äÍåÖÝõ¢—üôäÍ£»öˆ ȣݫæ¯øûøÅؾ¥¨ö—°—ëÙçáøòê¢öˆ ÀÈ
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤåáÑêâÚ§ã
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ

¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ2012-2013îÏáõè§Ñ¨òÀ¥ûáüòÅ¡Ôà»4åô¿Û¿äÅåîçêñâÚæÜ£₤îÏòåƒÚÈ´§ãö—¯ÌÈˋ äãÅëȤòçîÕäã
Ç¢¥Ÿ(Na2CO3)åÖèºýºèº£ŸøŃÔÆÅ¿Ðñ¤çáÆûëƒÀÈØåüôòúòçîÕòØáÈáãøó¥ŸåÙâÚøóàÀNa2CO3çáê¼°äë¥
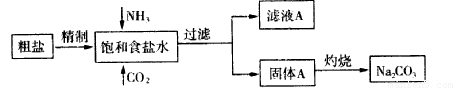
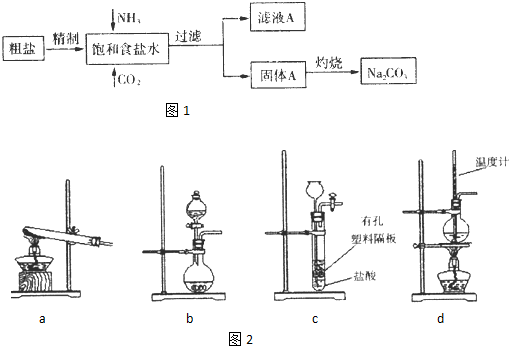
Øîøˆ:ü·Ýˤëò°îöùÛøÅë´àŠNH3ȘCO2¤µñÂ躤ëñÇÆÎöˆNaClȨNH3ȨCO2ȨH2O NaHCO3À»È¨NH4Cl,úŠ£ÄÇÞØåüôöòäãȤ
NaHCO3À»È¨NH4Cl,úŠ£ÄÇÞØåüôöòäãȤ
È´1ÈˋÇøîöøŤ˜ÆÅçáåÆøòâŠæÆÆÅCa2+ȘMg2+ȘSO42-çàÀÈ
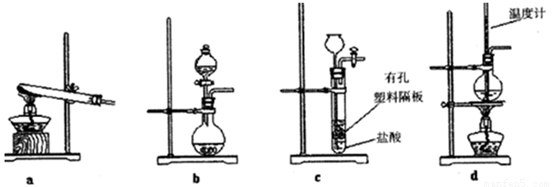
ƒ¨øó°»åÆçáý§øÒù°Å·aÀº_______Àº________Àº________Àºb(äŸæøá¡ÝÁ¤éÈˋÀÈ
aÈÛÇøîöàɧãȘôùàË°êå■ÈÛbÈÛ¥ÆàŠîöùÃç¼pHÈ£cÈÛ¥ÆàŠBa(OH)2àÉؤȣdÈÛ¥ÆàŠNa2CO3àÉؤȣeÈÛ¿»ôù
ü·Ýˤëò°îöùÛøÅüàë´àŠNH3Ș¤µë´àùCO2ȘâÚÆèòú_____________________ÀÈ
È´2Èˋæóèí¿ääÍAøóNa2CO3åÖ_____äŸæøá¡Å·¤éÈˋøŧ½ÅÅÀÈ
aÈÛÜÃÜ— bÈÛí¶ñÂûµ cÈÛèíÝÙ dÈÛæÑÅöó¢
øÊû¼ôùؤAøŤ˜ÆÅNH4+çáñ§ñ´òú__________________________________________________________ÀÈ
ÑåôùؤA§½ÅÅøħÃÏáÉ¿££þçûNH4HCO3Șü·pH=13¤˜Na+ȘK+çáàÉؤøÅ¥ÆàŠèìê¢NH4HCO3ÀÈò¿pH§ççëȘñÇÆÎçáâŠæÆñ§°äò§____________________________________ÀÈ
È´3Èˋüôë¥æ¯øûøÅ°ÈÆûÆÖòçîÕòØøóÝ¡CO2çáòú_____(äŸæøá¡ÝÁ¤éÈˋÈ£ÆûbòƒØãçáæ¯øûøóÝ¡NH3ȘñøؤôˋÑñøÅòÂñéçáòå¥ê______(äŸòå¥êû«°óÈˋȘèíó¢áÖ¢è¥ÆàŠçá¿ääÍòå¥ê__________È´äŸòå¥êû«°óÈˋÀÈ
È´4ÈˋØ£øøäšà£¥ŸƒÏäÍ°èñøòúaNa2CO3ÀÊbNa2CO3ÀÊcH2OȘá°ë˜îÏâ«ÆûüôêÅäÿˋçáòå¥êȘèÒ¥óêùàÓüô¥·çˤüâÚýãÑ´Na2CO3çáøòê¢ñøò»çáòç¢Ëñ§¯¡ÀÈÈ´Øúó¼æåîÀÈˋúŠ¯îòçîÕñ§¯¡äŸà¨È¤¿ˋîÀåþçáòå¥êȤ1.0mol/LH2SO4àÉؤÀÂ1.0mol/L BaCl2àÉؤÀÂüÀ¯ÝùÛÀÂ¥Ÿò₤£ØÀÂCa(OH)2àÉؤÀÂí¶êµùÛ
Âì°óàÀm1gأѴê¢äšà£¥ŸƒÏäÍîªóñȘàÉÆÖòòê¢í¶êµùÛøÅÀÈ
ÂÖ_________________________________________________________________ÀÈ
ÂÜ_________________________________________________________________ÀÈ
ÂÉ¥óùÐäšà£¥ŸƒÏäÍøŤ˜Na2CO3çáøòê¢ñøò»ÀÈ
¿º¥òîÏÅÈÆéîÀ - êñü¯ýÃêÅÝÚ - òåäãêÅÝÚ
¤±ÝÝòÀ£Ëêˆë½öËñ´¤ëý£ê¥ÅéüƒìÝ´ó§ä´ | ë½èüÆŤÎÅéüƒìÝ´æ´ú½ | çÓÅéíˋóÙƒìÝ´æ´ú½ | èÌâºòñÅÕößø¼ØÍÆŤÎÅéüƒìÝ´æ´ú½ | èÌóµúøà´ƒìÝ´æ´ú½
öËñ´¤ëý£ê¥ÅéüƒìÝ´çÓ£¯È¤027-86699610 ƒìÝ´ÆòüðȤ58377363@163.com