
分类是化学学习和研究的常用方法之一.下列物质的分类正确的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.H2O、H2CO3、NH3都是氧化物 |
| B.食用醋、冰红茶、加碘盐都是混合物 |
| C.烧碱、纯碱、熟石灰都属于碱 |
| D.氧气、氯气、铁都是常用氧化剂 |
科目:高中化学 来源:不详 题型:单选题
| A.H2O、H2CO3、NH3都是氧化物 |
| B.食用醋、冰红茶、加碘盐都是混合物 |
| C.烧碱、纯碱、熟石灰都属于碱 |
| D.氧气、氯气、铁都是常用氧化剂 |
科目:高中化学 来源:2012-2013学年河北省邢台市临西实验中学高一(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:2013届福建省南安一中高三上学期期末考试化学试卷(带解析) 题型:实验题
(10分)研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义。某学习小组查阅资料并进行相关探究,请帮忙完成以下探究。
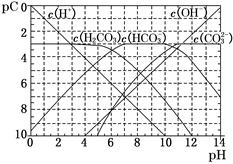
(1)pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3 mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3。如图为25℃时H2CO3溶液的pC-pH图。请回答下列问题:(若离子浓度小于10-5mol/L,可认为该离子不存在)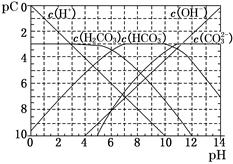
①在同一溶液中,H2CO3、HCO3-、CO32-________(填“能”或“不能”)大量共存。
②H2CO3一级电离平衡常数的数值Ka1 。
。
③人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3-)可以抵消少量酸或碱,维持pH 7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将 。
7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将 。
| A.变大 | B.变小 | C.基本不变 | D.无法判断 |
 CH3OH(g) +H2O(g) △H ;
CH3OH(g) +H2O(g) △H ;
| 容 器 | 甲 | 乙 |
| 反应物 投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
科目:高中化学 来源:2012-2013学年福建省高三上学期期末考试化学试卷(解析版) 题型:实验题
(10分)研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义。某学习小组查阅资料并进行相关探究,请帮忙完成以下探究。
(1)pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3 mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3。如图为25℃时H2CO3溶液的pC-pH图。请回答下列问题:(若离子浓度小于10-5mol/L,可认为该离子不存在)

①在同一溶液中,H2CO3、HCO3-、CO32-________(填“能”或“不能”)大量共存。
②H2CO3一级电离平衡常数的数值Ka1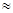 。
。
③人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3-)可以抵消少量酸或碱,维持pH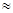 7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将 。
7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将 。
A.变大 B.变小 C.基本不变 D.无法判断
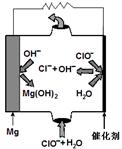
(2)高温时,用CO还原MgSO4可制备高纯MgO。由MgO可制成“镁—次氯酸盐”燃料电池,其装置示意图如图,
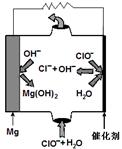
该电池反应的离子方程式为 。
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为: CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H
;
CH3OH(g) +H2O(g) △H
;
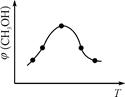
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图
所示,则上述CO2转化为甲醇反应热ΔH 0(填“>” “<”或“=”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
|
容 器 |
甲 |
乙 |
|
反应物 投入量 |
1molCO2 3molH2 |
a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中各物质浓度相同,且起始时维持反应逆向进行,则c的取值范围为 。
科目:高中化学 来源:不详 题型:实验题
 。
。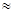 7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将 。
7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将 。| A.变大 | B.变小 | C.基本不变 | D.无法判断 |
 CH3OH(g) +H2O(g) △H ;
CH3OH(g) +H2O(g) △H ;
| 容 器 | 甲 | 乙 |
| 反应物 投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
科目:高中化学 来源: 题型:阅读理解
银及银合金材料是“神七”问天携带研究材料之一。银是日常生活中常见的金属,如银元、银手饰、银器等。
I.某研究性学习小组,设计实验探究某银元中银的质量分数(银元主要成分是银,含少量铜杂质)。取一块银元称质量为Wg,溶于足量的稀硝酸中,充分反应后,在溶液中滴加过量的盐酸,过滤、洗涤、烘干、称重得到固体质量为ag。
(1)根据上述数据,计算该银元中银的质量分数为 。
(2)下列情况使测定银元中银的质量分数偏高 。
A.烘干时,温度偏高 B.加入盐酸不足
C.沉淀没有洗涤干净 D.加入硝酸溶液浓度过大
II.原子利用率是衡量化学反应绿色化的重要依据之一,原子利用率=![]() 。硝酸银是中学重要化学试剂,某同学利用瓶胆上银制取硝酸银:
。硝酸银是中学重要化学试剂,某同学利用瓶胆上银制取硝酸银:
方案1 用14mol/L硝酸溶液溶解银制硝酸银;方案2 用2mol/L硝酸溶液溶解银制硝酸银。
(3)写出化学方程式:方案1 。
(4)方案1原子利用率为 ;方案2原子利用率为 。
你认为符合绿色化学要求的方案是 ,理由是 。
(5)已知硝酸银固体受热易分解,硝酸银溶解度变化规律类似硝酸钾的溶解度变化规律。
从硝酸银溶液中分离硝酸银的方法是 。
①冷却热饱和硝酸银溶液,结晶; ②蒸发溶剂,结晶。
除去硝酸银晶体表面杂质,适宜采用下列方法: 。
A.用蒸馏水洗涤 B.用75%酒精洗涤
C.用饱和硝酸钠溶液洗涤 D.用四氯化碳洗涤
除去硝酸银晶体表面的水份,下列措施合适的是 。
a.加热烘干 b.吹气凉干 c.用滤纸吸干
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com