
下列叙述中正确的是( )
|
科目:高中化学 来源:2012-2013学年江苏省南京市高淳高级中学高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.反应2A(g)![]() 2B(g)+C(g)△H<0 达到平衡时,要使正反应速率增大,B的浓度减少,可采取升温的措施
2B(g)+C(g)△H<0 达到平衡时,要使正反应速率增大,B的浓度减少,可采取升温的措施
B.恒温恒容容器中, A(s)+2B(g)![]() C(g)+D(g) 混合气体的密度不随时间变化而变化,说明已达平衡状态
C(g)+D(g) 混合气体的密度不随时间变化而变化,说明已达平衡状态
C. 平衡常数K与温度有关,温度升高,平衡常数减小,则正向是吸热反应
D. 改变反应物浓度或生成物浓度都会使平衡发生移动,改变平衡常数K
科目:高中化学 来源:2011年山东省实验中学高考化学一模试卷(解析版) 题型:解答题
科目:高中化学 来源:2012届安徽省舒城一中高三第四次月考化学试卷 题型:单选题
可逆反应2A(g)+aB(?) 2C(g)+D(g),其中a为正整数。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( )
2C(g)+D(g),其中a为正整数。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( ) 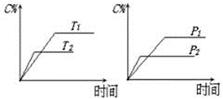
| A.达到平衡后,加入催化剂则C%增大 |
| B.达到平衡后,若升高温度,平衡向右移动 |
| C.a可以为任意的正整数 |
| D.达平衡后,增加B的量,有利于平衡向右移动 |
科目:高中化学 来源: 题型:
| A、①②⑤⑦⑨ | B、③④⑤⑥⑧ | C、②④⑤⑥⑨ | D、①②④⑤⑧ |
科目:高中化学 来源: 题型:
根据下列叙述回答(1)~(3)题。
在一个容积固定的反应容器有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应:
2A(g)+B(g)=2C(g) | D(g)+3E(g)=2F(g) |
各物质的起始加入量如下:A、B、C、D、E、F的物质的量分别为2mol,1mol,0 mol,Xmol,Ymol,Zmol,两边反应达平衡后,隔板恰好在正中间的位置。
(1)恒温时,若向左边容器中充入0.3mol He(He不与A、B、C、D、E、F反应),下列说法正确的是
A.A的物质的量增加 B.B的转化率增大
C.C的物质的量不变 D.F的浓度,体积分数一定都增大
(2)恒温时,若向左边容器中通人的不是He,而是2 molA和1mol B的气体,则下列说法正确的是
A.A的体积分数不变
B.B的转化率降低
C.C的体积分数、浓度都增大
D.右边容器中气体平均相对分子质量增加
(3)恒温时在(2)题的平衡体系中,若向左右两容器中同时再各注入lmolHe,平衡后与(2)题的平衡体系相比,下列说法正确的是
A.C、F的浓度都不变
B.B的转化率,F的分解率都增加了
C.A、D物质的量都增加了
D.A、B、C、D、E、F物质的量都不变
科目:高中化学 来源: 题型:
科目:高中化学 来源:物理教研室 题型:013
若t2>t1,下列叙述正确的是( )
A.![]() >
>![]() ,则平衡右移,Q>0
,则平衡右移,Q>0
B.![]() <
<![]() ,则平衡左移,Q>0
,则平衡左移,Q>0
C.![]() >
>![]() ,则平衡左移,Q<0
,则平衡左移,Q<0
D.![]() <
<![]() ,则平衡右移,Q<0
,则平衡右移,Q<0
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com