
下列方程式中,表示物质的电离且正确的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.H2S?S2-+2H+ |
| B.CH3COONH4?CH3COO-+NH4+ |
| C.HS-+H2O?H2S+OH- |
| D.HS-+H2O?S2-+H3O+ |
科目:高中化学 来源:2012-2013学年广东省深圳高级中学高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:
回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO42-和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为 。
(2)液氨类似于水的电离,试写出液氨的电离方程式 ;
(3)下列离子方程式书写正确的是 。 ?
A.石灰乳与Na2CO3溶液混合:Ca2++CO32—=====CaCO3↓?
B.NH4HSO3溶液与足量的NaOH溶液混合加热:
NH4+ + HSO3- +2OH-![]() NH3↑+SO32- +2H2O?
NH3↑+SO32- +2H2O?
C.酸性条件下KIO3溶液与KI溶液反应生成I2: IO32- +5I-+3H2O====3I2+6OH-
D.AgNO3溶液中加入过量氨水:Ag++NH3·H2O=====AgOH↓+NH4+
E.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-===== BaSO4↓+H2O?
F.CuSO4溶液吸收H2S气体:Cu2++H2S======CuS↓+2H+?
G.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O ===== AlO2- +4NH 4+ +2H2O
H.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
Ba2++2OH-+NH4+ +HCO3-=== BaCO3↓+NH3·H2O+H2O
I.LiAlH4溶于适量水后得到无色溶液,则化学方程式可表示为:
LiAlH4+2H2O ===LiAlO2 +4H2↑
(4)Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为 。
A.3∶2∶1 B.2∶4∶1? C.2∶3∶1 D.4∶2∶1
科目:高中化学 来源: 题型:
回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO42-和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为 。
(2)液氨类似于水的电离,试写出液氨的电离方程式 ;
(3)下列离子方程式书写正确的是 。 ?
A.石灰乳与Na2CO3溶液混合:Ca2++CO32—=====CaCO3↓?
B.NH4HSO3溶液与足量的NaOH溶液混合加热:
NH4+ + HSO3- +2OH- NH3↑+SO32- +2H2O?
C.酸性条件下KIO3溶液与KI溶液反应生成I2: IO32- +5I-+3H2O====3I2+6OH-
D.AgNO3溶液中加入过量氨水:Ag++NH3·H2O=====AgOH↓+NH4+
E.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-===== BaSO4↓+H2O?
F.CuSO4溶液吸收H2S气体:Cu2++H2S======CuS↓+2H+?
G.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O ===== AlO2- +4NH 4+ +2H2O
H.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
Ba2++2OH-+NH4+ +HCO3-=== BaCO3↓+NH3·H2O+H2O
I.LiAlH4溶于适量水后得到无色溶液,则化学方程式可表示为:
LiAlH4+2H2O ===LiAlO2 +4H2↑
(4)Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为 。
A.3∶2∶1 B.2∶4∶1? C.2∶3∶1 D.4∶2∶1
科目:高中化学 来源:2010-2011学年浙江省高三上学期11月月考化学卷 题型:填空题
回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO42-和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为 。
(2)液氨类似于水的电离,试写出液氨的电离方程式 ;
(3)下列离子方程式书写正确的是 。 ?
A.石灰乳与Na2CO3溶液混合:Ca2++CO32—=====CaCO3↓?
B.NH4HSO3溶液与足量的NaOH溶液混合加热:
NH4+ + HSO3- +2OH-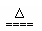 NH3↑+SO32- +2H2O?
NH3↑+SO32- +2H2O?
C.酸性条件下KIO3溶液与KI溶液反应生成I2: IO32- +5I-+3H2O====3I2+6OH-
D.AgNO3溶液中加入过量氨水:Ag++NH3·H2O=====AgOH↓+NH4+
E.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-===== BaSO4↓+H2O?
F.CuSO4溶液吸收H2S气体:Cu2++H2S======CuS↓+2H+?
G.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O ===== AlO2- +4NH 4+ +2H2O
H.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
Ba2++2OH-+NH4+ +HCO3-=== BaCO3↓+NH3·H2O+H2O
I.LiAlH4溶于适量水后得到无色溶液,则化学方程式可表示为:
LiAlH4+2H2O ===LiAlO2 +4H2↑
(4)Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为 。
A.3∶2∶1 B.2∶4∶1? C.2∶3∶1 D.4∶2∶1
科目:高中化学 来源: 题型:填空题
把大气中的游离态的氮转化为氮的化合物的过程称为固氮。生物固氮和大气固氮(闪电时N2转化为NO)属于自然固氮,这远不能满足人类的需要。工业固氮(合成氨)是目前人工固氮的主要方法。有关大气固氮和工业固氮的平衡常数K值分别如下表一和表二。
表一:N2+ O2 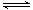 2NO
2NO
| 温度 | 27℃ | 2000℃ |
| K值 | 3.84×10-31 | 0.1 |
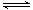 2NH3
2NH3 | 温度 | 25℃ | 350℃ | 400℃ | 450℃ |
| K值 | 5×108 | 1.847 | 0.507 | 0.152 |
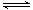 2NO是吸热反应
2NO是吸热反应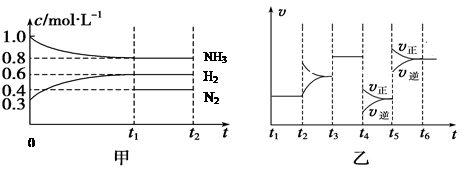
科目:高中化学 来源:2013-2014学年福建省四地六校高三上学期第三次月考化学试卷(解析版) 题型:填空题
(1)R+与S2–所含电子数相同,则R元素的原子序数为
(2)一种基于酸性燃料电池原理设计的酒精检测仪,正极上的反应为:O2 + 4e– + 4H+ = 2H2O,检测有酒精时,电解质溶液中的H+向 极移动,该电池负极上的反应为:
(3)X、Y、Z、M、G五种分属三个短周期主族元素,且原子序数依次增大。Z存在质量数为23,中子数为12的核素A;Y、M同主族,可形成MY2、MY3两种分子。
回答下列问题:
①用化学符号表示核素A: ;
②上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),写出该物质与氢氧化钠溶液反应的离子方程式: ;
③X2M的电子式为 ;
④ZG用途广泛,下列说法正确的是: 。
A、作调味剂 B、用于食物防腐 C、用于氯碱工业 D、用于医疗
科目:高中化学 来源: 题型:填空题
(1)R+与S2–所含电子数相同,则R元素的原子序数为
(2)一种基于酸性燃料电池原理设计的酒精检测仪,正极上的反应为:O2 + 4e– + 4H+ = 2H2O,检测有酒精时,电解质溶液中的H+向 极移动,该电池负极上的反应为:
(3)X、Y、Z、M、G五种分属三个短周期主族元素,且原子序数依次增大。Z存在质量数为23,中子数为12的核素A;Y、M同主族,可形成MY2、MY3两种分子。
回答下列问题:
①用化学符号表示核素A: ;
②上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),写出该物质与氢氧化钠溶液反应的离子方程式: ;
③X2M的电子式为 ;
④ZG用途广泛,下列说法正确的是: 。
| A.作调味剂 | B.用于食物防腐 | C.用于氯碱工业 | D.用于医疗 |
科目:高中化学 来源:不详 题型:填空题
| A.作调味剂 | B.用于食物防腐 | C.用于氯碱工业 | D.用于医疗 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com