
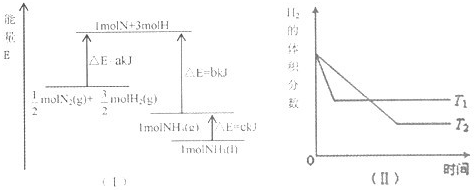
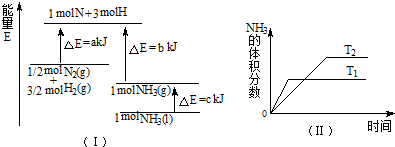
T℃时,N2与H2反应生成NH3,其能量变化如图(I)所示.若保持其他条件不变,温度分别为T1℃和T2℃时,NH3的体积分数与时间的关系如图(II)所示.则下列结论正确的是( )
|
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:多选题
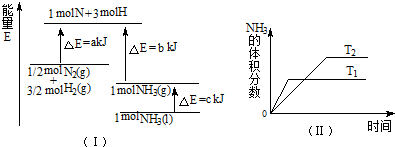
A.该反应的热化学方程式:
| ||||
| B.该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1);△H=2(a-b-c)kJ?mol-1 | ||||
| C.其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大 | ||||
| D.Tl>T2,且正反应为放热反应. |
科目:高中化学 来源:兖州市模拟 题型:单选题
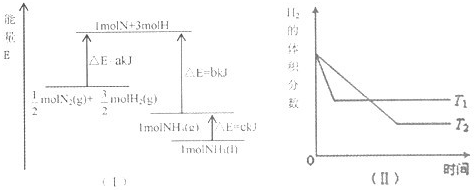
A.该反应的热化学方程式是:
| ||||
| B.该反应的热化学方程式:N2(g)+3H2(g)?2NH3(l)△H=-2(b+c-a)kJ?mol-1 | ||||
| C.T1<T2,且正反应为放热反应 | ||||
| D.其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大 |
科目:高中化学 来源:2012-2013学年江苏省南通市海门市三厂中学高二(上)期中化学试卷(选修)(解析版) 题型:选择题
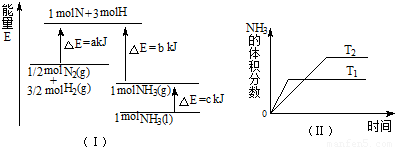
 N2(g)+
N2(g)+ H2(g)=NH3(g);△H=(a+b)kJ?mol-1
H2(g)=NH3(g);△H=(a+b)kJ?mol-1科目:高中化学 来源:2010年山东省济宁市兖州市高考化学模拟试卷(9月份)(解析版) 题型:选择题

 N2(g)+
N2(g)+ ?NH3(g)△H=-(a+b)kJ?mol-1
?NH3(g)△H=-(a+b)kJ?mol-1科目:高中化学 来源: 题型:
T ℃时,N2与H2反应生成NH3,其能量变化如图(Ⅰ)所示。若保持其他条件不变,温度分别为T1 ℃和T2 ℃时,H2的体积分数与时间的关系如图(Ⅱ)所示。则下列结论不正确的是
 |
A.该反应的热化学方程式:![]() N2(g)+
N2(g)+ ![]() H2(g)=NH3(g);△H = (a+b)kJ?mol-1
H2(g)=NH3(g);△H = (a+b)kJ?mol-1
B.该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1);△H = 2(a-b-c)kJ?mol-1
C. T1>T2,且正反应为放热反应
D. 其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:填空题
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)一定温度下,在1L容积恒定的密闭容器中充入2 mol N2和8molH2并发生反应。10min达平衡,测得氨气的浓度为0.4 mol·L-1,此时氮气的转化率为________。若想提高氨气的产率,根据化学平衡移动原理,提出合理的建议______________(写出一条即可)。
(2)如图是1mol NO2(g)和1mol CO(g)反应生成lmol CO2(g)和1 mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式_____________________。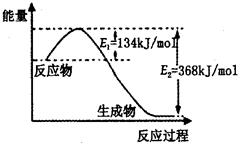
(3)在容积恒定的密闭容器中,进行如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,其平衡常数K与温度T的关系如下表:
2NH3(g) △H<0,其平衡常数K与温度T的关系如下表:
①该反应的平衡常数表达式:K=_____________;
②试判断K1__________K2(填写“>”“=”或“<”=;
③NH3(g)燃烧的方程式为:4NH3(g)+7O2(g)=4NO2(g)+6H2O(l),已知:
H2(g)+O2(g) 2H2O(l) △H=-483.6 kJ/mol
2H2O(l) △H=-483.6 kJ/mol
N2(g)+2O2(g) 2NO2(g) △H=+67.8 kJ/mol
2NO2(g) △H=+67.8 kJ/mol
N2(g)+3H2(g) 2NH3(g) △H=-92.0 kJ/mol
2NH3(g) △H=-92.0 kJ/mol
请计算NH3(g)的燃烧热________kJ/mol。
科目:高中化学 来源:2011-2012学年北京市丰台区高三(上)期末化学试卷(解析版) 题型:解答题
| T/K | 398 | 498 |
| 平衡常数K | K1 | K2 |

科目:高中化学 来源:江苏模拟题 题型:填空题

 CO2+H2
CO2+H2  2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中 T1____573K(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中 T1____573K(填“>”、“<”或“=”)。 
 4NO(g)+6H2O(g) △H=
4NO(g)+6H2O(g) △H=
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com