
【题目】研究和控制化学反应条件有重要意义。
(1)同学们想探究过氧化氢的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 30%双氧水 的质量(g) | 加入的水 的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
1 | 10 | 20 | 5 | 200 |
2 | 20 | 20 | 5 | 100 |
3 | 30 | 20 | ______________ | 67 |
①取用二氧化锰的仪器是 ______。
②二氧化锰在过氧化氢的分解中起_________作用。
③实验3中,加入的二氧化锰质量为_________g。
④相同条件下,实验3产生氧气的速率最快,说明_________。
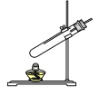
(2)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气。为了验证加热过氧化氢也可以产生氧气,同学们选择右图装置(气密性良好)进行实验。实验中观察试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是___________,同学分析原因后,采用了______法收集气体,再检验,证明加热双氧水也可产生氧气。
【答案】药匙 催化 5 过氧化氢溶液浓度越大,其分解的速率越快 加热水分蒸发加快,收集的氧气中含有大量的水蒸气,使氧气纯度降低 排水
【解析】
(1)①向试管中加入粉末状固体时,应将试管横放,用药匙或纸槽将固体放在试管底,然后将试管竖起,使固体滑到试管底;二氧化锰是固体粉末,取用时要用药匙; ②二氧化锰是过氧化氢分解常用的催化剂,能加快过氧化氢的分解速率,催化剂的作用叫催化作用;实验探究双氧水的溶质质量分数对反应速率的影响。所以在其他条件相同的情况下进行了三次实验,所以实验3中,根据控制变量原则,加入的二氧化锰质量为5g;
(2)通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气。为了验证加热过氧化氢也可以产生氧气,选择装置(气密性良好)进行实验。实验中观察试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是加热水分蒸发加快,收集的氧气中含有大量的水蒸气,使氧气纯度降低,同学分析原因后,采用了排水法收集气体,使混在氧气中的水蒸气被冷凝,使收集的氧气较纯,再检验,带火星的木条复燃,证明加热双氧水也可产生氧气。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
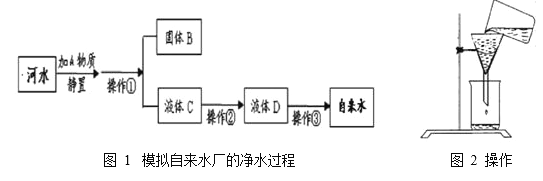
【题目】水是维系生命的重要物质.之一,天然水需净化才能饮用,下图是水厂净化水的过程:
(1)下列属于该自来水厂净水方法的是____________(填字母序号);
A.沉淀 B.过滤 C.消毒 D.蒸馏
(2)经过自来水厂净化后的水属于_______________(填“纯净物”或“混合物”);
(3)国家新版《生活饮用水卫生标准》从2012年7月1日起全面实施,其中消毒剂除氯气以外,同时补充了一氯胺(NH2Cl)、二氧化氯、臭氧(O3)三种物质,其中二氧化氯的化学式为 _____________;
(4)小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成自来水。其实验过程如下所示,请回答以下问题。
I : 图 1 中操作①的名称是 ________,在该操作中,小刚操作如图 2 所示,请你写出其中两处明显的错误:① ________________② ___________________;
II :图1操作②常用活性炭来除去一些异味和色素,这是利用活性炭的 __________性;
III:小刚发现经净化后的液体D 是硬水,要降低水的硬度,日常生活中可以采用的方法是: ________。
查看答案和解析>>
科目:初中化学 来源: 题型:
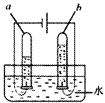
【题目】生活离不开水,我们可以从组成、结构、性质等角度认识水。如图所示是电解水的实验装置图,下列说法正确的是( )
A. 该实验中的电源是交流电源,水中加入少量硫酸钠目的是增强水的导电性
B. 水分子由2个氢原子和1个氧原子构成
C. 该反应中不变的粒子是水分子、氢原子、氧原子
D. 试管a、b中产生气体的体积数量关系是Va=2Vb
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢气和氯气的混合物在光照或点燃的条件下发生爆炸,生成氯化氢,其反应的微观示意图如下。下列说法正确的是
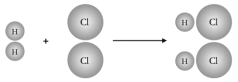
A. 此反应过程中分子的种类没有发生改变
B. 此反应过程中只有物质变化,没有能量变化
C. 在任何条件下,H2 和 Cl2 一定不能大量共存
D. 氢气、氯气、氯化氢都是由分子构成的物质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某粒子的结构示意图,回答下列问题:
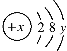
(1)x表示____;y表示____。
(2)当x=12时,y=___。
(3)当x=17时,该粒子带1个单位负电荷,则y=____。
(4)当x=13时,该粒子易____电子,变成带____(填“正”或“负”)电荷的____(填离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中,利用下列装置可以制取某些气体,请回答下列问题。

(1)写出带标号的仪器的名称:①__________ ;②__________。
(2)向气体发生装置内加入药品前,应该进行的操作是_________。
(3)实验室若用高锰酸钾制取氧气,选择的发生装置是_________;用双氧水制氧气的化学方程式为 _________
(4)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是_____________;收集装置是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答问题:
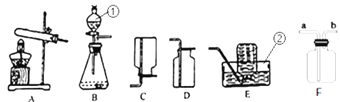
(1)写出上图所示装置中标有序号的仪器名称:①_______________ ② ______________。
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气,所选用的发生装置是________(选填装置序号,下同),请写出符号表达式:______________________,二氧化锰在该反应中的作用是_________。 若用F装置收集氧气,则验满的方法为____________________。
(3)甲烷是一种无色无味、难溶于水、密度比空气小的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷时,发生装置应选_________,若要收集一瓶干燥的甲烷气体,收集装置可选用____________(在“C、D、E”中选择)。
(4)下列图像表示在用过氧化氢溶液和二氧化锰的混合制取氧气的过程中某些量的变化趋势,其中能正确反应变化关系的是________ 。
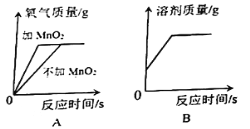
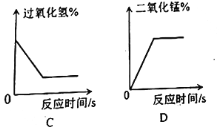
(5)走进实验室,寻找新的催化剂。
(提出问题)红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(实验探究)
实验步骤 | 实验现象 | 实验结论及解释 | |
I |
| A中无明显现象,B中产生大量能使带火星木条复燃的气体。 | 红砖粉能改变过氧化氢分解速率 |
II | B试管中重新加入5%的过氧化氢溶液,反应停止后,过滤分离出红砖粉,洗涤、干燥、称量 | B试管又产生大量能使带火星木条复燃的气体,滤渣的质量等于ag | 红砖粉末的____________在反应前后均没发生变化,能作为过氧化氢分解的催化剂。 |
III |
| 两支试管中均产生气泡,且___________________________________________。 | 红砖粉末的催化效果没有二氧化锰粉末好。 |
(拓展应用)
①实验中用到溶质质量分数为5%的过氧化氢溶液,若用10g溶质质量分数为30%的过氧化氢溶液来配制,加水的体积为____________mL。
②已知硫酸铜也可以作为过氧化氢分解的催化剂,向101.2g一定溶质质量分数的过氧化氢溶液中加入2g硫酸铜粉末。充分反应后得到溶质质量分数为2%的溶液,则生成氧气 _____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年国庆节长假期间,小刚同学到长江三峡旅游,带回来一瓶山峡的江水,他在实验室模拟自来水厂的净水过程,最终制成自来水。其实验流程如下图所示。请回答以下问题。
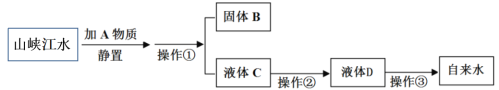
(1)操作①的名称是_________;现实验室提供了烧杯、漏斗、铁架台、滤纸和玻璃棒等用品,在该操作中,玻璃棒的作用是__________。
(2)对于饮用水而言,长期饮用硬水对人体健康不利,区分硬水和软水最简单的方法是加_____________。
(3)操作②主要是除去一些异味和色素,在实验中他应选用的物质是_____________,该过程主要是___________(填“物理”或“化学”)变化。
(4)小刚发现经过净化后的液体D是硬水,日常生活中常常用__________的方法使其软化后使用。操作③是消毒杀菌,这个过程主要是_________(填“物理”或“化学”)变化。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法中正确的是
A. K2FeO4是一种高效净水剂,其中Fe的化合价为+3价
B. 稀释10g质量分数为98%的浓硫酸, 可得到质量分数为10%的稀硫酸98g
C. 在电解水的实验中,产生的H2和O2体积比约为1:2
D. 在化学反应前后分子数目肯定没有变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com