
| 体重 | 小于等于15千克 | 15~23千克 | 23~40千克 | 大于40千克 |
| 每次用量 | 30mg | 45mg | 60mg | 60mg |
分析 (1)根据莽草酸分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析.
(6)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析.
(7)解答根据“体重-剂量表”可知体重是35千克,每次用量60mg,再根据题意计算即可.
解答 解:(1)1个莽草酸分子是由7个碳原子、10个氢原子和5个氧原子构成的,则莽草酸(C7H10O5)分子中原子个数比为7:10:5.
(2)莽草酸(C7H10O5)中碳元素与氧元素的质量比为(12×7):(16×5)=21:20.
(3)莽草酸的相对分子质量为12×7+1×10+16×5=174.
(4)莽草酸中氢元素的质量分数为$\frac{16×5}{174}$×100%≈46.0%.
(5)87克莽草酸中含氧元素质量为87g×46.0%=40g.
(6)设x质量的莽草酸(C7H10O5)中含有80克氧元素,
x×46.0%=80g,
x=174g
(7)由题意体重是35千克,由“体重-剂量表”每次用量60mg,每天服用“达菲”胶囊(每颗胶囊含“达菲”75mg)2次,一个疗程5天,该患儿一个疗程共需服用60mg×2×5=600mg,共需达菲片数是600mg÷75mg=8颗.
故答案为:(1)7:10:5;(2)21:20;(3)174;(4)46.0%;(5)40;(6)174;(7)8.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:推断题
| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 溶解度/g | 122 | 130 | 140 | 160 | 190 | 220 | 250 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
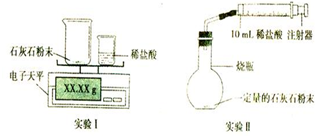
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
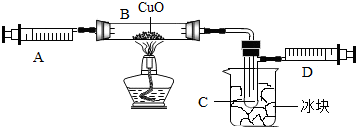
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 酸、碱是日常生活和实验中常用的两类物质.
酸、碱是日常生活和实验中常用的两类物质.| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 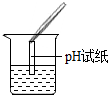 | 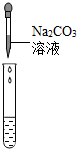 | 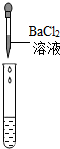 |
| 实验现象 | 试纸变色,对比标准比色卡:pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
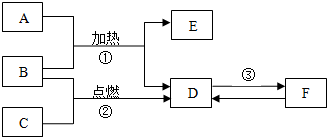
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com