
【题目】将金属镓做的勺子放入90℃的热水中,勺子很快就熔化;当水温降到26℃时,水中有凝 固的金属镓。己知镓在元素周期表中的信息和镓的一种粒子的结构示意图分别如图2、图3所示。下列说法错误的是

A. 金属镓的熔点高于26℃,低于90℃
B. 镓的相对原子质量是69.72
C. 镓原了核外有31个电子
D. 图3所表示粒子的化学符号是Ga
【答案】D
【解析】
在元素周期表中,元素名称左上角的数字为原子的序数,右上角是该元素的符号。名称下边的数值是原子的相对原子质量。在原子结构示意图中,小圆圈表示原子核,圆圈内的数字表示质子数,质子数决定原子的类别,弧线表示电子层,最外层电子数决定原子的化学性质,质子数决定原子的类别。
A. 将金属镓做的勺子放入90℃的热水中,勺子很快就熔化;当水温降到26℃时,水中有凝 固的金属镓,由此可知金属镓的熔点高于26℃,低于90℃,选项正确;
B. 由图中信息可知镓的相对原子质量是69.72,选项正确;
C. 同一原子中,质子数=核外电子数=核电荷数=原子序数,结合题中信息可知镓原了核外有31个电子,选项正确;
D. 图3所表示粒子质子数大于核外电子数,为带3个单位正电荷的离子,的化学符号是Ga3+,选项错误。故选D。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如右图,下列说法中正确的是

A. t1℃时,三种物质的溶解度大小关系为A>C>B
B. t1℃时,65 g A的饱和溶液中含有15 g A
C. t2℃时,A、B两溶液的溶质质量分数相同
D. B中含有少量杂质A时,可采用降温结晶的方法提纯B
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水乃万物之本原

(1)水的净化如图是一种水净化装置,可以除去 99.3% 的细菌和病毒。该装置中活性炭的作用是___,生活中使硬水软化的方法是____。
(2)水的电解通电一段时间后,正负两极收集气体体积比为____,反应的化学方程式是____。
(3)水的用途 对图中分析有误的是____(填序号)。

A.烧杯中的水便于观察是否有气体排出
B.集气瓶中的水主要用于降温
C.试管中的水作为反应物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图所示装置测定空气中氧气的含量。在玻璃管中放入过量铜粉,管中的空气体积为50 mL,将活塞拉至30 mL刻度处的注射器和瘪的气球接在玻璃管的两端,点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温,将气球中的气体全部挤入玻璃管,此时注射器的活塞停在14mL刻度处。下列说法错误的是

A. 用硫粉代替铜粉不能达到实验目的
B. 铜粉过量是为了使装置内的氧气完全反应
C. 实验测得空气中氧气的体积分数为17.5%
D. 未冷却至室温即读取注射器读数会导致实验结果偏小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示仪器(装置)回答问题(省略夹持仪器)。
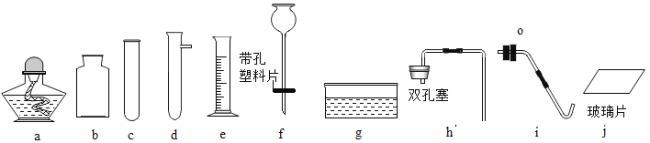
(1)仪器e的名称是__________。
(2)写出高锰酸钾制氧气的化学方程式:_________。制备并收集用于做铁丝燃烧实验的氧气,组装装置除需仪器a、c、i.j外,还需选用_______ (填标号),铁丝在氧气中燃烧的现象:_________。
(3)写出锌粒和稀硫酸制氢气的化学方程式:__________;欲使反应随时发生或终止,应选取仪器___ (填标号)组装发生装置。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是目前使用最广泛的金属。请回答下列问题。
(1)身体一旦缺铁可能患有的疾病是__________。
(2)工业炼铁的主要设备是_________。工业上选用赤铁矿(主要成分Fe2O3)为原料炼铁的化学反应方程式为_________。
(3)不锈钢是铁、铬(Cr) ,镍(Ni)的合金,常用来制造医疗器械、餐具等。通过实验得知,铬和镍两种金属都能与稀硫酸反应生成氢气,分别得到硫酸铬(CrSO4)和硫酸镍(NiSO4)溶液。请写出铬(Cr)与稀硫酸反应的化学方程式_______________。
(4)铁生锈的主要过程为![]()
Ⅰ.写出转化①的化学方程式_________________。
Ⅱ.转化③生成![]() ,则x≤______________(x为整数)。
,则x≤______________(x为整数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】完成下列变化的化学方程式。
(1)水通电分解:_____________。
(2)碳酸氢铵在烈日下暴晒:_____________。
(3)常温下,铝的表面生成一层致密的氧化膜:_____________。
(4)湿法炼铜:_____________。
(5)氨气(NH3)与氧化铜在加热条件下反应生成氮气、一种红色固态物质和一种无色液态物质:_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组在老师指导下进行课外实验,利用如图装置来探究单质在空气中燃烧后氧气浓度的变化情况。

(提出问题)足量红磷在密闭的四颈平底烧瓶内燃烧熄灭后,容器中是否有氧气剩余?
(猜想假设)猜想①:有氧气剩余;猜想②:无氧气剩余。
(实验验证)该小组同学按图组装好实验装置,利用高气压传感器能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;待装置氧气完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
(1)激光笔的作用是 ___________。
(2)红磷燃烧产物与瓶底热水反应生成磷酸(H3PO4)的化学方程式为_____。
(3)实验过程中,燃烧匙内的白磷先未燃着的原因是____________。
(实验结论)根据上述实验现象,得出结论如下:
(4)结论:猜想_________正确。
(拓展延伸)如图是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用氧气传感器测量容器内氧气浓度变化的曲线图。
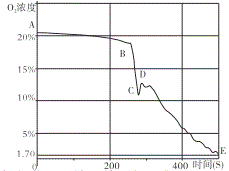
(5)在图中_____(填“A、B、C、D、E”)点时红磷燃烧熄灭;请你解释曲线AB段、DE段氧气浓度变化的主要原因:① _______。②________。
(6)小组同学通过查阅资料可知,验证空气中氧气体积分数较好的药品是铁丝绒,利用铁与氧气、水等的缓慢氧化,可以将空气中氧气浓度消耗至0.2%。将足量细铁丝绒置于试管底部,并倒扣在装有水的烧杯中(如图)较长时间后你将看到的现象是_______。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效多功能净水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为: 3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
(1)次氯酸钠(NaClO)的相对分子质量为__;其中氯元素的化合价为__;
(2)高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比为____(填最简比);
(3)现要制得830kg含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少__________?(列式计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com