
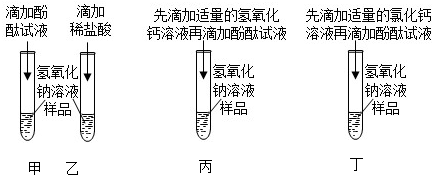
分析 【活动与探究1】
氢氧化钠溶液、碳酸钠溶液都是显碱性的溶液,都能够使酚酞试液变红色;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
【活动与探究2】
碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
【拓展应用】
氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠.
解答 解:【活动与探究1】
(1)如果氢氧化钠部分变质,生成的碳酸钠和氢氧化钠的溶液都能够使酚酞试液变红色,如果氢氧化钠全部变质,生成的碳酸钠溶液显碱性,也能够使酚酞试液变红色,因此甲同学在做实验时观察到酚酞溶液变红色,不能说明原试液没有变质.
故填:碳酸钠溶液显碱性,能使酚酞试液变红色.
【活动与探究2】
(3)丙同学观察到的实验现象是酚酞试液变红色,这是因为溶液中含有氢氧化钠,碳酸钠与氢氧化钙反应生成氢氧化钠,氢氧化钠溶液能使酚酞试液变红色.
故填:酚酞试液变红色.
(4)丁同学向试管滴加过量的氯化钙溶液的目的是使碳酸钠完全反应,防止对检验氢氧化钠产生影响;
丁试管中碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.
故填:使碳酸钠完全反应;Na2CO3+CaCl2═CaCO3↓+2NaCl.
(5)丙、丁两位同学的设计方案,合理的是丁,这是因为丙中无论氢氧化钠是否变质,酚酞试液都变红色,而丁中除去碳酸钠后,如果酚酞试液变红色,说明溶液中含有氢氧化钠,进一步说明氢氧化钠部分变质.
故填:丁.
【拓展应用】
要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的Ba(OH)2溶液,或Ca(OH)2溶液,这是因为氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,过滤除去沉淀后可得氢氧化钠溶液.
故填:AC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:推断题
 构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.
构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
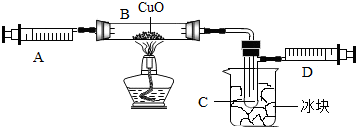
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 酸、碱是日常生活和实验中常用的两类物质.
酸、碱是日常生活和实验中常用的两类物质.| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 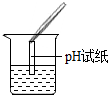 | 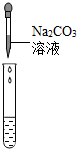 | 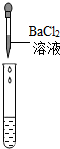 |
| 实验现象 | 试纸变色,对比标准比色卡:pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某专家称能“水变油”“点石成金” | |
| B. | 吸烟对青少年生长发育无害 | |
| C. | 生活中使用天然气做饭要通风透气 | |
| D. | 被毒鼠强药死的鸭水,煮熟后可以食用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com