
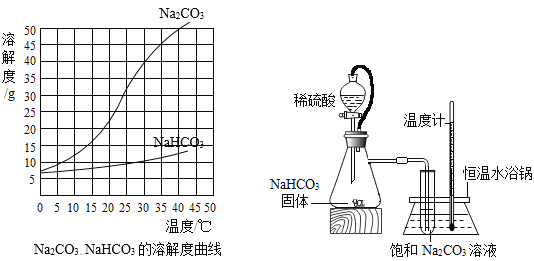
【题目】由于溶解度不同(如图所示),饱和碳酸钠溶液中通入CO 2会析出碳酸氢钠晶体而使溶液变浑浊。某化学课外小组同学发现不同条件下出现浑浊的时间不同。
(提出问题)影响碳酸氢钠晶体产生速率的因素有哪些?
(猜想与假设)碳酸氢钠晶体产生速率的影响因素有温度、试管内径、CO2流速、饱和碳酸钠溶液的体积。
(进行实验)实验装置如图所示。每次实验时均在试管里加入1mL饱和碳酸钠溶液并在试管后放置一张写有黑色字迹的白纸,从垂直于试管的方向观察白纸上字迹的清晰程度,记录时间,用于判断碳酸氢钠晶体的产生速率。部分实验记录如下表所示:
序号 | 温度(℃) | 试管内经(mm) | CO2流速 (个气泡/s) | 产生不同现象的时间(s) | ||
字迹变浅 | 字迹模糊 | 字迹消失 | ||||
① | 25 | 10 | 5~8 | 517" | 719" | 817" |
② | 32 | 10 | 5~8 | 350" | 409" | 428" |
③ | 40 | 10 | 5~8 | 348" | 406" | 418" |
④ | 25 | 14 | 5~8 | 636" | 738" | 828" |
⑤ | 25 | 25 | 5~8 | X | 943" | 1022" |
⑥ | 25 | 10 | 10~13 | 502" | 640" | 758" |
⑦ | 25 | 10 | 2~5 | 540" | 1045" | 1236" |
(解释与结论)
(1)由上述溶解度曲线图可知溶解度受温度影响相对更大的物质是_________________。
(2)锥形瓶中是利用碳酸氢钠与稀硫酸反应来制取二氧化碳。除生成二氧化碳外,还有水和硫酸钠生成,该反应的化学方程式为_____________________。
(3) 同学们若要研究饱和碳酸钠溶液的体积对碳酸氢钠晶体产生速率是否有影响,需要控制的变量有__________________。
(4)由实验①②③,可得出的结论是____________________。
(5)实验①④⑤研究的影响因素是___________________。
(6)通过对数据的观察和分析,小倩认为“二氧化碳流速越快,碳酸氢钠晶体产生速率越快”,得到该结论的依据是______________(填实验序号)。
(反思与评价)
(7)表中X的取值范围应该是_______________。
(8)该实验采用硫酸而不是盐酸来制备二氧化碳的原因是__________________。
(9)如图中使用橡皮管连接分液漏斗与锥形瓶的目的是__________________。
(10)如何除去碳酸钠中混有的少量碳酸氢钠?___________________。
【答案】碳酸钠(Na2CO3) 2NaHCO3+H2SO4=2CO2![]() +2H2O+Na2SO4 试管内径、CO2流速、饱和碳酸钠溶液的体积 温度越高,晶体产生速率越快 试管内径 ①⑥⑦ 502"~636" 防止盐酸挥发出的氯化氢气体对反应造成的影响 保证装置内部压强保持不变,以免对反应产生影响 降温结晶
+2H2O+Na2SO4 试管内径、CO2流速、饱和碳酸钠溶液的体积 温度越高,晶体产生速率越快 试管内径 ①⑥⑦ 502"~636" 防止盐酸挥发出的氯化氢气体对反应造成的影响 保证装置内部压强保持不变,以免对反应产生影响 降温结晶
【解析】
[解释与结论]
(1)由上述溶解度曲线图可知溶解度受温度影响相对更大的物质是:碳酸钠(Na2CO3)。
(2)锥形瓶中是利用碳酸氢钠与稀硫酸反应来制取二氧化碳。除生成二氧化碳外,还有水和硫酸钠生成,该反应的化学方程式为:2NaHCO3+H2SO4=2CO2![]() +2H2O+Na2SO4。
+2H2O+Na2SO4。
(3)由表中数据可知,温度是变量,故同学们若要研究饱和碳酸钠溶液的体积对碳酸氢钠晶体产生速率是否有影响,需要控制的变量有:试管内径、CO2流速、饱和碳酸钠溶液的体积。
(4)由表中数据可知,温度是变量,由实验①②③,可得出的结论是:温度越高,晶体产生速率越快。
(5)由表中数据可知,试管内径是变量,故实验①④⑤研究的影响因素是:试管内径。
(6)通过对数据的观察和分析,小倩认为“二氧化碳流速越快,碳酸氢钠晶体产生速率越快”,得到该结论的依据是:①⑥⑦。
[反思与评价]
(7)由温度为25℃可知,X的取值最小为502",由CO2流速为5~8个气泡/s可知,X的最大值为636",故表中X的取值范围应该是502"~636"。
(8)由于盐酸有挥发性,故该实验采用硫酸而不是盐酸来制备二氧化碳的原因是:防止盐酸挥发出的氯化氢气体对反应造成的影响。
(9)如图中使用橡皮管连接分液漏斗与锥形瓶的目的是:保证装置内部压强保持不变,以免对反应产生影响。
(10)由图可知,碳酸钠的溶解度受温度的影响变化较大,碳酸氢钠的溶解度受温度的影响变化较小,且都随温度的升高而增大,故除去碳酸钠中混有的少量碳酸氢钠应采取降温结晶的方法。


科目:初中化学 来源: 题型:
【题目】通过海水提取的粗盐中含有 MgCl2、CaCl2、MgSO4.以及泥沙等杂质.以下是一种 制备精盐的实验方案(用于沉淀的试剂均过量).
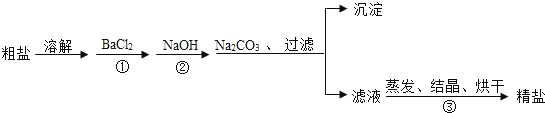
请回答下列问题:
(1)写出②中反应的化学方程式___________________________.
(2)加入 BaCl2、NaOH、Na2CO3 的顺序还可以改变吗?若能改变则写出改变的顺序,若不能改变,请说明理由_______________________________________.
(3)该实验方案还需完善,请写出具体的操作步骤___________________________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课外兴趣小组研究发现铜锈 [主要成分Cu2(OH)2CO3,学名:碱式碳酸铜]在加热后,除有二氧化碳和水生成外,在试管底部还有黑色粉末生成,他们对黑色粉末的成分进行了下列探究(不考虑杂质对实验的影响)。
(提出问题)黑色固体的成分是什么?
(提出猜想)①炭粉;②氧化铜;③______________。
(查阅资料)炭粉为黑色固体,不与稀酸反应,也不溶于稀酸。
(进行实验)(1)取少量黑色固体于坩埚中,用酒精灯加热,充分灼烧后,黑色固体无变化,猜想__不成立(填“①”、“②”或“③”,下同);
(2)用试管取少量黑色固体,滴加足量的_____________,振荡,充分反应后,观察到固体全部溶解,溶液显蓝色,猜想_____成立,发生反应的化学方程式是___________________________。
(拓展反思)孔雀石的主要成分与铜锈相同,结合上述实验探究结论,可以得出我国古代用孔雀石与木炭粉混合高温炼铜的反应原理是 __________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了除去粗盐中![]() 、
、![]() 、
、![]() 等可溶性杂质,需进行如下操作:①溶解;②依次加过量的
等可溶性杂质,需进行如下操作:①溶解;②依次加过量的![]() 、NaOH、
、NaOH、![]() 溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。
溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。
(1)加入过量![]() 溶液的作用是什么________?
溶液的作用是什么________?
(2)操作③得到的固体成分有哪些________?(写化学式)
(3)操作④加适量盐酸的作用是什么________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知铝在空气中会生成一层致密的氧化膜(Al2O3),实验小组将未打磨的铝片和稀盐酸放入密闭容器中,用传感器探究反应过程中温度和压强的变化,结果如图。下列说法不正确的是
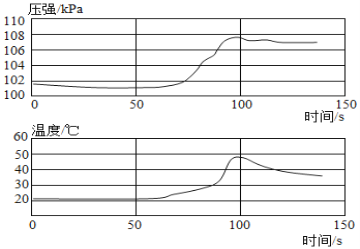
A.反应过程中有热量放出
B.0~50s,发生稀盐酸与 Al2O3 的反应
C.50 s 时,溶液中溶质为 AlCl3
D.100s~140s,压强减小是因为温度降低
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌碳酸氢铵化肥的标签如图所示。根据相关信息判断下列计算正确的是

A.碳酸氢铵中氮、氢、氧、碳四种元素的质量比14:4:48:12
B.碳酸氢铵中各元素的质量分数由大到小的顺序为O、C、H、N
C.该化肥中碳酸氢铵的纯度为79%
D.每袋该化肥中含氮量与30kg尿素[化学式为CO(NH2)2]含氮量相当
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去下列物质中的杂质,下列实验方案可行的是( )
A.木炭粉中混有![]() :在空气中灼烧
:在空气中灼烧
B.![]() 溶液中混有
溶液中混有![]() :通入过量的
:通入过量的![]() 过滤
过滤
C.![]() 溶液中混有盐酸:加入过量碳酸钙过滤
溶液中混有盐酸:加入过量碳酸钙过滤
D.![]() 中混有
中混有![]() 气体:依次通过足量的
气体:依次通过足量的![]() 溶液和浓
溶液和浓![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活息息相关。
(1)食物的成分主要有蛋白质、糖类、油脂、 、无机盐和水等六大类,通常称为营养素。下列各类食物中含糖类最丰富的是 (填字母)。




A.蔬菜 | B.米饭 | C.鸡蛋 | D.牛奶 |
(2)世界卫生组织推广使用中国铁锅炒菜,放点食醋,可以补充人体需要的微量元素 元素。
(3)餐具上的油污用加入洗洁精的水更容易洗掉,原因是洗洁精具有 作用。
(4)泡打粉是一种化学膨松剂,主要是通过碳酸氢钠与一些酸性成分发生化学反应产生 气体而起到发泡作用。
(5)磨牙器能有效帮助去除牙齿表面的牙垢,磨牙器磨头采用50%橡胶与50%的金刚砂(主要成分为碳化硅)特制而成。已知碳化硅中碳元素-4价,硅元素+4价,则碳化硅的化学式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属及其制品是现代生活中常见的材料,请回答下列问题:
(1)在空气中铝制品比铁制品更耐腐蚀的原因是:__________(化学方程式表示).
(2)某同学向氯化铜和氯化镁混合溶液中加入一定量的锌粉,待充分反应后过滤,向滤渣中滴加稀盐酸,有气体产生,则滤渣中一定含有______(填化学式),滤液中一定含有的溶质为______(填化学式)。
(3)用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是______t(计算结果保留到0.1)。
(4)一定质量含杂质的铁(杂质不溶于水,也不参与反应)与100g16%硫酸铜溶液恰好完全反应,过滤得到干燥的固体6.8g,则含杂质的铁中的铁的质量分数是________(计算结果保留至0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com