
| 实验事实 | 数据分析及结论 |
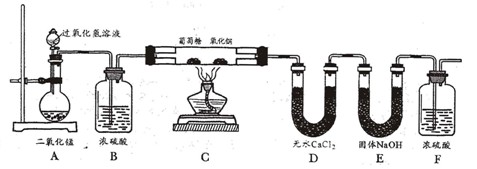
| 1.8g葡萄糖完全燃烧,得到2.64gCO2和1.08gH2O | 数据分析: 结论:葡萄糖含有C、H、O三种元素 |
 2H2O+O2↑;(2)干燥氧气;(3)检验葡萄糖与氧气是否反应生成一氧化碳
2H2O+O2↑;(2)干燥氧气;(3)检验葡萄糖与氧气是否反应生成一氧化碳 2H2O+O2↑.
2H2O+O2↑. 2H2O+O2↑;(2)吸收从A中溢出的水蒸气;
2H2O+O2↑;(2)吸收从A中溢出的水蒸气;

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案科目:初中化学 来源:不详 题型:实验题
 |


查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 猜想 | 实验操作 | 实验现象 | 结论(或化学方程式) |
| 猜想一:Na2CO3溶液显碱性 | 取少量Na2CO3溶液于试管中,滴入2-3滴酚酞试液,振荡 | | 溶液显碱性 |
| 猜想二:能与酸反应 | 取少量溶液于试管中,然后滴加稀盐酸 | 有大量气泡产生 | 化学方程式 |
| 猜想三:能与Ca(OH)2反应 | 向盛有少量Na2CO3溶液于试管中,滴加澄清石灰水 | 产生白色沉淀 | 化学方程式 |
| 猜想四:能与BaCl2反应 | | 产生白色沉淀 | Na2CO3+BaCl2=BaCO3↓+2NaCl 反应的基本类型为 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.常温下,1L水与1L酒精混合后的体积等于2L |
| B.室温下,1g镁与1g稀硫酸充分反应后所得的溶液质量为2g |
| C.室温下,1g硫粉在lg氧气中完全燃烧后生成2g二氧化硫 |
| D.20℃,lg氯化钠饱和溶液中加入1g氯化钠固体能得到2g氯化钠溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验 | A+D | A+B | B+C |
| 现象 | 产生气体 | 产生沉淀 | 产生沉淀 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 使用现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 | 现象一与现象二对比,说明 ① ▲ |
| 现象二:粗砂纸打磨的片刻内现象不明显。 | ||
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 | 现象三与现象一对比,说明 ② ▲ |
| 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象四与现象三对比,说明 ③ ▲ |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com