
 某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入固体化合物. | (加CaCO3),有气泡产生. | 盐酸过量 |
分析 探究一:根据酸的化学性质分析;
探究二:根据酸的定义及特征分析;
探究三:根据反应物的状态和反应条件选择发生装置,根据溶解性和密度选择收集方法,根据质量守恒定律书写方程式.
探究四:根据化学方程式的计算分析.
解答 解:探究一:因盐酸能与碳酸盐反应产生气泡的明显现象,可以用来检验盐酸,故答案为:Na2CO3(或CaCO3),有气泡产生.
探究二:酸的共同特征是电离出的阳离子都是氢离子,决定了酸具有相似的化学性质.故答案为:硫酸和盐酸溶液中都含有氢离子.
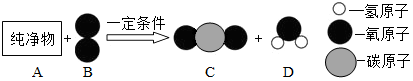
探究三:(1)制取二氧化氮的反应物状态和反应条件属于固液、常温型,故选B;有因为二氧化氮易与水反应,故不能用排水法收集,根据相对分子质量法比较:46>29可知二氧化氮的密度大于空气,故采用向上排空气法收集.
(2)因为NO和空气中的氧气发生化合反应生成了NO2,根据质量守恒定律,其反应的化学方程式为:2NO+O2═2N02.
探究四:根据反应前后的质量差可知,生成CaCO3沉淀的质量为1000g+10g-1009.8g=0.2g
设:反应物中Na2CO3的质量为x
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100
x 0.2g
$\frac{106}{100}$=$\frac{x}{0.2g}$
x=0.212g
碳酸钠溶液溶质质量分数为:0.212g/10g×100%=2.12%
答:所加碳酸钠溶液的溶质质量分数为2.12%.
答案为:故探究1:(加CaCO3),有气泡产生.
探究2:硫酸和盐酸溶液中都含有氢离子;
探究3:(1)向上排空气法; (2)2NO+O2═2N02;
探究4:2.12%.
点评 此题考查的内容较多,要逐一分析解答.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 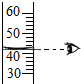 读出液体的体积 | B. | 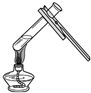 给液体加热 | C. | 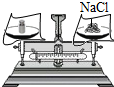 称取固体NaCl | D. | 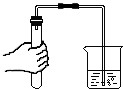 检查气密性 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 尿素、氨水、碳酸氢钠属于氮肥 | B. | 萘、铁、冰属于晶体 | ||
| C. | 干木头、金属、石墨属于导体 | D. | 酱油、黑芝麻糊、蒸馏水属于混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
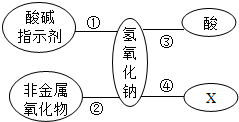
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸中肯定含有氢元素 | |
| B. | 碱一定由金属阳离子与氢氧根离子结合形成 | |
| C. | 分子的质量一定大于原子的质量 | |
| D. | 空气中含量最多的元素是氮 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com