
【题目】为减少污染并变废为宝,一化学兴趣小组在实验室探究工业废水的综合利用,设计了以下流程图并完成了回收铜和硫酸亚铁晶体的实验。
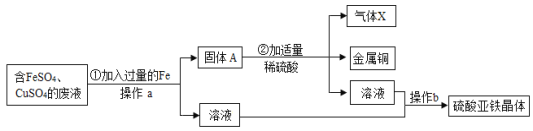
(1)A的成分为_____。
(2)写出②所发生反应的化学方程式为_____。
(3)操作a和操作b中都要用到一种玻璃仪器。该仪器在操作b中的作用是什么?____
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4nH2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计利用废弃铁锈合成草酸亚铁晶体并检验其热分解的产物及探究它的组成。
(一)制备草酸亚铁晶体(FeC2O4·nH2O)
资料1:FeSO4的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | 59.8 |
资料2:草酸亚铁难溶于水,在酸性条件下稳定存在。
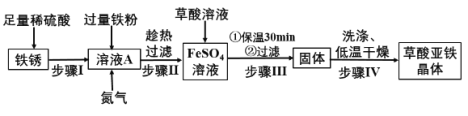
(制备流程)
(1)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和______,其作用是___
(2)步骤Ⅱ中趁热过滤的目的是______。
(3)草酸(H2C2O4)溶液加入FeSO4溶液中发生了复分解反应,请写出该反应的化学方程式为______。
(4)步骤Ⅲ中保温反应30min的目的是______。
(二)检验草酸亚铁晶体(FeC2O4·nH2O)热分解的产物及探究n的值
(实验装置)
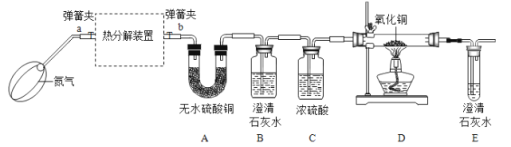
资料3:FeC2O4·nH2O加热至300℃完全失去结晶水;继续加热至400℃,剩余固体受热分解产生铁的氧化物、CO2和CO。
(实验分析)
(5)打开弹簧夹a、 b,先鼓入一段时间的氮气,然后再关闭a,加热分解装置的原因是______。
(6)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有______(填试剂名称)的洗气瓶。
(7)装置D硬质玻璃管中出现的现象是______。
(8)取7.20gFeC2O4·nH2O,按上述实验步骤进行实验,测得热分解装置中固体质量随温度变化曲线如图所示:
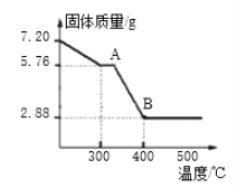
①FeC2O4·nH2O中n的值为______。(写出计算过程)
②若草酸亚铁晶体中混有杂质(杂质不参加反应),会导致测得的n的值______(选填“偏大”、“偏小”、“不变”)。/p>
③写出曲线中A至B发生反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常见的锅有陶瓷锅、铁锅、铜锅等。
(1)与陶瓷锅相比,用铜锅加热更快,利用的金属性质是_______。
(2)铁锅清洗后如未擦干,容易产生红色铁锈,该过程中发生了_____(填“物理”或“化学”)变化。
(3)铜锅加热后,锅底容易产生一层黑色的氧化铜,反应的化学方程式为________。
(4)用钢丝球清洗铜锅时,用力过大容易在铜锅上产生划痕。说明钢的硬度比铜___(填“大”或“小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学在实验室研究铝与氯化铜溶液的反应。
实验操作 | 实验现象 |
| ①红色物质附着于铝片表面 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色沉淀和白色沉淀 |
(1)打磨铝片的目的是__________。
(2)现象①和现象③中的红色物质均为Cu,生成该物质的化学方程式为______________。
(3)经检验,现象②中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性,经pH计检验,pH_____7,证实了甲的猜想。
(4)探究白色沉淀的化学成分。
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
CuCl中铜元素的化合价是________。
【查阅资料】
①CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl-。
②Cu(NH3)2+在空气中易被氧化变为蓝色;Cl-可与硝酸银溶液反应,产生白色沉淀。
【进行实验】
①取烧杯底部的白色沉淀,充分洗涤;
②向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
③取其中一份无色溶液……
④将另一份无色溶液放置于空气中……
以上步骤③的实验方案是________;步骤④的现象是________。
【得出结论】通过实验可以确定,该白色固体是CuCl。
【反思与评价】Al和CuCl2溶液反应为什么会出现CuCl呢?
丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl。
丙同学为了验证猜想,取Cu粉与15% CuCl2溶液混合,无白色沉淀产生。
(5)丙通过分析Al与CuCl2溶液反应的实验现象,改进了实验,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是________。
(6)丁同学认为丙同学的实验还不够严谨,还应考虑________对Cu与CuCl2溶液反应的影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定温度下,向烧杯中加入一定质量的水,仅有部分晶体溶解.所得溶液与原溶液相比,说法正确的是( )
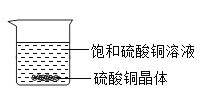
A.溶剂的质量增加,溶液颜色变浅 B.溶质溶解度不变,溶液颜色变深
C.溶质的质量增加,溶液颜色变深 D.溶质溶解度不变,溶液颜色不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入a克Zn粉,充分反应后过滤,将洗涤、干燥后称量,得到的固体质量为a克。据此,下列说法正确的是( )
A. 滤液中的物质一定至少有两种
B. 取反应后的滤液滴加稀盐酸,可能有白色沉淀产生
C. 取滤渣滴加稀盐酸,一定有气泡产生
D. 取反应后的滤液观察,滤液一定呈无色
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】了解物质的组成和结构,有助于认识物质的性质和变化。
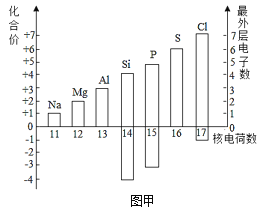
(1)图甲表示核电荷数为11~17的元素最高和最低化合价和原子的最外层电子数。
①若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为_____。硫元素既可显正价,又可显负价,硫元素与钠元素形成的化合物由_____(填“分子”、“原子”或“离子”)构成,其化学式为_____。
②铝原子失去最外层电子所形成的离子符号为_____。
③写出图中元素的化合价与最外层电子数有关的一条规律_____。
(2)将NaOH、KCl、MgCl2三种溶液按一定比例混合,微观变化情况如图乙。
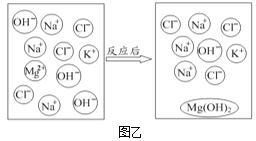
①图中OH-的名称是_____。
②该反应的本质是_____结合生成沉淀。
③写出与上述反应本质相同的另一反应的化学方程式:_____(反应物之一为MgCl2)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验中经常用到一定溶质质量分数的溶液,请回答:
(1)小明在实验室配置质量分数为12%的碳酸钠溶液。
①计算:配制100g该碳酸钠溶液需要碳酸钠固体的质量为_________g。
②称量:用托盘天平称量所需的碳酸钠,放入烧杯中,小明在称取时发现托盘天平的指针偏向右盘,正确的做法是_________(填序号)。
a 增加砝码 b减少砝码 c添加固体 d减少固体 e调节平衡螺母向右旋
③量取:用量筒量取水(水的密度是1g/mL)的体积时仰视读取液体体积,读数比实际量取液体体积________________(填偏大、偏小或不变)
④溶解:用玻璃棒搅拌,使碳酸钠溶解。
⑤将配制好的溶液装入试剂瓶,盖好瓶塞,贴上标签,请帮小明完成如图标签内容。_______

(2)小刚要把(1)配得的溶液稀释为6%,需要加水的质量为___________g。
(3)稀硫酸常作为工业上的除锈剂,现配制4.9%的稀硫酸2000g,需要98%的浓硫酸(密度为1.84g/mL)___________mL(计算结果精确至0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com