
| 物质的质量 | |
| 反应前:烧杯+盐酸 | 22g |
| 10片钙片 | 8g |
| 反应后:烧杯+剩余物 | 27.8g |
分析 (1)根据实验的得到二氧化碳的质量和质量守恒定律,然后根据碳酸钙与盐酸反应的化学方程式即可计算出参与反应的碳酸钙的质量(即10片钙片的质量),进而计算出每片此钙片含碳酸钙的质量;
(2)再根据碳酸钙(CaCO3)中钙元素的质量分数求出钙元素的质量,与标签中的含钙量比较,即可解答.
解答 解:根据质量守恒定律,减少的质量为二氧化碳的质量,由表中信息可知:二氧化碳的质量=22g+8g-27.6g=2.2g
设含碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
(1)每片此钙片含碳酸钙的质量=$\frac{5g}{8g}$×100%=0.4g
(2)每片此钙片的含钙量=0.4g×$\frac{40}{100}$×100%=0.16g,每片钙片中钙元素的质量分数=$\frac{0.16g}{0.4g}×$100%=40%
答案:
(1)每片此钙片含碳酸钙的质量0.4g
(2)每片此钙片的含钙元素的质量分数40%.
点评 将质量分数的计算与生活实际相联系;计算时要理清各个量之间的关系,再结合题意进行分析解答.


科目:初中化学 来源: 题型:解答题
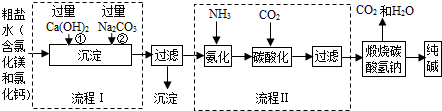
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
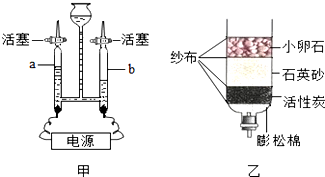
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验一 | 实验二 | 实验三 | |
实验 方案 | 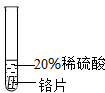 | 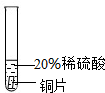 | 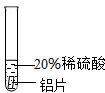 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快[ |
| 三种金属在金属活动性顺序中的相对位置关系是Al、Cr、Cu | |||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如下图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如下图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有 CaO和氢氧化钙 |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清的石灰水变浑浊 | 固体中一定含有CaCO3 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com