
【题目】氢气是一种理想的新能源,具有广阔的开发前景。铁酸锌(ZnFe2O4)可用于循环分解水制氢气,其反应可表示为:
![]() ;
;![]()
(1) ZnFe2O4中Fe的化合价为___________。
(2)该循环制氢中不断消耗的物质是___________。
(3)氢气作为新能源,有不污染环境、热值大、原料来源丰富等优点,但目前并没有被广泛应用,你认为主要原因是_______。
科目:初中化学 来源: 题型:
【题目】几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质、,每个箭号各表示一个化学反应,部分反应物、生成物及反应条件略去)。已知五种物质均由C、H、O中部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和D可以发生化合反应。
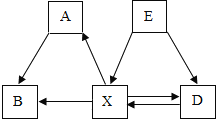
(1)A是_____,E是_____,X是_____。
(2)实现A→B转化的化学反应类型_____(填“一定”或“不一定”)属于化合反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体(均不 含结晶水)的溶解度曲线。据图回答:甲溶液中含有少量的乙时,可通过______________的方法提纯甲;取t2°C时甲、乙、丙三种饱和溶液各100g,均降温到t1°C,此时三种溶液中溶剂的质量大小关系为______________。t1°C时将65 g丙的饱和溶液加入_____________g水,得到溶质的质量分数为10%的丙溶液。
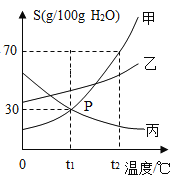
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,小明同学对含有泥沙的粗盐进行提纯并计算产率,请回答下列问题。

(1)粗盐提纯的实验步骤顺序是_____(填序号)。
(2)上述实验的操作中,有三处用到了同一种仪器:_____(填仪器名称),它在步骤⑤起到的作用是_____。
(3)蒸发加热到何时停止加热_____。
(4)计算产率时发现产率偏高了,你认为的可能原因是_____(写一个原因即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:
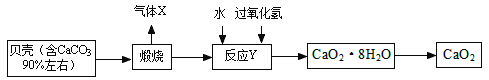
(1)气体X是 ;将过氧化钙晶体与溶液分离的方法是 。
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中,反应产物是CaO2·8H2O,,请写出化学方程式 该反应的基本反应类型是 。获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电字元件使用了黄铜。为测定某黄铜(假设合金中仅含铜,锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量(g) | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为____________g。
(2)该黄铜中铜的质量分数为多少?(写出计算过程)____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在人类生活和生产中应用十分广泛,下列是关于金属的三组实验,请回答下列问题。
实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
|
|
|
(1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为该实验设计不够合理,理由是___________________。
(2)写出实验Ⅱ中C试管内反应的化学方程式__________________。
(3)实验Ⅲ为实验室模拟炼铁的装置图。
①加热Fe2O3之前要先通一会 CO,目的是__________________。
②装置末加酒精灯装置的目的是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学在实验室研究铝与氯化铜溶液的反应。
实验操作 | 实验现象 |
| ①红色物质附着于铝片表面 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色沉淀和白色沉淀 |
(1)打磨铝片的目的是__________。
(2)现象①和现象③中的红色物质均为Cu,生成该物质的化学方程式为______________。
(3)经检验,现象②中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性,经pH计检验,pH_____7,证实了甲的猜想。
(4)探究白色沉淀的化学成分。
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
CuCl中铜元素的化合价是________。
【查阅资料】
①CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl-。
②Cu(NH3)2+在空气中易被氧化变为蓝色;Cl-可与硝酸银溶液反应,产生白色沉淀。
【进行实验】
①取烧杯底部的白色沉淀,充分洗涤;
②向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
③取其中一份无色溶液……
④将另一份无色溶液放置于空气中……
以上步骤③的实验方案是________;步骤④的现象是________。
【得出结论】通过实验可以确定,该白色固体是CuCl。
【反思与评价】Al和CuCl2溶液反应为什么会出现CuCl呢?
丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl。
丙同学为了验证猜想,取Cu粉与15% CuCl2溶液混合,无白色沉淀产生。
(5)丙通过分析Al与CuCl2溶液反应的实验现象,改进了实验,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是________。
(6)丁同学认为丙同学的实验还不够严谨,还应考虑________对Cu与CuCl2溶液反应的影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生产、生活密切相关。请用化学方程式表示下列有关反应的原理。
(1)铝抗腐蚀性强的原因_____________。
(2)实验室制取氢气的原理_____________。
(3)乙醇(C2H5OH)被用作酒精灯、火锅等的原料_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com