
【题目】根据下列反应事实写出相应的化学方程式。
(1)酒精(C2H5OH)在足量氧气中完全燃烧_______。
(2)稀盐酸与铁锈(主要成分是氧化铁)反应_________。
(3)炼铁高炉内焦炭与二氧化碳反应____。
(4)铜丝与硝酸银溶液反应____。
(5)实验室用双氧水和二氧化锰制取氧气_________。
【答案】C2H5OH+3O2![]() 2CO2+3H2O Fe2O3+6HCl=2FeCl3+3H2O C+CO2
2CO2+3H2O Fe2O3+6HCl=2FeCl3+3H2O C+CO2 ![]() 2CO Cu+2AgNO3=Cu(NO3)2+2Ag 2H2O2
2CO Cu+2AgNO3=Cu(NO3)2+2Ag 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
(1)酒精与氧气在点燃的条件下反应生成二氧化碳和水,故反应的化学反应式写为:C2H5OH+3O2![]() 2CO2+3H2O。
2CO2+3H2O。
(2)稀盐酸与氧化铁反应生成氯化铁和水,故反应的化学方程式写为:Fe2O3+6HCl=2FeCl3+3H2O。
(3)碳与二氧化碳在高温的条件下反应生成一氧化碳,故反应的化学方程式写为:C+CO2![]() 2CO。
2CO。
(4)铜与硝酸银反应生成硝酸铜和银,故反应的化学方程式写为:Cu+2AgNO3=Cu(NO3)2+2Ag。
(5)过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,故反应的化学方程式写为:2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。


科目:初中化学 来源: 题型:
【题目】常温下没有氧气存在时,铁与水几乎不反应,高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计实验探究铁粉与水蒸气反应后的产物。
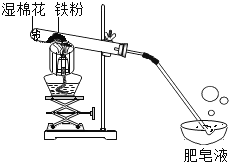
(1)试管尾部放一团湿棉花的目的是________
(2)酒精灯火焰上加一个网罩的目的是________
(3)加热一段时间后,同学们开始探究生成的气体以及试管中剩余固体是什么?
①将燃着的木条靠近肥皂泡有爆鸣声,且看到有肥皂泡飘到空中,说明生成的气体是______,实验刚开始产生的少许肥皂泡_______(填“会”或“不会”)往上飘,原因可能是________
②探究加热一段时间后成分是什么?
(查阅资料)
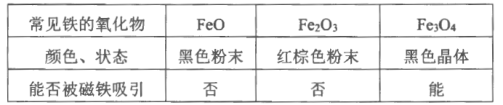
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe3O4;猜想二:剩余固体是________。
(实验探究)请设计一个实验验证猜想二成立,并完成下面的实验报告
实验操作 | 实验现象 | 结论 |
取少量反应后的固体与试管中加入_______ | ______ | 猜想二成立 |
(实验结论)铁和水蒸气反应的化学方程式为_________
(反思与交流)该黑色固体不可能是Fe2O3,理由是_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某样品硝酸钾中含有一定质量的氯化钾.为了测定其中硝酸钾的质量分数做如下实验:取10g该样品加入58.87g水使其完全溶解,向溶液中逐滴加入硝酸银溶液至恰好完全反应,共用去34g硝酸银溶液;过滤、烘干称得沉淀为2.87g.根据实验计算:
(1)样品中硝酸钾的质量分数为多少_____?
(2)反应后所得溶液中溶质的质最分数为多少_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如图1所示(已知氯化钙溶液呈中性;石灰石中的杂质不与酸反应,也不溶于水)。
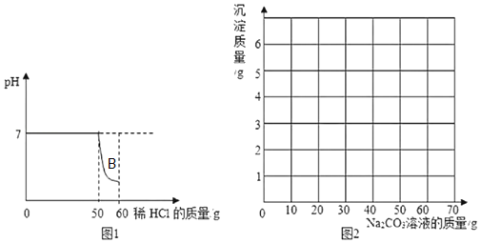
①图1中B点溶液中的溶质有_____(写化学式)。
②该小组同学能收集到的二氧化碳的质量是_____g,同时可得到CaCl2的质量为_____g。
③该小组同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | 0 | 1 | n | 3 | 4 | 5 | m |
则m=_____。加入10gNa2CO3溶液时发生反应的化学方程式是_____。
④请在图2中画出向滤液中加入Na2CO3溶液时产生的沉淀的质量随加入Na2CO3溶液的变化曲线_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下列20℃时的实验和数据回答以下问题。
已知:20℃时,KCl和KNO3的溶解度分别为34g和31.6g;
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | KCl | KCl | KCl | KNO3 | KNO3 | |
固体的质量/g | 20 | 35 | 40 | 25 | 40 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
【1】①~⑤所得溶液属于不饱和溶液的是
A. ①②B. ②③C. ①④D. ③⑤
【2】下列关于①~⑤所得溶液的说法正确的是
A. 溶质质量:③ = ⑤
B. 溶液质量:③﹥②
C. 溶质质量分数:①<④
D. ⑤中溶质与溶剂的质量比为2:5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】进行如下实验,研究物质的性质。
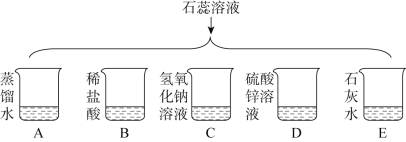
(1)D中溶液变为红色,说明硫酸锌溶液显_____(填“酸性”或“碱性”)。
(2)溶液变为蓝色的有_____(填字母序号,下同)。
(3)作为空白对照实验的是_____。
(4)再向B烧杯中加入适量石灰水,溶液变为紫色,用化学方程式解释其原因_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。课外小组同学利用H2与金属钙反应制取CaH2(见图)
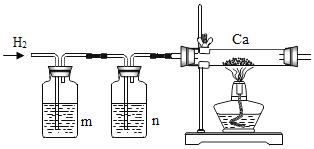
(1)反应所需H2可利用锌粒与稀盐酸反应制取,方程式为_____,该反应属于基本反应类型中的_____反应。
(2)洗气瓶中m、n应依次选择下列试剂的_____、_____(填序号)
A NaHCO3溶液 B NaOH溶液 C 浓硫酸
(3)为防止钙被氧化,在加热钙之前必须进行的操作是_____。
(4)CaH2与水反应的化学方程式为_____。氢气密度比空气_____(填“大”或“小”),试从微观探析角度解释其原因_____(已知同温同压下相同体积的任何气体都含有相同数目的分子)
(5)为防止空气中的二氧化碳、水蒸气与玻璃管中Ca或CaH2反应,在导管末端还应该连接一干燥管,所装试剂为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某固体粉末由Mg、MgO、Mg (OH)2中的一种或几种组成。某化学小组为了探究该固体粉末的成分,设计如图所示的装置(固定装置省略)。
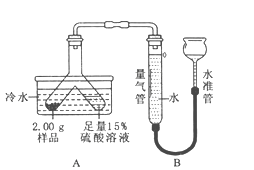
【信息资料】本实验条件下,氢气密度为0.09g/L。
【实验过程】
步骤Ⅰ:检查装置气密性,装入药品并连接仪器。
步骤Ⅱ:倾斜Y形管,使样品充分反应,测的生成气体的探究为55.6mL。
步骤Ⅲ:拆下装置,往Y形管内残余液中加入氢氧化钠溶液,至不再生成沉淀。经过滤、洗涤和干燥后,称得沉淀质量为2.90g。
【回答问题】
(1)该套装置气密性的检验方法是 。
(2)①使样品与硫酸充分反应的正确操作是 (填标号)。
A.硫酸溶液转移到样品中 B.样品转移到硫酸溶液中
②判断样品完全反应的现象是 。
(3)根据实验结果分析:
①通过步骤Ⅱ推断,样品中一定含有的物质是 。
通过步骤Ⅲ计算,样品中镁元素的总质量为 。
②结论:该样品中的成分是 。
【反思】
(4)该化学小组同学经过讨论得出以下结论,正确的是 (填标号)。
A.利用该实验方案,能计算出样品中各物质的质量
B.实验前可通过样品的质量估算硫酸溶液的质量,确保样品完全反应
C.仅称量步骤Ⅱ中Y形管内药品减轻的质量,即能计算出样品中各物质的质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com