
【题目】依据下列20℃时的实验和数据回答以下问题。
已知:20℃时,KCl和KNO3的溶解度分别为34g和31.6g;
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | KCl | KCl | KCl | KNO3 | KNO3 | |
固体的质量/g | 20 | 35 | 40 | 25 | 40 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
【1】①~⑤所得溶液属于不饱和溶液的是
A. ①②B. ②③C. ①④D. ③⑤
【2】下列关于①~⑤所得溶液的说法正确的是
A. 溶质质量:③ = ⑤
B. 溶液质量:③﹥②
C. 溶质质量分数:①<④
D. ⑤中溶质与溶剂的质量比为2:5
【答案】
【1】C
【2】C
【解析】
【1】根据KCl和KNO3的溶解度可知,20℃时,100g水中最多溶解的氯化钾质量为34g,硝酸钾的质量为31.6g;由题表可知溶剂量都为100g,①中溶质氯化钾质量小于34g,属于不饱和溶液;②③中溶质氯化钾质量均大于34 g,属于饱和溶液;④中溶质硝酸钾质量小于31.6g,属于不饱和溶液;⑤中溶质硝酸钾质量大于31.6g,属于饱和溶液;故选C。
【2】A、③为20℃时氯化钾的饱和溶液,溶质质量为34g,⑤为20℃时硝酸钾的饱和溶液,溶质质量为31.6g,二者不相等,故不符合题意;
B、②③均为20℃时氯化钾的饱和溶液,溶液质量均为134g,溶液质量③=②,故不符合题意;
C、由上分析可知,①中溶质质量分数为![]() ≈16.7%,④中溶质质量分数为
≈16.7%,④中溶质质量分数为![]() =20%,即溶质质量分数①<④,故符合题意;
=20%,即溶质质量分数①<④,故符合题意;
D、⑤是20℃时硝酸钾的饱和溶液,溶质与溶剂的质量比为31.6∶100≠2:5,故不符合题意。
饱和溶液是指在一定温度下,一定量的溶剂里不能继续溶解某种溶质的溶液,叫做该种溶质的饱和溶液,还能继续溶解某种溶质的溶液,叫做该种溶质的不饱和溶液;二者的区别是能否继续溶解某种溶质。所以证明某一溶液是饱和溶液还是不饱和溶液,只要向该溶液中加入该种溶质,如果能溶则为不饱和溶液,反之为饱和溶液。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
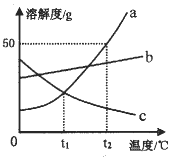
(1)温度为_______时,a、c两种物质的溶解度相同。
(2)将t2℃时a物质的饱和溶液30.0g稀释成10%的溶液,需加水___g;完成该实验需要的仪器是_____________。
(3)下列说法正确的是______。
A 将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是a>b>c
C 配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高
D 若b物质中混有少量a物质,提纯b物质应该采用的方法是蒸发结晶
E 将t2℃时a、b、c三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序是b>a>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自来水厂常用氯气杀菌消毒,用明矾、氯化铁等净化水。以硫铁矿(主要成分是FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的流程如下图所示:
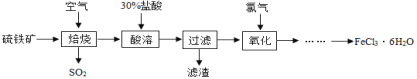
(1)“焙烧”前将硫铁矿进行粉碎,其目的是___。
(2)已知“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,写出该反应的化学方程式__。
(3)大量排放出SO2能形成酸雨,危害环境。常用下列方法除去:
方法1:将含SO2的废气通入氨水中,以减少空气污染,反应的化学方程式为:2SO2+4NH3H2O+O2=2__+2H2O。某兴趣小组测定了不同溶质质量分数的氨水在不同温度下吸收SO2气体的情况,获得如下图象,从实验数据可知,吸收SO2最佳的生产条件是__、__;

方法2:将含有二氧化硫的废气通入石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫。写出该反应的化学方程式____。
(4)流程中用30%盐酸“酸溶”焙烧后的残渣,写出化学方程式____;若在实验室欲用质量分数为37%(密度为1.18 g/ml)的盐酸配制30%的100g盐酸,则需要加水___g(保留1位小数),需要的玻璃仪器有烧杯、___、___胶头滴管等。
(5)“氧化”后从FeCl3溶液中获得FeCl3·6H2O晶体的操作方法是:在HCl气流中蒸发浓缩、____、过滤、洗涤、干燥。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”。其标签如图所示,某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究。
品名:504双吸剂
成分:铁粉、生石灰等
(提出问题):久置固体的成分是什么?
(查阅资料):铁与氯化铁溶液在常温下发生反应:Fe+2FeCl3=3FeCl2打开固体包装观察:部分固体呈黑色,部分固体呈白色,另有少量红棕色的块状固体。
(作出猜想):久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。其中可能含有Fe2O3的依据是_____________。
(实验探究):甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌 | 固体溶解,试管外壁发烫 | 固体中一定含有______ |
(2)过滤,在滤液中滴加无色酚酞溶液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
(3)取滤渣放入试管中,滴加足量的________ | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有______,一定不含氧化铁 |
(实验质疑)乙同学认为甲同学在实验中得出“一定不含氧化铁”的结论是错误的,理由是______________。你认为甲同学哪一步实验操作得出的结论也不合理:__________,理由是___________(用化学方程式表示。)
(继续探究)乙同学另取久置的固体进行实验探究:
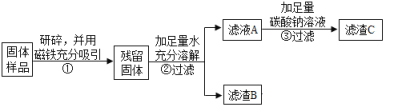
乙同学对滤渣B进行探究:
实验操作 | 实验现象 | 实验结论 |
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、______有气泡冒出、______ | 固体中一定含有CaCO3和Fe2O3。写出Fe2O3和稀盐酸反应的化学方程式_______ |
(计算得出结论):如上述实验流程,乙同学现取5g久置固体研碎,用磁铁吸引,得残留固体3g,加足量水充分溶解过滤,得滤渣B的质量为1.8g。在滤液A中加足量碳酸钠溶液后过滤得滤渣C的质量为2g,通过计算后得出残留固体的成分为:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列反应事实写出相应的化学方程式。
(1)酒精(C2H5OH)在足量氧气中完全燃烧_______。
(2)稀盐酸与铁锈(主要成分是氧化铁)反应_________。
(3)炼铁高炉内焦炭与二氧化碳反应____。
(4)铜丝与硝酸银溶液反应____。
(5)实验室用双氧水和二氧化锰制取氧气_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用如图所示实验,验证铁和铜的金属活动性顺序。
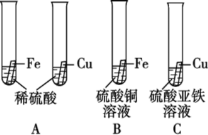
(1)A中可观察到的现象是____________。
(2)B中反应的化学方程式为___________。
(3)请描述C中的实验现象,并进行分析,得出结论。_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Na2SO3的溶解度曲线如图所示,下列说法错误的是( )
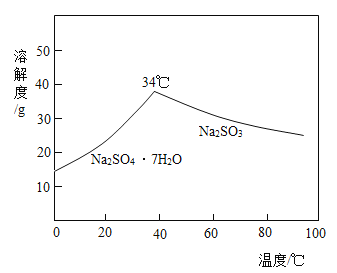
A. 34℃时Na2SO3的溶解度最大
B. 低于34℃时析出Na2SO37H2O固体
C. 采用升温结晶的方法可以得到Na2SO3固体
D. 采用降温结晶的方法可以得到Na2SO3固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)水是生命的源泉,也是不可缺少的资源:
![]() 自然界的水常常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,人们把这种现象称之为水质富营养化
自然界的水常常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,人们把这种现象称之为水质富营养化![]() 这里的“氮和磷”是指______。
这里的“氮和磷”是指______。![]() 填字母
填字母![]()
A 元素B 原子C 离子D 分子
![]() 生活中,既能降低水的硬度,又能杀菌消毒的方法是______。
生活中,既能降低水的硬度,又能杀菌消毒的方法是______。
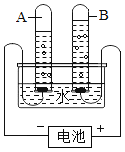
![]() 电解水的装置如图所示,管A、管B中的气体质量比是______。
电解水的装置如图所示,管A、管B中的气体质量比是______。
(2)除去下列物质中的杂质,所用试剂和操作方法正确的是_____(多选)。
选项 | 实验目的 | 实验方案 |
A | 除去NaCl溶液中的 | 加适量稀硫酸 |
B | 除去 | 将混合气体通入饱和NaHCO3溶液 |
C | 除去CaO中的 | 加水溶解,过滤 |
D | 除去 | 加适量的 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如下图所示。图中a、b、c、d分别表示相应物质的质量分数。下列数据正确的是

A. a=56% B. b=6% C. c=17% D. d=8%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com