
【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”。其标签如图所示,某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究。
品名:504双吸剂
成分:铁粉、生石灰等
(提出问题):久置固体的成分是什么?
(查阅资料):铁与氯化铁溶液在常温下发生反应:Fe+2FeCl3=3FeCl2打开固体包装观察:部分固体呈黑色,部分固体呈白色,另有少量红棕色的块状固体。
(作出猜想):久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。其中可能含有Fe2O3的依据是_____________。
(实验探究):甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌 | 固体溶解,试管外壁发烫 | 固体中一定含有______ |
(2)过滤,在滤液中滴加无色酚酞溶液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
(3)取滤渣放入试管中,滴加足量的________ | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有______,一定不含氧化铁 |
(实验质疑)乙同学认为甲同学在实验中得出“一定不含氧化铁”的结论是错误的,理由是______________。你认为甲同学哪一步实验操作得出的结论也不合理:__________,理由是___________(用化学方程式表示。)
(继续探究)乙同学另取久置的固体进行实验探究:
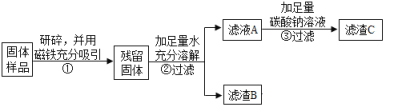
乙同学对滤渣B进行探究:
实验操作 | 实验现象 | 实验结论 |
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、______有气泡冒出、______ | 固体中一定含有CaCO3和Fe2O3。写出Fe2O3和稀盐酸反应的化学方程式_______ |
(计算得出结论):如上述实验流程,乙同学现取5g久置固体研碎,用磁铁吸引,得残留固体3g,加足量水充分溶解过滤,得滤渣B的质量为1.8g。在滤液A中加足量碳酸钠溶液后过滤得滤渣C的质量为2g,通过计算后得出残留固体的成分为:__________。
【答案】固体中少量红棕色的块状固体 CaO 盐酸 CaCO3 铁与氯化铁溶液在常温下反应生成氯化亚铁 实验操作(2) CaO+H2O═Ca(OH)2 澄清石灰水变浑浊 溶液由无色变成黄色 Fe2O3+6HCl═2FeCl3+3H2O Fe2O3、CaO、Ca(OH)2和CaCO3
【解析】
作出猜想:
其中可能含有Fe2O3的依据是固体中少量红棕色的块状固体;
实验探究:
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌,固体溶解,试管外壁发烫,是因为氧化钙和水反应放热,因此固体中含有氧化钙;
(3)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳。取滤渣放入试管中,滴加足量的稀盐酸,固体逐渐消失,有大量无色气体产生,得到浅绿色溶液,固体中一定含有碳酸钙,一定不存在氧化铁。实验过程如下所示:
实验操作 | 实验现象 | 实验结论 |
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌 | 固体溶解,试管外壁发烫 | 固体中一定含有CaO |
(2)过滤,在滤液中滴加无色酚酞溶液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
(3)取滤渣放入试管中,滴加足量的盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有CaCO3,一定不含氧化铁 |
实验质疑:
根据“铁与氯化铁溶液在常温下发生反应:Fe+2FeCl3=3FeCl2”可知,乙同学认为甲同学在实验中得出“一定不含氧化铁”的结论是错误的,理由是铁与氯化铁溶液在常温下反应生成氯化亚铁;
甲同学实验操作(2)得出的结论也不合理,理由是氧化钙能和水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;
继续探究:
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水,固体逐渐消失、澄清石灰水变浑浊、有气泡冒出,是因为稀盐酸和碳酸钙反应生成了二氧化碳,溶液由无色变成黄色,是因为氧化铁和稀盐酸反应生成了氯化铁,实验过程如下所示:
实验操作 | 实验现象 | 实验结论 |
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、澄清石灰水变浑浊,有气泡冒出、溶液由无色变成黄色 | 固体中一定含有CaCO3和Fe2O3。Fe2O3和稀盐酸反应的化学方程式:Fe2O3+6HCl═2FeCl3+3H2O |
计算得出结论:
(1)设滤液A中含氢氧化钙的质量为x。
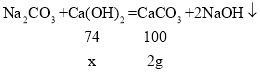
![]() x=1.48g;
x=1.48g;
现取5g久置固体研碎,用磁铁吸引,得残留固体3g,加足量水充分溶解过滤,得滤渣B的质量为1.8g,则氧化钙、或氧化钙和氢氧化钙的质量=3g-1.8g=1.2g;如果1.2g物质全部是氧化钙;
设:1.2g氧化钙和水反应生成氢氧化钙质量为y。

![]() y=1.6g;
y=1.6g;
滤液A中含氢氧化钙的质量为1.48g,因此1.2g物质是氧化钙和氢氧化钙的混合物,通过滤渣B的探究可知,固体中一定含有CaCO3和Fe2O3。所以残留固体成分是Fe2O3、CaO、Ca(OH)2和CaCO3。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:
【题目】分别向50gFeSO4和CuSO4溶液中,加入一定质量Mg粉恰好完全反应。随Mg粉消耗,Mg粉与帶液中FeSO4、CuSO4的质量变化见图。请读取图象信息并结合金属活动性服序分析,下面说法不合理的是
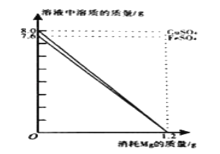
A. 反应前,溶液中溶质质量分数:FeSO4<CuSO4
B. 反应后,两容液底部分别析出的金属是Fe和Cu
C. 反应后,两溶液底部析出金属的质量:Fe<Cu
D. 反应后,若FeSO4和CuSO4对应新溶液的溶质质星分数分别为A、B,则A>B
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】微观粒子模型化是研究化学变化的重要方法。
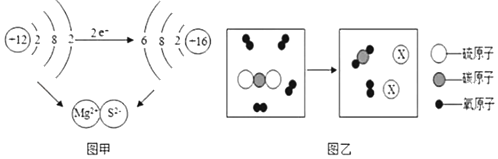
(1)图甲是镁与硫反应生成硫化镁的示意图,该图说明在化学反应过程中一定发生变化的是_____(填字母)。
A 原子核 b 原子的最外层电子数 c 原子的电子层数
(2)某反应的微观示意图如图乙所示
①请你画出微粒X的图示_____。
②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是_____。
③图乙的反应可表示为CS2+3O2![]() 2SO2+CO2,其中化合价发生变化的元素是硫和氧两种元素,请分别表示出它们的化合价变化的情况_____。
2SO2+CO2,其中化合价发生变化的元素是硫和氧两种元素,请分别表示出它们的化合价变化的情况_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如图1所示(已知氯化钙溶液呈中性;石灰石中的杂质不与酸反应,也不溶于水)。
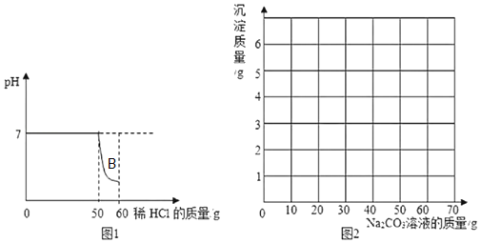
①图1中B点溶液中的溶质有_____(写化学式)。
②该小组同学能收集到的二氧化碳的质量是_____g,同时可得到CaCl2的质量为_____g。
③该小组同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | 0 | 1 | n | 3 | 4 | 5 | m |
则m=_____。加入10gNa2CO3溶液时发生反应的化学方程式是_____。
④请在图2中画出向滤液中加入Na2CO3溶液时产生的沉淀的质量随加入Na2CO3溶液的变化曲线_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象反映的变化规律与其对应操作不相符的是
A. 向氯化钠的饱和溶液中加入氯化钾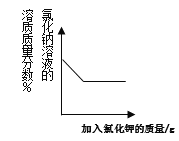
B. 向灼热的赤铁矿中通入CO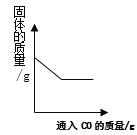
C. 向等质量的Al和Mg中加入足量的等质量等溶质质量分数的稀盐酸
D. 将饱和的氯化钠溶液恒温蒸发水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下列20℃时的实验和数据回答以下问题。
已知:20℃时,KCl和KNO3的溶解度分别为34g和31.6g;
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | KCl | KCl | KCl | KNO3 | KNO3 | |
固体的质量/g | 20 | 35 | 40 | 25 | 40 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
【1】①~⑤所得溶液属于不饱和溶液的是
A. ①②B. ②③C. ①④D. ③⑤
【2】下列关于①~⑤所得溶液的说法正确的是
A. 溶质质量:③ = ⑤
B. 溶液质量:③﹥②
C. 溶质质量分数:①<④
D. ⑤中溶质与溶剂的质量比为2:5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)冬天,北方菜农常在地客中保存蔬菜,小刚同学在学习化学知识后,知道蔬菜在一定条件下发酵生成气体,其成分可能含有CO2、CH4等,进入久未开启的菜窖可能造成死亡。于是他和化学兴趣小组的同学用如图装置对自家久未开启的菜窖内的气体成分进行了探究。
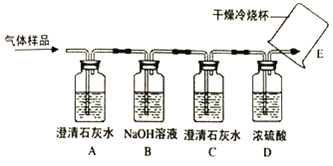
①若装置A中澄清石灰水变浑浊,证明气体样品中含有_____;
②装置B内发生反应的化学方程式为_____
③装置C的作用是_____;
④E处观察到干燥冷烧杯内壁有水珠出现,待火焰熄灭后,把烧杯迅速倒转过来,立刻向烧杯内倒入少量澄清石灰水并振荡,石灰水变浑浊,证明气体样品中含有_____。
(反思与评价)
⑤小强观察上述实验装置发现:装置A和装置C完全相同,他认为可以取消装置C,你是否认同,理由是_____
⑥根据上述实验探究结果,气体样品中含有CO2,由于二氧化碳_____,所以进入久未开启的菜窖前,应先敞开菜窖通风。
(2)某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊。为了弄清原因,他设计以下方案,进行探究、验证,请你帮他补充完整以下内容。
问题猜想 | 实验步骤 | 实验现象 | 实验结论 |
原因一:石灰水已完全变质 | 取少量未通入CO2的澄清石灰水于试管中向试管中滴加_____试剂。 | 溶液_____色 | 猜想正确 |
原因二:产生的CO2中带有HCl气体 | _____ | _____ | 猜想正确 |
请写出验证原因二的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究中和反应放热的问题进行了下列实验,回答有关问题。
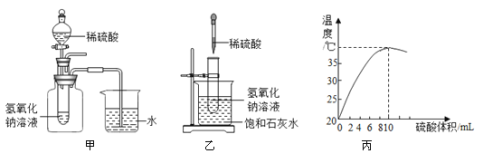
(1)实验甲,依据___现象证明该反应是放热的。
(2)实验乙,饱和石灰水出现了浑浊现象,其原因是___。
(3)丙图为向10mL10%的NaOH溶液中逐滴加入10%的稀硫酸的溶液温度数据,本实验用10%的NaOH溶液而未用NaOH固体的理由是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com