
【题目】某样品硝酸钾中含有一定质量的氯化钾.为了测定其中硝酸钾的质量分数做如下实验:取10g该样品加入58.87g水使其完全溶解,向溶液中逐滴加入硝酸银溶液至恰好完全反应,共用去34g硝酸银溶液;过滤、烘干称得沉淀为2.87g.根据实验计算:
(1)样品中硝酸钾的质量分数为多少_____?
(2)反应后所得溶液中溶质的质最分数为多少_____?
科目:初中化学 来源: 题型:
【题目】某同学为了研究在实验室中用某氯酸钾样品制取氧气的有关问题,他将5g氯酸钾样品与1g二氧化锰混合加热,在不同时刻测得部分数据如下表(友情提示:可把表中的空白补全后作答)。
加热时间 | t1 | t 2 | t3 | t4 |
剩余固体质量/g | 5.04 | 4.08 | ||
生成O2质量/g | 1.84 | 1.92 |
回答:
(1)t3时刻后,氯酸钾是否已经完全反应?_____。
(2)该样品中氯酸钾的质量分数_____。
(3)求t1时刻原氯酸钾中已分解的氯酸钾的质量分数____(写出解题过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】联欢会上,萌萌给同学们表演了魔术。她先向烧杯中倒入无水乙醇,将布手帕放入其中,完全浸透,取出手帕,轻轻挤干,用镊子夹住,从下方点燃,片刻后,手帕烧成灰烬(如图1所示)。之后,她向另一只烧杯中倒入白酒,取另一块材质、大小完全相同的手帕重复上述操作,火焰熄灭后,手帕依然完好如初(如图2所示)。已知:白酒由乙醇和水组成。

(1)白酒属于_____(填“混合物”或“纯净物”)。
(2)布手帕“烧不坏”的原因有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制取气体的常用装置,请结合图示回答下列问题。
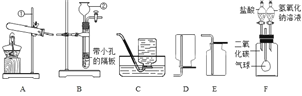

图 1 图2
(1)写出图 1 中标号②的仪器名称____。
(2)实验室制取并收集一瓶较纯净氧气,应选择图 1 的装置组合是____,该反应的化学方程式为_____________________________。
(3)实验室用石灰石和盐酸反应制取二氧化碳气体的化学反应方程式为___________,
某同学将制得的二氧化碳气体通入未变质的澄清石灰水中,未观察到明显现象,其可能的原因有____(合理即可)。
(4)图 1 装置 F 中的气球是“魔幻可变气球”。实验前,装置 F 中分液漏斗的活塞均处于关闭状态。打开____边(填“左”或“右”)分液漏斗的活塞并轻轻振荡集气瓶,可观察到气球变大。
(5)该活动小组用如图 2 所示装置,测量一定质量的塑料袋燃烧后产生 CO2的质量(该塑料袋充分燃烧只产生水和二氧化碳)。
①为了保证测量的准确性,连接好实验装置后应检查_____,再加 入药品进行实验。装置Ⅰ的小烧杯中加入过量 H2O2 和催化剂,可持续产生 O2 供塑料袋充分燃烧。
②塑料袋燃尽,装置Ⅰ逐渐冷却时,装置Ⅱ中的液体也不易倒吸进入装置Ⅰ中, 原因是____。
③根据实验目的,需要称量的是______(填字母)。(不考虑空气成分的影响)
A 实验前塑料袋的质量
B 实验前和实验后装置Ⅱ的质量
C 实验前和实验后装置Ⅲ的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组欲配制49g溶质质量分数为20%的稀硫酸来进行实验,老师为它们提供了溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)。
(1)通过计算,需要用到溶质质量分数为98%的浓硫酸的质量是____g。
(2)量取浓硫酸时仰视读数(其他操作正确),则配制的稀硫酸的溶质质量分数____(填“大于”、“小于”或“等于”) 20%。
(3)A和B是两个同学稀释浓硫酸操作的示意图,正确的是____(填“A”或“B”)。 . \ }
(4)玻璃棒搅拌的作用是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自来水厂常用氯气杀菌消毒,用明矾、氯化铁等净化水。以硫铁矿(主要成分是FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的流程如下图所示:
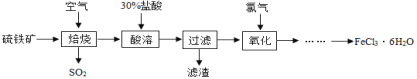
(1)“焙烧”前将硫铁矿进行粉碎,其目的是___。
(2)已知“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,写出该反应的化学方程式__。
(3)大量排放出SO2能形成酸雨,危害环境。常用下列方法除去:
方法1:将含SO2的废气通入氨水中,以减少空气污染,反应的化学方程式为:2SO2+4NH3H2O+O2=2__+2H2O。某兴趣小组测定了不同溶质质量分数的氨水在不同温度下吸收SO2气体的情况,获得如下图象,从实验数据可知,吸收SO2最佳的生产条件是__、__;

方法2:将含有二氧化硫的废气通入石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫。写出该反应的化学方程式____。
(4)流程中用30%盐酸“酸溶”焙烧后的残渣,写出化学方程式____;若在实验室欲用质量分数为37%(密度为1.18 g/ml)的盐酸配制30%的100g盐酸,则需要加水___g(保留1位小数),需要的玻璃仪器有烧杯、___、___胶头滴管等。
(5)“氧化”后从FeCl3溶液中获得FeCl3·6H2O晶体的操作方法是:在HCl气流中蒸发浓缩、____、过滤、洗涤、干燥。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】归纳是化学科学研究中常用的一种方法。在进行归纳之前。常需要以大量的实验事实作为基础。探究氧气的化学性质;如图所示,是探究氧气性质的一组实验,试回答下列问题:
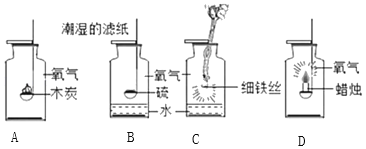
(1)A实验若要检验生成物,需要进行的操作是_____,发生反应的化学方程式为_____。
(2)B实验中潮湿的滤纸和水的共同作用是_____,将水换成氢氧化钠溶液效果更好,试推测可能的原因是_____。
(3)C实验中水的作用是_____。
(4)D实验中涉及的化学反应与其他三个反应有所不同,它属于_____(填“化合反应”或“氧化反应”)。
(5)以上实验将可燃物放入集满氧气的集气瓶中燃烧时均应该注意的一点实验操作是_____。
(归纳与交流)
①上述可燃物在氧气中燃烧通常比在空气中剧烈,说明氧气的化学性质比较_____(填“活泼”或“稳定”)。
②我们将上述物质与氧气的反应称为氧化反应,可以根据其反应的剧烈程度分为剧烈氧化(如燃烧)和缓慢氧化,下列变化属于缓慢氧化的是_____(填序号)。
A 动植物的新陈代谢
B 金属器皿的锈蚀
C 石油的分馏
D 食物的腐烂
E 有机肥的腐熟
F 煤的干馏
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列反应事实写出相应的化学方程式。
(1)酒精(C2H5OH)在足量氧气中完全燃烧_______。
(2)稀盐酸与铁锈(主要成分是氧化铁)反应_________。
(3)炼铁高炉内焦炭与二氧化碳反应____。
(4)铜丝与硝酸银溶液反应____。
(5)实验室用双氧水和二氧化锰制取氧气_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图甲、图乙所示。将图甲与图乙的阴影部分进行叠加,发现两者基本重合。下列有关分析错误的是
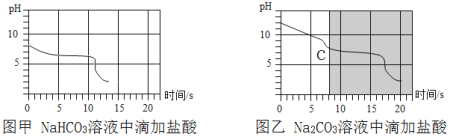
A. 图甲涉及反应的化学方程式为NaHCO3 + HCl = NaCl + H2O + CO2↑
B. 实验中所使用的NaHCO3溶液的碱性比Na2CO3溶液弱
C. 实验中碳酸氢钠、碳酸钠溶液完全反应,消耗的盐酸一样多
D. 图乙中c点对应溶液的溶质含有NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com