
【题目】豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(化学式为C6H13NO2)。下列关于亮氨酸的说法不正确的是( )
A. 亮氨酸由碳、氢、氮、氧四种元素组成
B. 一个亮氨酸分子由22个原子构成
C. 亮氨酸中碳元素的质量分数为27.3%
D. 亮氨酸中氢、氮两种元素的质量比为13:14
科目:初中化学 来源: 题型:
【题目】根据下图回答问题
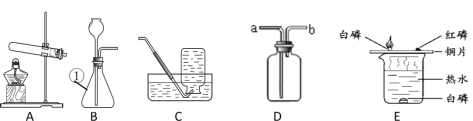
(1)仪器①的名称是__________。
(2)B与C连接制取气体,反应的化学方程式为________。
(3)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷气的发生装置应选用____(填字母)装置;收集甲烷气可选用C装置,由此推断甲烷气具有的物理性质是_______。
(4)用图D的装置排水法收集氧气。瓶中装入水的量应为___(选:“少量”、“多量”或“满瓶”),进气口为____(选“a”或“b”)。
(5)E装置用来探究燃烧的条件,由铜片上白磷燃烧而红磷不燃烧得出的结论______。
(6)在实验室制取二氧化碳的研究中,进行了如下实验:
药品 | 甲 | 乙 | 丙 | 丁 |
大理石 | 2g,块状 | 2g,块状 | 2g,粉末状 | 2g,粉末状 |
盐酸(过量) | 20g,10%盐酸 | 20g,20%盐酸 | 20g,10%盐酸 | 20g,20%盐酸 |
Ⅰ、若要研究盐酸浓度大小对反应的影响,可选择实验甲与______对照(选填实验编号)。
Ⅱ、研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是_____(填字母序号)
①反应更为剧烈 ②最终剩余溶液的质量更小
③产生的二氧化碳的质量更大 ④粉末状大理石利用率更高
A.① B.①④ C.①③④ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组对“一氧化碳还原氧化铁”的实验进行拓展研究。
(查阅资料)I.碳酸镁和锌能发生如下反应MgCO3+Zn![]() MgO+ZnO+CO↑
MgO+ZnO+CO↑
Ⅱ.氯化亚铜的氨水溶液能和CO反应,产生红色固体
(设计方案)根据上述资料设计如图实验装置(固定装置略,装置气密性良好):
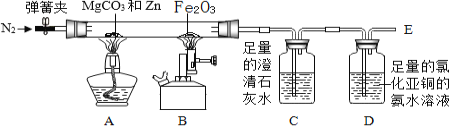
(实验步骤)①打开弹簧夹,通入适量氮气;②关闭弹簧夹,点燃A处酒精灯、B处酒精喷灯;③观察实验现象;④熄灭酒精灯和酒精喷灯。
(实验分析)(1)步骤①的目的是______;
(2)步骤③中,B处玻璃管内反应的化学方程式为_______,D装置的作用是_______。
(3)工业炼铁的产品为生铁,将5.8克生铁与94.6克稀盐酸恰好完全反应(杂质不溶于水,不与酸反应),烧杯中剩余物总质量为100.2克,求:①生成氢气的质量______;②反应后所得溶液中溶质的质量分数______。(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验课,同学们利用下列装置进行气体制备的学习。请你用已学的化学知识回答下列问题:
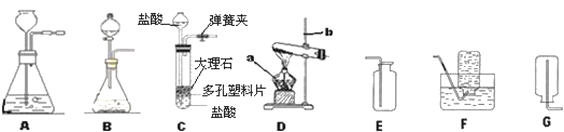
(1)图中仪器a的名称是 __________;
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,收集二氧化碳的装置是:___不用粉末状大理石的原因是_______,写出上述反应化学方程式____________。
(3)装置A、B和C都能制取二氧化碳气体,但装置C与前两者相比较,你认为装置C的优势是_____________。
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体.在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小。现实验室制取较纯净的甲烷应选用的装置的组合是_________(填字母编号)。
(5)某同学设计如图装置制取和收集氧气(向上排空气法和排水法),再进行相关实验。A瓶中发生反应的方程式为__________,滴入过氧化氢溶液,观察到A瓶中有气泡产生,C瓶中液面平稳下降,当C瓶中水正好排尽时,取出集气瓶B和C,盖上玻璃片。该同学应选择集气瓶_____(填“B”或 “C”)用于铁丝燃烧实验,另一瓶不合适的具体原因是_____________。
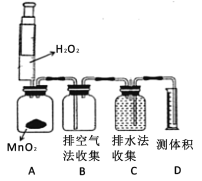
(6)若用氯酸钾和二氧化锰的混合物制氧气,反应的化学方程式为 ________反应前后二氧化锰在固体混合物中质量分数是_________ (“不变”或“变大”或“变小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验是科学探究的重要途径,请根据下列实验图示回答相关问题:
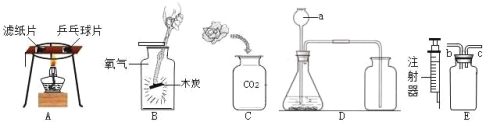
(1)图A 是燃烧条件的探究实验。将大小相同的滤纸片和乒乓球碎片放在薄铜片的两侧,加热铜片的中部,观察到_____(填“滤纸片”或“乒乓球碎片”)先燃烧。通过此现象说明燃烧的条件之一是_________
(2)图 B 是木炭在氧气中燃烧的实验示意图。操作方法是:把加热到红热的木炭_____(填“快速”或“缓慢”)伸入盛有氧气的集气瓶中;为进一步证明木炭与氧气发生了化学反应,继续进行的实验是_____
(3)在图 C集气瓶中,放入用石蕊溶液染成紫色的小花,小花一半干燥一半润湿。可观察的实验现象是_____, 此现象说明二氧化碳具有的化学性质是_____________
(4)用图 D 装置在实验室中制取二氧化碳,化学方程式为_________________。仪器 a 的名称为____________,用注射器可以代替仪器a,其优点是_____________
(5)用图 E 装置收集一瓶二氧化碳气体,请在图中将导管补画完整。证明该装置中二氧化碳收集满的方法是__________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】初中化学课本中的部分实验如下图。请你回答下列问题。

(1)图1是检查装置气密性的实验。将导管放入水中的目的是__________。
(2)图2是验证质量守恒定律的实验装置。在锥形瓶瓶塞上的玻璃管外端套一个瘪气球,瘪气球的作用是_____________。
(3)图3是过滤液体的实验。倒入液体时漏斗内液面要低于滤纸边缘,主要是为了防止_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
(实验目的)测定金属铁、铜和镁的活动性强弱。
(实验过程)
步骤Ⅰ 将铁片、铜片、镁片分别在空气中加热片刻,观察燃烧现象;
步骤Ⅱ 将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的稀硫酸的试管中;
步骤Ⅲ 将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的硝酸银溶液的试管中。
(实验记录)用“×”表示实验无明显现象,用“√”表示实验有明显现象,(见表);
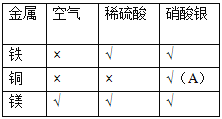
记录表A处应填写的现象是(1)________________,
该反应的化学方程式为(2)______________________。
(实验结论)由步骤Ⅰ和Ⅱ可判断金属铁、铜和镁的活动性由强到弱的顺序是(3)______________________;
(反思交流)小欣同学认为除了以上实验方案以外,在老师提供的药品中(金属已打磨):铁片、铜片、镁片、FeCl2溶液、CuCl2溶液、MgCl2溶液,只选三种药品也能达到实验目的,她选用的药品是(4)__________________________。(任写一种组合即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是
A. 硬水和软水的物质组成完全不同
B. 在煤炉上放一壶水就能防止一氧化碳中毒
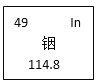
C. 从如图可知,铟元素的质子数为49,相对原子质量为114.8
D. 硫粉、铁丝、乙醇等物质都能与氧气发生剧烈的化合反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示加热铜丝引燃白磷测定空气中氧气的体积分数,相关说法正确的是( )
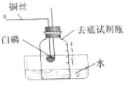
A. 用加热铜丝的方法引燃白磷,可以减小误差
B. 试剂瓶内液面上升至 1,证明氧气的质量分数约是 20%
C. 用木炭粉代替白磷也可达到实验目的
D. 若白磷过量,实验数据可能偏大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com