
分析 熟石灰为氢氧化钙,可以写出其化学式,根据化合物正负化合价的代数和为零,可以判断碘元素的化合价.
解答 解:熟石灰为氢氧化钙,其化学式Ca(OH)2;根据化合物正负化合价的代数和为零,可以设碘元素的化合价为x,则:+2+[x+(-2)×3]×2=0,.解得:x=+5,用于中和含有盐酸的废酸水,反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
故答案为:Ca(OH)2;+5;Ca(OH)2+2HCl═CaCl2+2H2O
点评 解答这类题目时,首先,要熟记和理解生石灰的性质与用途等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,按照题目的要求进行解答.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | BaCl2、Na2SO4、K2CO3、HNO3 | B. | NaOH、NaCl、石蕊、稀HCl | ||
| C. | AgNO3、NaCl、CaCl2、HNO3 | D. | CuSO4、NaCl、KOH、HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝是地壳里含量最多的元素,铝合金的密度一般都比较小 | |
| B. | 合金的硬度一般比组成它们的纯金属更高 | |
| C. | 铁在潮湿的空气中比在干燥的空气中更易生锈 | |
| D. | 在金属表面涂油漆能防止金属生锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验步骤 | 实验操作(说明仪器和试剂) | 实验现象 | 结论 |
| ① | 取少许粉末放入大试管中,再用滴管滴加足量(或过量)的NaOH溶液,充分反应后,静置,弃去清液得到固体. | 固体粉末部分溶解, 并有气泡放出. | 仅除去铝 |
| ② | 再往大试管中加足量(或过量)的稀硫酸(或稀盐酸),充分反应. | 固体部分溶解,气泡放出, 溶液呈浅绿色. | 证明含有铁 |
| ③ | 将大试管静置,弃去上层清液,加水,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
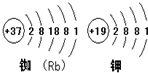 阅读下列材料,回答有关问题.
阅读下列材料,回答有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学中学习的很多化学物质之间存在反应关系,回答下列问题:
化学中学习的很多化学物质之间存在反应关系,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com