
【题目】请结合下图回答问题。
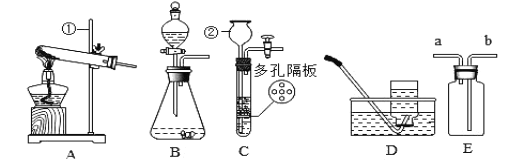
(1)仪器②的名称:________________。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置________________(选填序号)和装置D组合,反应的化学方程式为________________。若用B和D组合制取氧气,其反应的化学方程式为________________,若用E收集氧气,验满的方法是______________。
(3)实验室可用装置B或C制![]() ,C装置相对于B的优点有________________,用E装置收集
,C装置相对于B的优点有________________,用E装置收集![]() ,气体应从________________(选填“a”或“b”)端通入。
,气体应从________________(选填“a”或“b”)端通入。
(4)利用纯净干燥的氢气与下列装置测定碱式碳酸镍晶体(![]() )组成,准确称3.77g样品进行如下实验(假设每个装置试剂足量,反应均完全)。试回答如下问题:
)组成,准确称3.77g样品进行如下实验(假设每个装置试剂足量,反应均完全)。试回答如下问题:
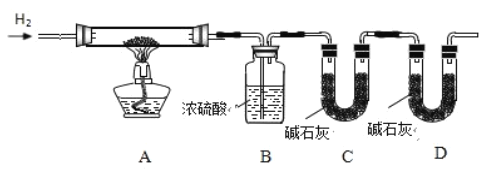
①装置C和D的作用分别是________________、________________。
②完全反应后装置A中得到1.77g金属,B增重1.62g、C增重0.44g。该样品中结晶水质量为_______________g,化学式为_______________。
③保持其他条件不变,仅将![]() 改为
改为![]() ,能否测定碱式碳酸镍的组成?________________(填“能”或“不能”)。
,能否测定碱式碳酸镍的组成?________________(填“能”或“不能”)。
【答案】长颈漏斗 A 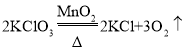
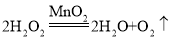 带火星的木条放在a导管口处,木条复燃,证明已满 能控制反应的发生与停止 a 吸收
带火星的木条放在a导管口处,木条复燃,证明已满 能控制反应的发生与停止 a 吸收![]() 防止空气中的
防止空气中的![]() 和
和![]() 从后面进入C中 0.72
从后面进入C中 0.72 ![]() 能
能
【解析】
(1)仪器②的名称长颈漏斗;
(2)用氯酸钾制氧气,反应物是固体,反应条件是加热,发生装置选用A;氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应的化学方程式为: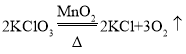 ;如果用双氧水和二氧化锰制氧气就不需要加热,若用B和D组合制取氧气所用药品是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为:
;如果用双氧水和二氧化锰制氧气就不需要加热,若用B和D组合制取氧气所用药品是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为: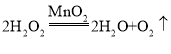 ;氧气的密度大于空气,若用E收集氧气,氧气应从b端通入,氧气具有助燃性,能使燃着的木条复燃,验满的方法是:把带火星的木条放在a处,木条复燃,证明氧气满了;
;氧气的密度大于空气,若用E收集氧气,氧气应从b端通入,氧气具有助燃性,能使燃着的木条复燃,验满的方法是:把带火星的木条放在a处,木条复燃,证明氧气满了;
(3)实验室可用装置B或C制H2,在装置C中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。反应后关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。C装置相对于B的优点有:可以控制反应的发生和停止;用E装置收集H2,气体应从短管进入,因为氢气的密度比空气小;
(4)①装置C和D的作用分别是:吸收生成的二氧化碳;防止空气中的二氧化碳和水蒸气进入;
②碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O。NiO与氢气反应生成Ni和水。完全反应后装置A中得到 1.77g 金属,该金属为Ni。
设:生成1.77g的镍,需NiO的质量为a,同时生成水的质量为b。
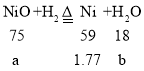
![]() a=2.25g
a=2.25g
![]() b=0.54g;
b=0.54g;
浓硫酸具有吸水性,B增重 1.62g是反应生成水的质量,碱式碳酸镍晶体受热会完全分解生成水的质量=1.62g-0.54g=1.08g,碱石灰能吸收二氧化碳,C增重 0.44g是反应生成的二氧化碳质量。
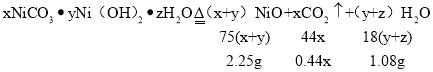
![]() y=2x
y=2x
![]() z=4x
z=4x
计算xNiCO3yNi(OH)2zH2O中x:y:z=1:2:4,所以化学式为;
=3.77g﹣1.77g﹣0.44g=1.56g;化学式为:NiCO3Ni(OH)24H2O;该样品中结晶水质量=![]() ;
;
③保持其他条件不变,仅将 H2改为 N2,可通过测定反应后A、B、C的质量,通过![]() 分解的化学方程式可计算出x、y、z的比值从而确定碱式碳酸镍的组成;
分解的化学方程式可计算出x、y、z的比值从而确定碱式碳酸镍的组成;


科目:初中化学 来源: 题型:
【题目】以下是在实验室里制取气体时常用的仪器,回答下列问题。
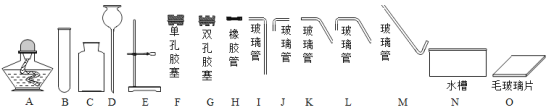
(1)加热高锰酸钾并用排水法收集氧气时,应从上述仪器中选择A、C、E、F、H、K、M、N、O和___组装制取装置,发生反应的化学方程式为____;
(2)从上述仪器中选择合适的组装也可以制取二氧化碳,若用73g10%稀盐酸与足量的大理石充分反应,能产生二氧化碳____g,检验二氧化碳需要的溶液是____;
(3)在实验室里,用块状碳化钙和水在常温下混合制取难溶于水的乙炔气体,组装的发生装置可以与上述制取____(选填“氧气”或“二氧化碳”)的一致。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是中学化学中常见物质的转化关系,A与B常温下反应放出大量热,A常温为液体,F与H组成元素相同,E是红色粉末(反应条件、部分反应物和生成物均已略去)。
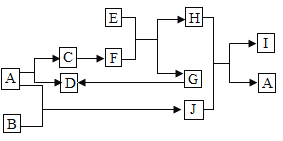
(1)A物质的化学式为_______________________;
(2)H的一种用途________________________;
(3)写出E+F→G+H的化学方程式_________________________;
(4)按物质的分类I属于__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
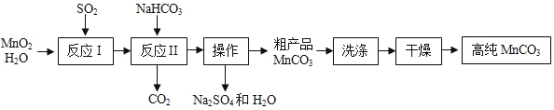
已知:①反应Ⅱ的化学方程式:MnSO4+2NaHCO3=Na2SO4+MnCO3↓+CO2↑+H2O
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解。
(1)反应Ⅰ的化学方程式为___________,属于基本反应类型中的_____________反应。
(2)流程中“操作”的名称为___________,所需要的主要玻璃仪器有烧杯、玻璃棒、____________。
(3)反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有___________(填化学式)。
(4)验证MnCO3粗产品是否洗净:取最后一次洗涤液,向其中加入适量的____________(填化学式)溶液,无白色沉淀产生,证明已经洗净。
(5)为获得高纯MnCO3,需选择“低温”干燥的原因是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水垢中一般含 CaCO3、Mg(OH)2,可能含有 MgCO3(不考虑其他任何杂质)。某同学取不含结晶水的水垢样品进行研究(过程如图),下列说法正确的是(相关物质相对分子质量:CaCO3 100 Mg(OH)2 58 MgCO3 84)( )
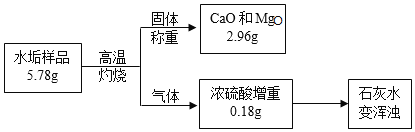
A. 该水垢灼烧生成 CO2气体 2.64 g
B. 该水垢中一定含有 CaCO3、Mg(OH)2,一定不含 MgCO3
C. 该水垢中一定含有 CaCO3、Mg(OH)2,可能含有 MgCO3
D. 该水垢中一定含有 CaCO3、Mg(OH)2和 MgCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有三瓶失去标签的无色溶液,已知分别是![]() 溶液、
溶液、![]() 溶液和
溶液和![]() 溶液中的各一种。下列四种试液中,能将上述三种无色溶液一次鉴别开来的是( )
溶液中的各一种。下列四种试液中,能将上述三种无色溶液一次鉴别开来的是( )
A.![]() 溶液B.酚酞试液
溶液B.酚酞试液
C.![]() 溶液D.
溶液D.![]() 溶液
溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有200g硫酸铜溶液的烧杯中,逐滴加入质量分数为8%的氢氧化钠溶液,产生沉淀的质量与所滴入![]() 溶液质量的关系曲线如图所示,请回答下列问题:
溶液质量的关系曲线如图所示,请回答下列问题:
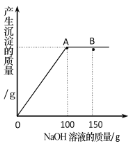
(1)反应过程中能看到的一项明显的现象是______________。
(2)上述反应恰好完全时,所得溶液呈_____________性(填“酸”、“碱”、“中”之一)。
(3)当加入氢氧化钠溶液至B点时,溶液中的溶质为(写化学式)_______。
(4)当加入氢氧化钠溶液至A点时,试通过计算,求此时烧杯中所得不饱和溶液的质量_______。(计算结果精确到0.1g)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是以空气和其他原料合成NH4NO3的工业流程。下列说法正确的是( )
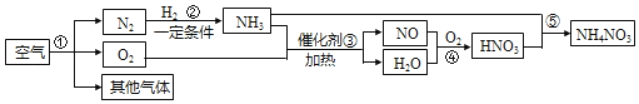
A. ①中发生的是物理变化
B. 上述流程中涉及到的化合反应只有2个
C. ③中参加反应的NH3和O2质量比为17:32
D. 理论上,若③和⑤中NH3的量相同,则合成NH4NO3时氨气的利用率最高
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶标签被腐蚀的盐酸,小红同学为了测定该溶液中溶质的质量分数.在烧杯中配制了8g10%的氢氧化钠溶液.然后往烧杯中滴加盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示,请回答下列问题:
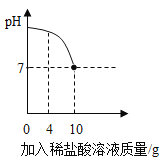
(1)该反应前后钠元素的质量保持不变,原因是________________.
(2)计算该盐酸的溶质质量分数__________(写出计算过程).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com