
| 商品名称 | 小苏打 | 食臭粉 | 混合碱性膨松剂 |
| 主要成分 | 碳酸氢钠 | 碳酸氢铵 | 碳酸氢钠和碳酸氢铵 |
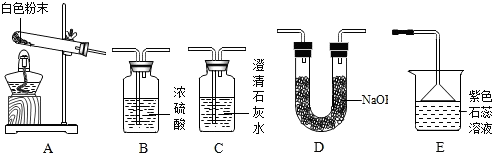
| 实验序号 | 实验装置 | 实验现象 | 实验结论及分析 |
| 实验1 | 选用A、B、C | C中澄清石灰水变浑浊 | 有CO2生成,C中反应的化学方程式是 CO2+Ca(OH)2═CaCO3↓+H2O |
| 实验2 | 选用A、 D和E | E中紫色石蕊溶液变成 蓝色 | 有NH3生成 |
| 实验序号 | 实验目的 | 实验装置 | 数据记录 | 实验结论 |
| 实验3 | 测定生成CO2的质量 | 选用A、B、D | 装置D增重a g | 该粉末为“混合碱性膨松剂” |
| 实验4 | 测定生成NH3的质量 | 选用A、B、D | 装置B增重1.7g |
分析 由题目的信息可知:选用A,B,C,C中澄清石灰水变浑浊,是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;选用A,D,E,D是吸收二氧化碳和水蒸气的,E是检验氨气的,氨气溶于水是氨水,氨水能使紫色石蕊试液变蓝色;实验3中装置B的作用是:除尽水蒸气和氨气,装置D增重的质量是二氧化碳的质量;如果装置B增重1.7g,因为碳酸氢铵受热分解生成一份氨气和一份二氧化碳,那么生成二氧化碳的质量是4.4g,又因为碳酸氢钠分解也生成二氧化碳,因此a大于4.4g;若测得a为92.4g,那么碳酸氢钠分解生成的二氧化碳的质量=92.4g-4.4g=88g,根据88g二氧化碳的质量求碳酸氢钠的质量,然后求NaHCO3与NH4HCO3的质量比.
解答 解:(1)【实验记录】选用A,B,C,C中澄清石灰水变浑浊,是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;选用A,D,E,D是吸收二氧化碳和水蒸气的,E是检验氨气的,氨气溶于水是氨水,氨水能使紫色石蕊试液变蓝色,故答案为:实验1 Ca(OH)2+CO2═CaCO3↓+H2O;实验2 D;蓝;
(2)【实验分析】实验3中装置B的作用是:除尽水蒸气和氨气,装置D增重的质量是二氧化碳的质量;如果装置B增重1.7g,因为碳酸氢铵受热分解生成一份氨气和一份二氧化碳,那么生成二氧化碳的质量是4.4g,又因为碳酸氢钠分解也生成二氧化碳,因此a大于4.4g;若测得a为92.4g,那么碳酸氢钠分解生成的二氧化碳的质量=92.4g-4.4g=88g,根据88g二氧化碳的质量求碳酸氢钠的质量,然后求NaHCO3与NH4HCO3的质量比;设生成88g二氧化碳需要碳酸氢钠的质量为x
2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
168 44
x 88g
$\frac{168}{x}$=$\frac{44}{88g}$
x=336g,因此NaHCO3与NH4HCO3的质量比=336g:7.9g=3360:79.
故答案为:(1)除尽水蒸气和氨气;(2)>4.4;(3)3360:79.
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| FeCl2溶液 | FeCl3溶液 | |
| 加入Fe粉 | 无明显变化 | 溶液变成浅绿色 |
| 加KSCN溶液 | 无明显变化 | 溶液变成红色 |
| 实验操作 | 实验现象 | 结论与解释 |
| ①取少量的黑色固体于试管中,滴加适量的稀盐酸 ②向步骤①所得的溶液中,滴加KSCN溶液 | 甲组: 固体溶解,无气泡冒出 加KSCN溶液后,溶液变成红色 | 甲组用CO还原Fe2O3反应的化学方程式是CO+3Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2 |
| 乙组: 固体溶解,有气泡冒出 加KSCN溶液后,溶液颜色无明显变化 | 黑色固体的成分是Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.
实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com