


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
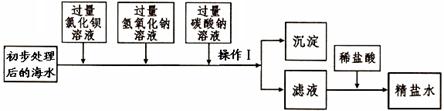
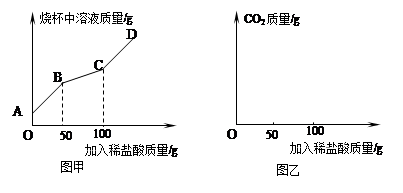

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.1﹕71 | B.2﹕71 | C.1﹕79 | D.2﹕79 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
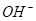 的数量有关;一定体积的溶液中
的数量有关;一定体积的溶液中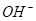 数量越多,则溶液的碱性越强。同体积的10%的NaOH溶液与10%的KOH溶液(溶液密度相同)相比,碱性更强的是
数量越多,则溶液的碱性越强。同体积的10%的NaOH溶液与10%的KOH溶液(溶液密度相同)相比,碱性更强的是| A.NaOH | B.KOH | C.一样强 | D.无法比较 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固体质量(g) | 8.5 | 6.9 | 6.7 | 6.7 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A. 1.3% | B. O.3% | C. 3% | D. 1.21% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com