
| 该原子的相对原子质量×该原子个数 |
| 该物质的相对分子质量 |
| 该原子的相对原子质量×该原子个数 |
| 该物质的相对分子质量 |
| 16×3 |
| 76 |
| 15g |
| 100g+200g |
| 100g×15%+100g×5% |
| 100g+100g |


科目:初中化学 来源: 题型:
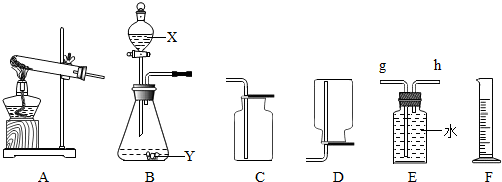
查看答案和解析>>
科目:初中化学 来源: 题型:
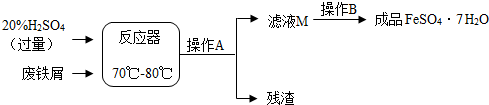
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | |||||||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
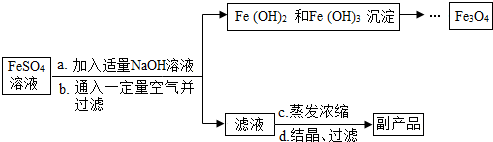
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 A、B、C、D、E、F均为初中化学常见的物质,它们之间有如图所示的反应关系,E是氧化物.请针对以下两种情况回答问题:
A、B、C、D、E、F均为初中化学常见的物质,它们之间有如图所示的反应关系,E是氧化物.请针对以下两种情况回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 能源与环境问题是当今社会备受关注的热点.
能源与环境问题是当今社会备受关注的热点.查看答案和解析>>
科目:初中化学 来源: 题型:
 铝的原子结构示意图如图所示,下列有关铝的叙述错误的是( )
铝的原子结构示意图如图所示,下列有关铝的叙述错误的是( )| A、铝原子的质子数为13 |
| B、铝的化学性质比较活泼 |
| C、铝是地壳中含量最多的元素 |
| D、化合物中铝元素通常显十3价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com