
| A. | 邻叔丁基苯酚的各元素质量比为10:14:1 | |
| B. | 邻叔丁基苯酚是由许许多多的离子构成 | |
| C. | 邻叔丁基苯酚溶于酒精形成的酒精溶液进行蒸馏,先变成蒸气分离出来的是邻叔丁基苯酚 | |
| D. | 邻叔丁基苯酚中的碳元素的质量分数为80% |
分析 根据物质的化学式可以计算组成元素的质量比、判断原子构成、计算组成元素的质量比多方面的问题.
解答 解:A、邻叔丁基苯酚的各元素质量比为:(12×10):(1×14):16=60:7:8,该选项说法不正确;
B、邻叔丁基苯酚是由分子构成的物质,该选项说法不正确;
C、邻叔丁基苯酚的沸点大于酒精的沸点,邻叔丁基苯酚溶于酒精形成的酒精溶液进行蒸馏,先变成蒸气分离出来的是酒精,该选项说法不正确;
D、邻叔丁基苯酚中的碳元素的质量分数为:$\frac{12×10}{(12×10)+(1×14)+16}$×100%=80%,该选项说法正确.
故选:D.
点评 邻叔丁基苯酚是由许许多多的邻叔丁基苯酚分子构成的,其中不含有离子,要注意理解.


 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:初中化学 来源: 题型:解答题
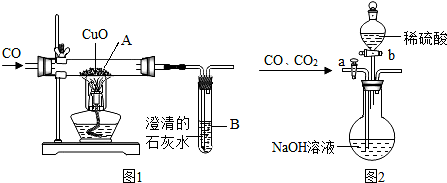
| 实验步骤 | 取少量该红色固体放入盛有稀硫酸的试管中,振荡 |
| 实验现象及结论 | 若溶液变蓝,则含有氧化亚铜,若溶液颜色不变,则不含有氧化亚铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 196g | B. | 49g | C. | 100g | D. | 98g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所用稀硫酸的质量/g | 60 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X3Y2 | B. | X3Y4 | C. | X2Y3 | D. | XY |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学活动小组探究金属的反应规律.
某化学活动小组探究金属的反应规律.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 现代生活中,人们越来越注意微量元素的摄入.血红蛋白中的铁是人体内氧的输送者,缺铁易患贫血.
现代生活中,人们越来越注意微量元素的摄入.血红蛋白中的铁是人体内氧的输送者,缺铁易患贫血.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com